Proteină
Cele Proteinele au fost definite ca macromolecule prezente biologice in toate celulele vii , dar studiile recente arată că există , de asemenea , sute , daca nu mii de micro- sau nano-proteine. Acestea sunt formate dintr-unul sau mai multe lanțuri polipeptidice . Fiecare dintre aceste lanțuri este compus din secvența de reziduuri de aminoacizi legați între ei prin legături peptidice .
Proteinele îndeplinesc o multitudine de funcții în interiorul celulelor vii și în țesuturi . Sunt proteine enzimatice ( enzime ) care catalizează sinteza chimică și reacțiile de degradare necesare pentru metabolismul celulei. Alte proteine oferă un rol structural în cadrul citoscheletului sau țesuturilor ( actină , colagen ), unele sunt motoare moleculare care permit mobilitatea ( miozina ), altele sunt implicate în condiționarea ADN-ului ( histone ), reglarea expresiei genelor ( factori de transcripție ), energie metabolismul ( ATP sintaza ) sau transmiterea semnalelor celulare ( receptori de membrană ).
Lanțurile proteice sunt sintetizate în celulă de către ribozomi , din informațiile codificate în gene , care determină ordinea în care sunt legați cei 22 de aminoacizi, numiți proteinogeni , care sunt încorporați direct în timpul biosintezei genelor . Secvența de aminoacizi se numește secvență polipeptidică. Din modificările post-translaționale pot interveni apoi odată proteina sintetizată, care poate avea ca efect modificarea proprietăților fizice sau chimice. Este, de asemenea, obișnuit ca moleculele neproteice, numite grupe protetice , să se lege stabil de proteine și să contribuie decisiv la funcțiile lor biologice: acesta este de exemplu cazul hemului din hemoglobină , fără de care această proteină nu ar putea transporta oxigen în sânge .
Proteinele adoptă o structură tridimensională care le permite să își îndeplinească funcția biologică. Această structură specială este determinată mai ales de secvența lor de aminoacizi, ale cărei proprietăți fizico-chimice conduc lanțul proteic să adopte o pliere stabilă.
În laborator, aceștia pot fi separați de alți constituenți celulari folosind diverse tehnici, cum ar fi ultracentrifugarea , precipitația , electroforeza și cromatografia . Inginerie genetica a introdus o serie de metode pentru a facilita purificarea proteinelor. Structura lor poate fi studiată prin imunohistochimie , mutageneză direcționată către sit , cristalografie cu raze X , rezonanță magnetică nucleară și spectrometrie de masă .
Proteinele sunt o componentă importantă a animalului alimentar , sunt degradate în tractul digestiv și aminoacizii eliberați sunt apoi reutilizați de către organism.
facem diferența între proteinele complete și proteinele incomplete. O proteină completă conține toți cei nouă aminoacizi esențiali, în timp ce o proteină incompletă găsită în alimentele de origine vegetală nu le conține pe toți.
Etimologie
Proteinele au fost descoperite din 1835 în Olanda de către chimistul organic Gerardus Johannes Mulder (1802-1880), sub numele de wortelstof . A fost ilustrul său coleg suedez, Jöns Jacob Berzelius , care i-a sugerat numele de proteină în 1838 .
Termenul de proteină provine din grecescul antic prôtos care înseamnă mai întâi , esențial . Acest lucru se referă probabil la faptul că proteinele sunt esențiale pentru viață și constituie adesea majoritatea (parte 60%) din greutatea uscată a celulelor (animale). O altă teorie este că proteina se referă, la fel ca adjectivul protean, la zeul grec Proteus care ar putea schimba forma după bunul plac . Proteinele iau multe forme și îndeplinesc funcții multiple. Dar acest lucru nu a fost descoperit până mult mai târziu, în timpul XX - lea secol .
Biochimie
Proteinele sunt formate dintr-unul sau mai multe lanțuri polipeptidice , care sunt biopolimeri liniari, pot fi destul de lungi, compuse dintr-un douăzeci de acizi L -α-amino diferiți. În general, vorbim de proteine cu mai mult de cincizeci de reziduuri în moleculă și de peptidă cu până la câteva zeci de reziduuri.
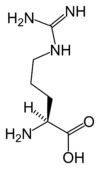
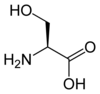
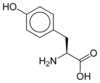
Toți aminoacizii proteinogeni - cu excepția prolinei - au o structură comună constând dintr-o funcție acid carboxilic , o amină primară pe carbonul α și un lanț lateral . Acesta din urmă are o foarte mare varietate de structuri chimice și este efectul combinat al tuturor acestor lanțuri laterale ale unui lanț polipeptidic care determină structura tridimensională, precum și proprietățile chimice ale acestuia din urmă. Tabla de mai jos prezintă structura chimică a celor 22 de aminoacizi proteinogeni:
|
Structura a 22 de aminoacizi proteinogeni . Pirolizina și selenocisteină (peste greyed) sunt specifice pentru anumite proteine : - pentru pirolizina găsit doar în unele archaeal metanogene , - pentru selenocisteină este prezentă și printre eucariotelor , ci a priori în zeci de enzime de familie de oxidoreductaze . Ceilalți 20 de aminoacizi, numiți standarde, sunt pe de altă parte distribuiți universal în toate ființele vii cunoscute. |
Aminoacizii dintr-un lanț polipeptidic sunt legați între ei prin legături peptidice care se stabilesc între carboxil –COOH al unui prim aminoacid și amina primară –NH 2 o secunda:
Coloana vertebrală a proteinei este astfel formată dintr-un lanț liniar de aminoacizi la care lanțurile laterale sunt conectate și legate prin legături peptidice. Legătura peptidică are două forme de rezonanță care îi conferă parțial proprietățile unei legături duble , care limitează rotațiile în jurul axei sale, astfel încât cei patru atomi ai grupului amidic ((C = O) NH- sunt întotdeauna aproximativ coplanari . Celelalte două legături care constituie coloana vertebrală a aminoacidului, pe de altă parte, se pot roti liber. Cele două unghiuri diedre corespunzătoare acestor două legături interne determină geometria locală adoptată de lanțul proteic.
Capătul carboxil al lanțului lateral polipeptidic se numește capătul C -terminal , în timp ce partea amină se numește capătul N -terminal . Cuvintele proteină, polipeptidă și peptidă sunt destul de ambigue și semnificațiile lor se pot suprapune. În general, vorbim de proteine cu referire la molecula biologică completă dotată cu o conformație stabilă, în timp ce o peptidă desemnează, în general, o moleculă mai scurtă, fără o structură tridimensională stabilă. Linia dintre cele două este foarte imprecisă și este în jur de câteva zeci de reziduuri de aminoacizi.
Mărimi
S-a crezut întotdeauna că proteinele sunt mari (la scări biomoleculare); a existat un sens din anii 1980 și am știut de la începutul anilor 1990 că acest lucru nu a fost cazul, ca urmare a descoperirii unul, apoi de alte câteva MicroProteins (numite uneori MIPS ). De atunci, oamenii de știință au demonstrat existența a sute și apoi a mii de microproteine și nanoproteine (uneori asociază doar câțiva aminoacizi, poate auto-asamblați), atât de mici încât sistemele clasice de analiză genomică nu le-au putut observa. Se pare că au roluri cheie în cadrul celulelor din complexul proteic , prin interacțiunea în relațiile proteină-proteină. Unii controlează astfel activitatea proteinelor mai mari, jucând un rol de regulatori post-translaționali, fără a interacționa direct cu ADN sau ARN. Alții promovează dezvoltarea musculară și reglează contracția musculară . Alții contribuie la gestionarea deșeurilor intracelulare (ARN vechi, degradat sau defect). La plante, acestea ar putea participa la detectarea luminii și, în alte cazuri, pot juca un rol în semnalizarea fitohormonală . La animale, ei participă la funcționarea ceasului biologic .
Se găsește în special în veninuri (de la păianjeni , scorpioni și alte animale otrăvitoare ). Nanoproteinele complexe pot fi create in vitro prin auto- asamblare a aminoacizilor ; ar putea fi folosite pentru recunoașterea și cataliza biomoleculare. S-a dovedit deja că sunt de interes comercial: unele insecticide îl folosesc. Acestea prezintă interes medical: sunt utilizate pentru a marca tumorile cerebrale pentru a permite o intervenție chirurgicală mai precisă.
Structura
Natura proteinelor este determinată mai ales de secvența lor de aminoacizi, care constituie structura lor primară . Aminoacizii având proprietăți chimice foarte diverse, dispunerea lor de-a lungul lanțului polipeptidic determină dispunerea lor spațială. Aceasta este descrisă local prin structura lor secundară , stabilizată prin legături de hidrogen între resturile de aminoacizi învecinate și la nivel global prin structura lor terțiară , stabilizată de toate interacțiunile dintre reziduuri - uneori foarte îndepărtate pe secvența peptidică, dar aduse în contact spațial prin pliere a proteinei - precum și între proteina însăși și mediul său. În cele din urmă, asamblarea mai multor subunități proteice pentru a forma un complex funcțional este descrisă de structura cuaternară a acestui set.
Legături covalente suplimentare se pot forma, de asemenea, fie în cadrul aceluiași lanț proteic, fie între diferite lanțuri peptidice din cadrul unei proteine, în special prin formarea de punți disulfidice între reziduurile de cisteină .
Majoritatea proteinelor adoptă o conformație tridimensională unică. Forma naturală a unei proteine in vivo este starea sa nativă , care este forma pe care o ia pentru a fi biologic activă și funcțională. Multe proteine sunt ele însele active din punct de vedere biologic sub efectul distribuției spațiale a reziduurilor de aminoacizi care le constituie, altele trebuie să fie ajutați în acest sens prin proteine chaperone pentru a fi pliate în funcție de starea lor nativă.
Niveluri de organizare
În biochimie , prin urmare, putem distinge patru niveluri de organizare pentru a descrie structura proteinelor:
- Structura primară corespunde secvenței de aminoacizi.
- Structura secundară descrie dispunerea reziduurilor de aminoacizi observabile la scară atomică. Stabilizate prin legături de hidrogen , aceste aranjamente locale sunt de exemplu elici α , foile β , butoaiele β sau coate. Există mai multe soiuri și este comun ca o proteină să aibă mai multe tipuri de structuri secundare în ansamblu.
- Structura terțiară corespunde formei generale a proteinei observabilă pe scara întregii molecule. Descrie interacțiunile dintre diferitele elemente ale structurii secundare. Acesta este stabilizat de un întreg set de interacțiuni care conduc cel mai adesea la formarea unui miez hidrofob , posibil cu legături de sare , legături de hidrogen, punți disulfură sau chiar modificări post-translaționale . O structură terțiară este adesea denumită plierea unei proteine.
- Structura cuaternară descrie complexul rezultat din asamblarea mai multor molecule proteice (mai multe lanțuri polipeptidice), numite în acest caz subunități proteice pentru a forma un singur complex proteic. Toate proteinele nu constă neapărat din mai multe subunități și, prin urmare, nu au întotdeauna o structură cuaternară.
Proteinele nu sunt molecule complet rigide. Este probabil să adopte mai multe conformații conexe în timp ce își îndeplinesc funcțiile biologice. Trecerea de la una dintre aceste conformații la alta se numește schimbare conformațională . În cazul unei enzime, de exemplu, astfel de modificări conformaționale pot fi induse prin interacțiunea cu substratul la nivelul situsului activ . În soluție, proteinele suferă, de asemenea, multe modificări conformaționale datorate vibrației termice a coliziunii cu alte molecule.
Implicații biologice și determinarea structurilor terțiare și cuaternare
Există trei grupuri majore de proteine în funcție de structura terțiară sau cuaternară: proteinele globulare , proteinele fibroase și proteinele de membrană . Aproape toate proteinele globulare sunt solubile și sunt adesea enzime . Proteinele fibroase joacă adesea un rol structural, precum colagenul , principalul constituent al țesutului conjunctiv sau keratina , un constituent proteic al părului și al unghiilor . Proteinele de membrană sunt adesea receptori sau canale care permit moleculelor polare sau încărcate electric să treacă prin membrană .
Cunoașterea structurii terțiare sau chiar cuaternare a unei proteine poate oferi informații importante pentru înțelegerea modului în care această proteină își îndeplinește funcția biologică. Cristalografie cu raze X și spectroscopie RMN sunt metode experimentale comune structura proteinei de studiu, care poate unul și celălalt furnizând informații cu o rezoluție la scala atomica . Datele RMN oferă informații din care este posibil să se estimeze un subset de distanțe între anumite perechi de atomi, ceea ce face posibilă deducerea posibilelor conformații ale acestei molecule. Interferometria dublă polarizare este o metodă analitică cantitativă pentru măsurarea conformația globală a proteinei și a modificărilor conformaționale în funcție de interacțiunea cu alți stimuli. Dicroismul circular oferă o altă tehnică de laborator pentru rezolvarea anumitor elemente ale structurii secundare a proteinelor ( spiralele alfa și foi p particular). Crio-microscopie electronică furnizează informații structurale la rezolutie minima pe proteine foarte mari, inclusiv viruși . Cristalografie de electroni (în) , capătul tehnic al precedent, permite , în unele cazuri , de asemenea , produc date de mare rezoluție, în special pentru cristalele bidimensionale ale proteinelor membranare . Structurile proteice rezolvate sunt în general depozitate în Protein Data Bank (PDB), o bază de date cu acces deschis care oferă structura a o mie de proteine pentru care sunt disponibile coordonatele carteziene ale fiecărui atom.
Numărul de proteine a căror structură a fost rezolvată este mult mai mic decât numărul de gene a căror secvență este cunoscută. În plus, subsetul de proteine a căror structură a fost rezolvată este influențat în favoarea proteinelor care pot fi ușor pregătite pentru analiză prin cristalografie cu raze X, una dintre principalele metode de determinare a structurilor proteinelor. În special, proteinele globulare sunt comparativ cele mai ușor de cristalizat pentru cristalografie, în timp ce proteinele de membrană sunt mai dificil de cristalizat și sunt subreprezentate printre proteinele disponibile în PDB. Pentru a remedia această situație, au fost întreprinse abordări de genomică structurală pentru a rezolva structurile reprezentative ale principalelor clase de pliere a proteinelor . Metodele de predicție a structurii proteinelor își propun să ofere mijloacele pentru a genera structura plauzibilă a unei proteine din structuri care ar putea fi determinate experimental.
Sinteză
A -amino proteinogenii acizi sunt asamblați în polipeptide din celule de către ribozomi din informațiile genetice transmise de ARN-ul mesager din ADN - ul care conține genele . Este secvența nucleotidică a ADN-ului, transcrisă identic în ARN-ul mesager, care transportă informațiile citite de ribozomi pentru a produce proteine în conformitate cu secvența peptidică specificată de gene. Corespondența dintre secvența nucleotidică a ADN-ului și ARN-ul mesager pe de o parte și secvența peptidică a proteinelor sintetizate pe de altă parte este determinată de codul genetic , care este în esență același pentru toate viețuitoarele cunoscute, cu excepția unui număr destul de limitat de variații.
Cod genetic
Codul genetic stabilește corespondența dintre un triplet de baze nucleici , numit un codon , pe mesager ARN și o proteinogenici α-amino acizi. Această corespondență este realizată in vivo de ARN-urile de transfer , care sunt ARN-uri care conțin cel mult o sută de nucleotide și care poartă un aminoacid care le esterifică capătul 3'-OH. Fiecare dintre aminoacizii este legat de ARN-uri de transfer specifice, purtând, de asemenea, codoni specifici, astfel încât fiecare dintre cei 64 de codoni posibili poate codifica doar un aminoacid. Pe de altă parte, fiecare dintre cei 22 de aminoacizi proteinogeni poate fi codificat de mai mulți codoni diferiți. Acesta este enzimele care efectuează esterificarea RNAs mesager cu aminoacizi - sintetaze aminoacil-ARNt - care mențin codul genetic. De fapt, aceste enzime leagă în mod specific atât la un anumit transfer ARN și la un aminoacid dat, astfel încât fiecare tipul de ARN de transfer este esterificat doar cu un aminoacid specific.
Cazul selenocisteinei și pirolizinei este oarecum diferit prin faptul că acești aminoacizi nu sunt codificați direct de codoni specifici, ci prin recodarea translațională a codonilor de oprire în prezența unor secvențe de inserție particulare numite elementul SECIS și respectiv elementul. PYLIS , care recodifică UGA (Opal) și UAG (Chihlimbar) opresc codonii în selenocisteină și, respectiv, pirolizină. În plus, selenocisteina nu este legată ca atare de ARN-ul său de transfer, deoarece este prea reactivă pentru a exista liber în celulă; este serina care este legată de un ARNt ARN Sec de transfer de selenocisteină de către serina tARN AR ligază . Seril - tARN Sec nu poate fi utilizat de ribozomi , deoarece nu este recunoscut de către factorii de alungire implicate în biosinteza proteinelor , astfel încât serina poate fi încorporat în selenoproteins în loc de selenocysteine. In contrast, seril-ARNt Sec este un substrat pentru anumite enzime care transformarea sa în sélénocystéinyl - ARNt Sec : conversie directă de către selenocisteină sintaza în bacterii , conversia indirectă prin O -phosphoséryl -ARNt Sec succesiv de O - phosphoseryl-ARNt Sec kinază și O -fosfoseril-ARNt: selenocisteinil-ARNt sintază în arhee și eucariote .
Genele codificate în ADN sunt în primul rând transcrise în ARN pre-mesager de către enzime precum ARN polimeraze . Majoritatea ființelor vii modifică acest ARN pre-mesager printr-un set de procese numite modificări post-transcripționale care duc la ARN mesager matur. Acesta din urmă poate fi apoi utilizat de ribozomi pentru a servi drept model în timpul biosintezei proteinelor . În procariote , ARN-ul mesager poate fi utilizat de îndată ce este sintetizat sau poate fi tradus în proteine după părăsirea nucleoidului . În schimb, în eucariote , ARN-ul mesager este produs în nucleul celulei, în timp ce proteinele sunt sintetizate în citoplasmă , astfel încât ARN-ul mesager trebuie să traverseze membrana nucleară .
Biosinteza
Biosinteza unei proteine dintr-un ARN mesager este traducerea acestui ARNm. ARN-ul Messenger se leagă de ribozom, care îl citește secvențial la trei nucleotide în fiecare etapă de sinteză. Fiecare triplet de nucleotide constituie un codon pe ARN-ul mesager, la care se poate lega anticodonul unui ARN de transfer care furnizează aminoacidul corespunzător. Asocierea dintre codonul și anticodon se bazează pe complementaritatea dintre lor respective secvențe . Această complementaritate asigură recunoașterea între ARN-ul de transfer și codonul ARN-ului messenger. Aminoacidul furnizat de ARN de transfer pe ribozomului stabilește o legătură peptidică cu C aminoterminal capătul lanțului în formare, ceea ce îi permite să fie prelungită cu un rest de aminoacid. Ribozomul mută apoi trei nucleotide pe ARN-ul mesager pentru a înfrunta un nou codon, care urmează exact codonul anterior. Acest proces se repetă până când ribozomul se află în fața unui codon de oprire , caz în care se oprește traducerea.
Biosinteza unei proteine este efectuată și reziduul după reziduu, capătul N- terminal până la capătul C- terminal . Odată sintetizată, proteina poate suferi diverse modificări post-translaționale, cum ar fi clivarea , fosforilarea , acetilarea , amidarea , metilarea , glicozilarea , lipidarea sau chiar formarea de legături disulfură . Mărimea proteinelor astfel sintetizate este foarte variabilă. Această dimensiune poate fi exprimată în număr de aminoacizi reziduuri acide constituie aceste proteine, precum și în daltoni (simbol Da), care în biologia moleculară corespunde la unitatea de masă atomică . Deoarece proteinele sunt adesea molecule destul de mari, masa lor este adesea exprimată în kilodaltoni (simbol kDa). De exemplu, proteinele de drojdie au o lungime medie de 466 reziduuri de aminoacizi, pentru o masă de 53 kDa . Cele mai mari proteine cunoscute sunt titins ale sarcomers formează myofibrils ale mușchilor scheletici striați : mouse - ul Titin conține unele 35213 resturi de aminoacizi formate din 551,739 atomi cu o masă de peste 3.900 kDa și o lungime l de ordinul 1 pm .
Sinteza chimică
Proteinele mici pot fi, de asemenea, sintetizate in vitro printr-o varietate de metode cunoscute de sinteză peptidică , care se bazează pe tehnici de sinteză organică, cum ar fi ligarea chimică (in) pentru a produce în mod eficient peptide. Sinteza chimică face posibilă introducerea aminoacizilor nenaturali în lanțul polipeptidic, de exemplu prin plasarea sondelor fluorescente pe lanțul lateral al unora dintre ele. Aceste metode sunt utile în laborator în biochimie și biologie celulară, dar nu sunt utilizate în general pentru aplicații comerciale. Chimice de sinteză nu este eficient la sintetizarea peptidelor cu mai mult de aproximativ 300 de amino reziduuri acide, iar proteinele produse astfel nu își poate asuma cu ușurință lor nativă structura terțiară . Majoritatea metodelor de sinteză chimică a proteinelor se desfășoară de la capătul C- terminal până la capătul N- terminal , adică în direcția opusă biosintezei proteinelor de către ribozomi .
Funcții
Printre toți constituenții celulei, proteinele sunt cele mai active elemente. În afară de unele ARN-uri , majoritatea celorlalte molecule biologice nu sunt suficient de reactive chimic și proteinele acționează asupra lor. Proteinele reprezintă aproximativ jumătate din substanța uscată a unei celule E. coli , în timp ce ARN-ul și ADN - ul reprezintă un al cincilea și, respectiv, 3%. Toate proteinele exprimate într-o celulă constituie proteomul său .
Principala caracteristică a proteinelor care le permite să își îndeplinească funcțiile biologice este capacitatea lor de a se lega de alte molecule într-un mod foarte specific și foarte strâns. Regiunea unei proteine care se leagă de o altă moleculă este locul său de legare, care adesea formează o depresiune, cavitate sau „buzunar” în suprafața moleculei. Este structura terțiară a proteinei și natura chimică a catenelor laterale ale resturilor de aminoacizi ale situsului de legare care determină specificitatea acestei interacțiuni. Siturile de legare pot duce la legături deosebit de specifice și strânse: astfel, inhibitorul ribonucleazei se leagă de angiogenina umană cu o constantă de disociere sub-femtomolară ( <10 -15 mol L -1 ), dar nu se leagă deloc de Ranpirnaza , omologă a amfibian al acestei proteine (constantă mai mare de 1 mol L -1 ). O ușoară modificare chimică poate modifica radical capacitatea unei molecule de a interacționa cu o anumită proteină. Astfel, aminoacil-ARNt sintetaza specifică pentru valină se leagă de aceasta din urmă fără a interacționa cu izoleucina , care este totuși structural foarte apropiată de aceasta.
Proteinele se pot lega de alte proteine sau de molecule mici ca substraturi . Când se leagă în mod specific de alte proteine care sunt identice cu ele însele, se pot polimeriza pentru a forma fibrile . Acest lucru este comun pentru proteinele structurale, formate din monomeri globulari care se auto-asamblează pentru a forma fibre rigide. Dintre interacțiunile proteină-proteină, de asemenea, reglează activitatea enzimei , progresul ciclului celular și asamblarea complexelor proteice mari realizând partajarea reacțiilor strâns legate de o funcție biologică comună. Proteinele se pot lega, de asemenea, de suprafața membranelor celulare și adesea chiar devin o parte integrantă a acestora. Capacitatea anumitor proteine de a schimba conformația atunci când se leagă de molecule specifice permite construirea unor rețele de semnalizare celulară extrem de complexe. În general, studiul interacțiunilor dintre proteinele specifice este un element cheie în înțelegerea noastră a modului în care funcționează celulele și a capacității lor de a schimba informații.
Enzime
Cea mai mare parte vizibilă a proteinelor din celula este cea a enzimei , adică biomolecule catalizând a reacțiilor chimice . Enzimele sunt în general foarte specifice și accelerează doar una sau câteva reacții chimice. Marea majoritate a reacțiilor chimice din metabolism sunt efectuate de enzime. În plus față de metabolism, aceștia din urmă sunt de asemenea implicate în expresia genelor , replicarea ADN - ului , ADN repararea , transcriere a ADN în ARN , și traducerea de ARN mesager in proteine. Unele enzime lucrează pe alte proteine pentru a lega sau a scinda anumite grupări funcționale și resturi ale altor biomolecule din ele, într-un proces numit modificare post-translațională . Enzimele catalizează peste 5.000 de reacții chimice diferite. La fel ca toți catalizatorii, aceștia nu modifică echilibrele chimice, ci accelerează reacțiile, uneori în proporții considerabile; astfel, orotidina-5'-fosfat decarboxilaza catalizează în milisecunde o reacție care altfel ar dura câteva milioane de ani.
Moleculele care se leagă de enzime și sunt modificate chimic de acestea se numesc substraturi . Deși uneori enzimele constau din câteva sute de reziduuri de aminoacizi, doar câteva dintre ele intră în contact cu substratul (ele) enzimei, iar un număr foarte mic - de obicei trei sau patru - sunt direct implicați în cataliză. Situl activ este regiunea unei enzime implicate în reacția chimică catalizată de această proteină: grupează împreună reziduurile care se leagă de substrat sau contribuie la poziționarea acestuia, precum și reziduurile care catalizează direct reacția.
Semnalizarea celulară și legarea ligandului
Multe proteine sunt implicate în mecanismele de semnalizare celulară și de transducție a semnalului . Anumite proteine precum insulina aparțin mediului extracelular și transmit un semnal din celulă unde sunt sintetizate către alte celule situate uneori în țesuturile îndepărtate. Altele sunt proteine de membrană care acționează ca receptori a căror funcție principală este de a se lega de moleculele care poartă semnale și de a induce un răspuns biochimic în celula țintă. Mulți receptori de membrană au un situs de legare expus la exteriorul celulei și un efector de câmp (en) în contact cu mediul intracelular. Acest domeniu efector poate avea o activitate enzimatică sau poate suferi modificări conformaționale care acționează asupra altor proteine intracelulare.
De Anticorpii sunt componente proteice ale sistemului imunitar , a cărui funcție principală este de a se lega la antigene sau xenobiotice pentru a le marca pentru eliminarea din organism. Anticorpii pot fi secreti în mediul extracelular sau ancorați în membrana plasmatică a limfocitelor B specializate numite celule plasmatice . Acolo unde enzimele sunt foarte specifice pentru substraturile lor pentru a accelera reacții chimice foarte precise, anticorpii nu au această constrângere; pe de altă parte, afinitatea lor pentru ținta lor este extrem de mare.
Multe proteine transportoare de liganzi se leagă în mod specific de molecule mici și le transportă la destinațiile lor prin celulele și țesuturile organismelor multicelulare . Aceste proteine trebuie să aibă o afinitate ridicată pentru ligandul lor atunci când concentrația acestuia este ridicată, dar trebuie, de asemenea, să fie capabile să o elibereze atunci când concentrația sa este scăzută în țesuturile țintă. Exemplul canonic al proteinei purtătoare de ligand este hemoglobina , care transportă oxigenul din plămâni către alte organe și țesuturi din toate vertebratele și are omologi înrudiți în toate regatele vii. Cele lectine sunt proteine care se leagă reversibil la anumiți carbohidrați cu specificitate foarte mare. Acestea joacă un rol în fenomenele de recunoaștere biologică care implică celule și proteine.
De proteine transmembranare pot juca , de asemenea , rolul de proteină ligand transportor poate modifica permeabilitatea membranei celulare a moleculelor mici polare și ioni . Membrana în sine are un miez hidrofob prin care moleculele polare sau încărcate electric nu se pot difuza. Proteinele de membrană pot conține astfel unul sau mai multe canale prin membrana celulară și permițând acestor molecule și acestor ioni să o traverseze. Multe canale ionice sunt foarte specifice ionului pe care îl circulă. Astfel, canalele de potasiu și canalele de sodiu sunt deseori specifice pentru unul dintre cei doi ioni de potasiu și sodiu, cu excepția celuilalt.
Proteine structurale
Proteinele structurale conferă rigiditate și rigiditate constituenților biologici care, fără ele, ar fi fluide. Majoritatea proteinelor structurale sunt fibroase. Acesta este, de exemplu, cazul colagenului și elastinei, care sunt constituenți esențiali ai țesuturilor conjunctive, cum ar fi cartilajul și cheratina prezentă în structuri dure sau filamentoase, cum ar fi părul , unghiile , penele , copitele și exoscheletul unor animale . Anumite proteine globulare pot juca, de asemenea, un rol structural, de exemplu actina și tubulina ai căror monomeri sunt globulari și solubili, dar se polimerizează pentru a forma filamente rigide lungi care constituie citoscheletul , ceea ce permite celulei să își mențină forma și dimensiunea.
Cele Proteinele motorii sunt proteine structurale specifice care sunt capabile să genereze forțe mecanice. Acestea sunt, de exemplu , miozina , kinesin si dynein . Aceste proteine sunt esențiale pentru motilitatea organismelor unicelulare , precum și pentru sperma organismelor pluricelulare . De asemenea, ele ajută la generarea forțelor de lucru în contracția musculară și joacă un rol esențial în transportul intracelular.
Cu toate acestea, manoproteinele par să aibă roluri cheie în interiorul celulelor, în special prin controlul porozității peretelui celular.
Rezumatul funcțiilor îndeplinite de proteine
Proteinele îndeplinesc astfel o mare varietate de funcții în interiorul celulei și al corpului:
- a proteinelor structurale care permit celulei să mențină organizarea sa în spațiu, și care sunt constituenții citoscheletului ;
- a proteinelor de transport , care asigură transferul de molecule diferite , în și din celule;
- a proteinelor de reglementare , care modulează activitatea altor proteine sau care controlează expresia genelor ;
- a proteinelor de semnalizare care surprind semnalele externe și asigură transmiterea acestora în celulă sau organism; există mai multe tipuri, de exemplu proteinele hormonale , care ajută la coordonarea activităților unui organism acționând ca semnale între celule;
- a proteinelor de receptori , care a detecta molecule mesager și alte semnale pentru celula de a acționa în consecință:
- a proteinelor senzoriale detecta semnale de mediu: și răspund prin transmiterea semnalelor în celulă; ( de exemplu , lumina).
- a receptorilor hormonali detecta hormoni și semnale de trimitere la celula de a acționa în mod corespunzător ( de exemplu. Insulina este un hormon care, atunci când a primit, indică celula pentru a absorbi și utilizarea glucozei );
- a proteinelor cu motor , care permite celulelor sau a organismelor, sau anumite elemente (cilia) să se deplaseze sau se deformeze ( de ex. actină și miozină permite mușchiului să contractului );
- a proteinelor de apărare care protejează celula împotriva agenților infecțioși ( de ex. anticorpul );
- a proteinelor de depozitare care permit rezervarea de acid amino ordine biosintetizează alte proteine ( de exemplu. ovalbumina , principala proteina din albușul asigură stocarea pentru dezvoltarea embrionilor de pui );
- a enzimele care modifică rata de aproape toate reacțiile chimice din celulă , fără a fi transformată în reacție.
Metode de studiu
Structura și funcțiile proteinelor pot fi studiate in vivo , in vitro și in silico . Studiile in vivo permit explorarea rolului fiziologic al unei proteine în cadrul unei celule vii sau chiar în cadrul unui organism în ansamblu. Studiile in vitro ale proteinelor purificate în medii controlate sunt utile pentru a înțelege modul în care o proteină funcționează in vivo : de exemplu, studierea cineticii unei enzime permite analiza mecanismului chimic al activității sale catalitice și a afinității sale relative față de diferite substraturi . În studiile silico folosesc algoritmi computerizați pentru modelarea proteinelor.
Purificarea proteinelor
Pentru a putea fi analizată in vitro , o proteină trebuie să fi fost mai întâi purificată din ceilalți constituenți chimici ai celulei. Aceasta începe de obicei cu liza celulei, în timpul căreia membrana plasmatică este ruptă pentru a elibera conținutul său într-o soluție pentru a da un lizat. Acest amestec poate fi purificat prin ultracentrifugare , ceea ce face posibilă separarea constituenților săi în fracțiuni care conțin proteine solubile, lipide și proteine de membrană , organite celulare și acizi nucleici . Precipitarea proteinelor prin eliberare face posibilă pentru a le concentra din acest lizat. Apoi este posibil să se utilizeze mai multe tipuri de cromatografie pentru a izola proteinele pe care se dorește să le studieze în funcție de proprietățile lor fizico - chimice, cum ar fi masa lor molară , sarcina electrică sau chiar afinitatea lor de legare. Gradul de purificare poate fi urmărit folosind mai multe tipuri de electroforeză pe gel dacă se cunoaște masa moleculară și punctul izoelectric al proteinelor studiate, prin spectroscopie dacă proteina are caracteristici spectroscopice identificabile sau prin test enzimatic (în) dacă proteina are activitate enzimatică . Mai mult, proteinele pot fi izolate în funcție de sarcina lor electrică prin focalizare izoelectrică .
Proteinele naturale necesită în cele din urmă o serie de etape de purificare înainte de a putea fi studiate în laborator. Pentru a simplifica acest proces, ingineria genetică este adesea utilizată pentru a modifica proteinele prin dotarea acestora cu caracteristici care le fac mai ușor de purificat fără a le modifica structura sau activitatea. Se adaugă astfel „etichete” recunoscute pe proteină sub formă de secvențe de aminoacizi identificați, adesea un număr de reziduuri de histidină - etichetă polihistidină sau etichetă His - la capătul C- terminal sau la sfârșitul N -terminal al lanțul polipeptidic . Prin urmare, atunci când lizatul este plasat într-o coloană cromatografică care conține nichel , reziduurile de histidină se complexează cu nichelul și rămân legate de coloană în timp ce constituenții nemarcați trec prin ea fără a fi opriți. Au fost dezvoltate mai multe tipuri de etichete pentru a permite cercetătorilor să purifice anumite proteine din amestecuri complexe.
Localizare celulară
Studiul in vivo al proteinelor implică deseori cunoașterea exactă a locului în care sunt sintetizate și unde se găsesc în celule. Deși majoritatea proteinelor intracelulare sunt produse în citoplasmă și majoritatea proteinelor membranare sau secretate în mediul extracelular sunt produse în reticulul endoplasmatic , este rar să înțelegem exact cum proteinele vizează în mod specific anumite structuri celulare sau anumite structuri celulare . Inginerie genetică oferă instrumente utile pentru a obține o idee de localizarea anumitor proteine, de exemplu , prin legarea proteinei la o proteină studiat permițând locului, adică, prin efectuarea unei proteine de fuziune între proteina studiată și o proteină utilizată ca un marker, cum ar fi proteina fluorescentă verde . Localizarea intracelulară a proteinei de fuziune rezultate poate fi vizualizată cu ușurință și eficient prin microscopie .
Alte metode de localizare intracelulară a proteinelor implică utilizarea unor markeri cunoscuți pentru anumite compartimente celulare precum reticulul endoplasmatic , aparatul Golgi , lizozomii , mitocondriile , cloroplastele , membrana plasmatică etc. De exemplu, este posibilă localizarea proteinelor marcate cu o etichetă fluorescentă sau vizate cu anticorpi împotriva acestor markeri. Tehnicile de imunofluorescență fac astfel posibilă localizarea proteinelor specifice. Pigmenții fluorescenți sunt utilizați, de asemenea, pentru etichetarea compartimentelor celulare într-un scop similar.
Imunohistochimia utilizează în general , un anticorp care vizează una sau mai multe proteine diferite , care sunt conjugați cu enzime care emit semnale luminescent sau cromogen pot fi comparate cu diferite mostre, ceea ce permite a informațiilor deduce pe localizarea proteinelor studiate. De asemenea, este posibil să se utilizeze tehnici de co-fracționare într-un gradient de zaharoză (sau altă substanță) folosind centrifugarea izopicnică.
Microscopia imunoelectronică combină utilizarea microscopiei electronice convenționale cu utilizarea unui anticorp îndreptat împotriva proteinei studiate, acest anticorp fiind conjugat anterior cu un material cu densitate mare de electroni precum aurul . Acest lucru face posibilă localizarea detaliilor ultrastructurale, precum și a proteinelor studiate.
Proteomica
Setul de proteine ale unei celule sau al unui tip de celulă constituie proteomul său , iar disciplina științifică care o studiază este proteomica . Acești doi termeni au fost creați prin analogie cu genomul și genomica . Dacă proteomul este derivat din genom, totuși, nu este posibil să se prezică exact ce va fi proteomul unei celule din simpla cunoaștere a genomului său. Într-adevăr, expresia unei gene variază de la o celulă la alta în cadrul aceluiași organism ca funcție de diferențiere celulară , sau chiar în aceeași celulă ca funcție a ciclului celular . Mai mult, aceeași genă poate da mai multe proteine (de exemplu poliproteine virale ), iar modificările post-translaționale sunt deseori necesare pentru a face o proteină activă.
Dintre tehnicile experimentale utilizate în proteomica, observăm electroforeza bidimensională , ceea ce permite separarea unui număr mare de proteine, spectrometrie de masă , ceea ce permite throughput ridicată identificarea rapidă și de proteine precum secvențiere a peptidelor. (Cel mai adesea după digestie pe gel (en) ), chipsuri proteice (en) , care permit detectarea concentrațiilor relative ale unui număr mare de proteine prezente într-o celulă și abordarea dublă hibridă care permite, de asemenea, explorarea interacțiunilor proteină-proteină . Setul de interacțiuni proteină-proteină dintr-o celulă se numește interacteom . Abordarea pentru determinarea structurii proteinelor printre toate conformările posibile ale acestora este genomica structurală .
Bioinformatica
Există acum o varietate de metode computerizate disponibile pentru a analiza structura, funcția și evoluția proteinelor. Dezvoltarea unor astfel de instrumente a fost necesară prin cantitatea mare de date genomice și proteomice disponibile pentru un număr foarte mare de ființe vii, începând cu genomul uman . Este imposibil să se studieze toate proteinele în mod experimental, astfel încât doar un număr mic dintre acestea sunt studiate în laborator, în timp ce instrumentele de calcul fac posibilă extrapolarea rezultatelor astfel obținute cu alte proteine, care sunt similare cu acestea. Astfel de proteine omoloage sunt identificate eficient prin tehnici de aliniere a secvenței . Instrumentele de profilare a secvenței peptidice fac posibilă localizarea siturilor scindate de enzime de restricție , citirea cadrelor în secvențe de nucleotide și prezicerea structurilor secundare . De asemenea, este posibil să se construiască arbori filogenetici și să se dezvolte ipoteze cu privire la evoluție folosind software cum ar fi ClustalW (in) pentru a urmări strămoșii organismelor moderne și genele acestora. Instrumentele de bioinformatică au devenit esențiale pentru studiul genelor și proteinelor exprimate de aceste gene.
Predicția și simularea structurii
În plus față de genomica structurală, predicția structurii proteinelor își propune să dezvolte mijloace pentru a construi în mod eficient modele plauzibile care descriu structura proteinelor care nu au putut fi rezolvate experimental. Cel mai eficient mod de a prezice structura, numit modelare homologică , se bazează pe existența unor structuri model cunoscute a căror secvență este similară cu cea a proteinei în studiu. Scopul genomicii structurale este de a furniza suficiente date despre structurile rezolvate pentru a permite elucidarea celor care rămân de rezolvat. Deși rămâne dificil de modelat structurile exact atunci când există doar modele structurale îndepărtate la care se poate face referire, se crede că esența problemei constă în alinierea secvențelor, deoarece se pot găsi modele foarte exacte. este cunoscut. Multe predicții ale structurilor au fost utile domeniului emergent al ingineriei proteinelor (în) , care a inclus dezvoltarea de noi moduri de pliere . O problemă mai complexă de rezolvat prin calcul este predicția interacțiunilor intermoleculare, cum ar fi predicția ancorării moleculelor și a interacțiunilor proteină-proteină .
Plierea și legarea proteinelor pot fi simulate folosind tehnici precum mecanica moleculară , dinamica moleculară și metoda Monte Carlo , care beneficiază de tot mai multe arhitecturi de calcul paralele și distribuite , ca proiectul Folding @ home sau modelarea moleculară pe un procesor grafic . Plierea unor mici domenii de proteine α-elicoidale , cum ar fi capacul vilinei și proteina accesorie a HIV, au fost simulate cu succes în silico , iar metodele hibride care combină dinamica moleculară standard cu elemente ale mecanicii cuantice au permis explorarea stărilor electronice ale rodopsine .
Proprietăți
Fenotip
Prin urmare, planul de producere a proteinelor depinde în primul rând de genă . Cu toate acestea, secvențele genelor nu sunt strict identice de la un individ la altul. În plus, în cazul ființelor vii diploide , există două copii ale fiecărei gene. Și aceste două exemplare nu sunt neapărat identice. Prin urmare, o genă există în mai multe versiuni de la un individ la altul și uneori la același individ. Aceste versiuni diferite se numesc alele . Setul de alele ale unui individ formează genotipul .
Deoarece genele există în mai multe versiuni, proteinele vor exista și în diferite versiuni. Aceste versiuni diferite de proteine va duce la diferențe de la un individ la altul, astfel de individ va avea ochii albastri , dar ca nu au ochi negri, etc . Aceste caracteristici, vizibile sau nu, specifice fiecărui individ sunt numite fenotip . La același individ, un grup de proteine cu o secvență similară și funcție identică se spune că este izoformă . Izoformele pot fi rezultatul îmbinării alternative a aceleiași gene, a expresiei mai multor alele ale unei gene sau a prezenței mai multor gene omoloage în genom.
Evoluţie
În timpul evoluției , acumulările de mutații au făcut ca genele să divergă în interiorul și între specii . De aici provine diversitatea proteinelor asociate acestora. Cu toate acestea, este posibil să se definească familiile de proteine, ele însele corespunzând familiilor de gene. Astfel, la o specie gene foarte asemănătoare și, prin urmare, proteine, pot coexista formând o familie. Două specii strâns legate sunt susceptibile de a avea reprezentanți ai aceleiași familii de proteine.
Vorbim de omologie între proteine atunci când diferite proteine au o origine comună, o genă ancestrală comună.
Compararea secvențelor de proteine face posibilă demonstrarea gradului de „relaționare” între diferite proteine, se vorbește aici de similitudinea secvenței. Funcția proteinelor poate diferi pe măsură ce similitudinea scade, dând astfel naștere unor familii de proteine care au o origine comună, dar care au funcții diferite.
Analiza secvențelor și structurilor proteice a arătat că mulți se organizează în domenii , adică părți care dobândesc structură și îndeplinesc o funcție specifică. Existența proteinelor cu mai multe domenii poate fi rezultatul recombinării într-o singură genă a mai multor gene inițial individuale, iar invers proteinele compuse dintr-un singur domeniu pot fi rezultatul separării în mai multe gene a unei gene inițial. -proteina domeniului.
Hrana umană
În timpul digestiei , din stomac, proteinele de origine vegetală, bacteriană, fungică sau animală sunt descompuse ( hidrolizate ) de proteaze ; descompuse în polipeptide și apoi în aminoacizi utili organismului , inclusiv aminoacizi esențiali (pe care organismul nu îi poate sintetiza). Pepsinogen este convertit la pepsină în contact cu acid clorhidric stomac. Pepsina este singura enzimă proteolitică care digeră colagenul , principala proteină din țesutul conjunctiv .
Digestia proteinelor are loc în principal în duoden . Acestea sunt absorbite în principal când ajung în jejun și doar 1% din proteinele ingerate se găsesc în fecale . Anumiți aminoacizi rămân în celulele epiteliale ale intestinului, utilizate pentru biosinteza proteinelor noi, inclusiv a proteinelor intestinale care sunt în mod constant digerate, reciclate și absorbite de intestinul subțire .
Digestibilitatea proteinelor variază considerabil în funcție de natura lor și de prepararea alimentelor.
Cantități recomandate
De ANSES recomandă un recomandat aport alimentar (CDI) de 0,83 g · kg -1 · d -1 , pentru maximum 2,2 g · kg -1 · d -1 la adulți sănătoși, 62 g pe zi pentru un om 75 kg . Trebuie remarcat faptul că ANC sunt mai mari decât nevoile medii, care sunt de 0,66 g · kg -1 · d -1 conform aceluiași raport, care ar da 49,5 g pe zi pentru cazul anterior.
Necesarul mediu de proteine a fost definit de FAO, care recomandă 49 g de proteine pentru bărbații adulți și 41 g pentru femei (47 dacă sunt însărcinate, 58,5 dacă alăptează).
Proteine animale, fungice, vegetale
Potrivit Asociației Americane a Inimii , nu este necesar să consumați proteine animale pentru a avea suficiente proteine în dieta dvs.: proteinele vegetale pot furniza suficienți aminoacizi esențiali și neesențiali, atâta timp cât sursele de proteine dietetice sunt variate și că aportul este suficient pentru a satisface nevoile de energie. Nu este necesar să le combinați în aceeași masă. Asociatia Dietetica Americana , de asemenea , reamintește că proteina de plante poate îndeplini cerințele de proteine în cazul în care dieta plantelor este variată și satisface necesarul de energie. În plus, „un sortiment de alimente vegetale consumate pe parcursul unei zile poate furniza toți aminoacizii esențiali și poate asigura o retenție și o utilizare suficientă a azotului la adulții sănătoși, astfel încât combinația de proteine din timpul aceleiași mese să nu fie necesară. "
- Proteine animale : sunt întotdeauna însoțite de lipide saturate , al căror consum este adesea excesiv și, uneori, de aditivi alimentari (cum ar fi nitriții din mezeluri , suspectați de a fi cancerigeni). Proteinele animale sau produsele asociate precum aminele heterociclice sunt, de asemenea, considerate a fi un factor de risc pentru anumite tipuri de cancer ( colon , vezică ). Începând cu 2015 , OMS și IARC au clasificat carnea roșie (carne de porc, carne de vită, oaie, cal și capră) ca fiind probabil carcinogenă și carnea procesată ca fiind cancerigenă dovedită (34.000 de decese / an la nivel mondial, potrivit unui studiu realizat de Global Burden of Disease Proiect ; conform OMS: consumul a 50 de grame de carne procesată pe zi crește riscul de cancer colorectal cu 18% (se spune că o carne este procesată dacă a suferit sărarea, maturarea, fermentarea, fumatul sau alte procese menite să-i îmbunătățească Din cauza lipsei de date, Grupul de lucru IARC nu a reușit să clasifice carnea crudă în ceea ce privește riscul de cancer, dar reamintește că prezintă un risc infecțios . să aibă poluanți bioconcentrați prin intermediul lanțului alimentar
- Proteine vegetale : efectele pozitive sunt asociate cu plantele bogate în proteine. Cele Impulsurile sunt bogate in proteine, dar , de asemenea , în fibre , minerale și să aducă un sentiment de sațietate pentru un indice glicemic scăzut. Consumul de fasole contribuie la scăderea nivelului de colesterol și la riscul accidentelor cardiovasculare și a anumitor tipuri de cancer ( colorectal , prostată și pancreas ). Ele sunt în mod evident o alternativă pentru vegani sau vegetarieni. Nucile, legumele, fasolea, quinoa și cerealele conțin cantități mari de proteine, dar și energie.
- Proteine fungice : ciupercile comestibile sunt deseori bogate în proteine și, la fel ca plantele, sunt surse de fibre dietetice și minerale. Pe de altă parte, recoltate în natură sau cultivate pe substraturi poluate, acestea tind să acumuleze o mare cantitate de metale grele , metaloizi și chiar radionuclizi .
Calitatea proteinelor
Toți aminoacizii necesari trebuie să fie furnizați de alimente, cu durerea de deficiență, ceea ce implică surse diversificate de proteine.
Recomandarea de a combina proteinele animale și vegetale în fiecare masă a fost invalidată din 1994 în urma unui articol al lui Vernon Young și Peter Pellett care a devenit o referință privind metabolismul proteinelor la om, confirmând că combinația de proteine din masă este total inutilă. Persoanele care nu doresc să mănânce proteine animale nu sunt expuse riscului unui dezechilibru de aminoacizi al proteinelor vegetale în dieta lor. Multe proteine vegetale conțin puțin mai puțin de unul sau mai mulți aminoacizi esențiali ( lizina în special și într-o măsură mai mică metionină și treonină ), fără consumul exclusiv de surse de proteine vegetale care împiedică o dietă echilibrată în aminoacizi.
Concluziile articolului de la Young și Pellet trebuie luate în considerare doar în cazul foarte general în care cerealele nu sunt sursa exclusivă de hrană, pe care au grijă să le precizeze, în plus, unde explică în alte articole. Astfel, în unele regiuni defavorizate, rațiile alimentare pot include numai cereale, ceea ce provoacă probleme grave de sănătate copiilor mici, de exemplu în gospodăriile sărace din statul Madhya Pradesh din India (grâu și orez).
În plus, companiile de semințe caută să obțină sau au obținut deja soiuri de cereale cu un conținut modificat de aminoacizi ( OMG ), de exemplu porumb îmbogățit în lizină.
Autoritățile franceze de sănătate (AFSSA / ANSES ) încă refuză să soluționeze această chestiune.
Suplimente alimentare
Suplimente alimentare de proteine există pentru sportivii care doresc să dezvolte volumul lor musculare, cât și pentru persoanele din deficiențe de proteine. Proteinele utilizate sunt adesea proteine obținute din lucernă ( lucernă sub formă de extract de frunze (EFL) ) , fasole , mazăre sau zer (sub denumirea de "zer") și aminoacizi ramificați desemnați sub denumirea de "BCAA" .
Alimente bogate în proteine
- De ciuperci au un conținut de proteine dificil de a măsura cu precizie (conținutul supraestimate anterior cu 70 până la 200% la ori) , dar de multe ori relativ ridicată (15 până la 35% din greutatea uscată a ciupercii), mult mai mare decât cerealele , cum ar fi grâu și porumb, de interes alimentar. Aceste niveluri sunt comparabile cu cele ale leguminoaselor precum mazărea și linte.
Cei aminoacizi esențiali adesea reprezintă o parte semnificativă a acestor proteine ( de ex. 61,8 și 63,3% din totalul de amino nivelurile de acid , respectiv în Tricholoma portentosum și Tricholoma terreum (în care leucina , izoleucină și triptofan sunt aminoacizi limitați) corectată amino scorurile acide (PDCAAS) ale proteinelor din aceste două ciuperci sunt mici în comparație cu cele ale cazeinei, albușul de ou și soia, dar mai mare decât cele ale multor proteine vegetale. conţinutul de grăsimi a fost redus (5,7% pentru Tricholoma porterosum și 6,6 % pentru Tricholoma terreum ) la ambele specii, cu acizi oleici și linoleici reprezentând peste 75% din totalul acizilor grași.
Unii, cum ar fi ciuperca de la Paris (3,09 g de proteine la 100 g ) au fost mult timp cultivate și uscate, dar individual ( ca și alte alimente) pot avea deficit de anumiți aminoacizi (de exemplu aminoacizi care conțin sulf, metionină și cistina în cazul ciupercilor de stridii, de exemplu), dar sunt bogate în lizină și leucină, care lipsesc, de exemplu, în cereale. Încă sunt descoperite virtuți (de exemplu: una dintre aceste proteine pare la șoareci să inhibe alergiile alimentare ) și defecte (de exemplu: s-a dovedit că o altă proteină fungică este cardiotoxică ).
- Alimentele de origine animală sunt, în general, mai proteice decât cele de origine vegetală, în special ouăle (bogate în albumină) sau brânza (cazeină etc.), cum ar fi parmezanul, de exemplu, care conține 39,4 g / 100 g, mai mult decât carnea și pești. În plus față de anumite carne (de exemplu: piept de pui gătit cu un conținut mediu de 29,2 g / 100 g), cum ar fi carnea de vită care conține 26 g / 100 g, peștele, cum ar fi tonul alb sau sardinele , conțin, de asemenea, aproximativ 30 g / 100 g. Ouăle sunt, de asemenea, o sursă de proteine (24 g / 100 g pentru patru ouă).
- Anumite plante sau semințe sunt foarte bogate în proteine: ulei de seminte ( migdale , fistic , de in , etc. ) și leguminoase ( năut , fasole , linte , etc. ). Astfel, 100 g de produs brut conțin o cotă de proteine de: 58 g pentru spirulină , 38 g pentru boabe de soia , 30 g pentru semințe de dovleac , 25 g pentru fasole neagră , 24 g pentru linte , 21 g pentru seitan (gluten) și nuci , 20 g pentru migdale și gris , 15 g pentru fulgi de ovăz , 15 g pentru orez sălbatic, 14 g pentru quinoa .
- La drojdii , bacterii si cianobacterii sunt rareori crescute pentru a fi consumate în mod direct, dar drojdie sau Spirulina (58 g proteină per 100 g spirulină) sunt foarte bogate în proteine.
Note și referințe
- Descoperiri de proteine
- Gregory A. Petsko și Dagmar Ringe ( trad. Din engleză), Structura și funcția proteinelor , Bruxelles, Universitatea De BoekNoiembrie 2008, 190 p. ( ISBN 978-2-8041-5888-0 , citit online )
- (în) Alex Gutteridge și Janet M. Thornton , „ Understanding nature’s catalytic toolkit ” , Trends in Biochemical Sciences , vol. 30, n o 11,noiembrie 2005, p. 622-629 ( PMID 16214343 , DOI 10.1016 / j.tibs.2005.09.006 , citiți online )
- (în) Harvey Lodish, Arnold Berk, Paul Matsudaira, Chris A. Kaiser, Monty Krieger, Matthew P. Scott, Lawrence Zipursky și James Darnell, Molecular Cell Biology , New York, WH Freeman & Company 5 - lea ediție,august 2003, 973 p. ( ISBN 978-0-7167-4366-8 )
- Garcia Martin S (2015) Nanoproteine dinamice: auto-asamblare a peptidelor pe nanoparticule de aur protejate monostrat
- Mitch Leslie (2019) Impact supradimensionat ; | Știință 18 Oct 2019: Vol. 366, Ediția 6463, pp. 296-299 | DOI: 10.1126 / science.366.6463.296 ( rezumat )
- Staudt, AC și Wenkel, S. (2011). Reglarea funcției proteinelor de către „microProteine” . Rapoarte EMBO, 12 (1), 35-42.
- (Wang și colab. (2009)
- zhang și colab., 2009)
- (în) Zhaohui Xu, Arthur L. Horwich și Paul B. Sigler , " Structura cristalină a asimetricului GroEL-GroES- (ADP) 7complex chaperonin ” , Natura , vol. 388, nr . 6644,21 august 1997, p. 741-750 ( PMID 9285585 , DOI 10.1038 / 41944 , citiți online )
- (în) Lisa J Harris, Eileen Skaletsky și Alexander McPherson , " Structura cristalografică a unui anticorp monoclonal IgG1 intact " , Journal of Molecular Biology , vol. 275, nr . 5,6 februarie 1998, p. 861-872 ( PMID 9480774 , DOI 10.1006 / jmbi.1997.1508 , citiți online )
- (în) W. Bolton și MF Perutz , " Sinteza Fourier tridimensională a dezoxiemoglobinei calului la rezoluția 2,8 Å " , Nature , vol. 228, nr . 5271,7 noiembrie 1970, p. 551-552 ( PMID 5472471 , DOI 10.1038 / 228551a0 , Bibcode 1970Natur.228..551B , citiți online )
- (în) Edward N. Baker, Thomas L. Blundell, John F. Cutfield, Susan M. Cutfield, Eleanor J. Dodson, Guy G. Dodson, Dorothy Crowfoot Hodgkin Domnul Roderick E. Hubbard, Neil W. Isaacs, Colin D. Reynolds, Kiwako Sakabe, Norioshi Sakabe și Numminate M. Vijayan , „ Structura cristalelor de insulină de porc 2Zn la o rezoluție de 1,5 Å ” , Philosophical Transactions B , vol. 319, nr . 11956 iulie 1988, p. 369-456 ( PMID 2905485 , DOI 10.1098 / rstb.1988.0058 , Bibcode 1988RSPTB.319..369B , citiți online )
- (ro) Michael B. Berry și George N. Phillips Jr. , „ Structuri cristaline ale adenilat kinazei Bacillus stearothermophilus cu Ap 5 A legat , Mg 2+ Ap 5 A și Mn 2+ Ap 5 Adezvăluie o poziție intermediară a capacului și o geometrie octaedrică de șase coordonate pentru Mg 2+ legat și Mn 2+ ” , Proteine: Structure, Function, and Bioinformatics , vol. 32, n o 3,15 august 1998, p. 276-288 ( PMID 9715904 , citiți online )
- (în) Harindarpal S. Gill și David Eisenberg , „ Structura cristalină a fosfinotricinei în situl activ al glutaminei sintetaza luminează mecanismul de inhibare enzimatică ” , Biochimie , vol. 40, nr . 7,20 februarie 2001, p. 1903-1912 ( PMID 11329256 , DOI 10.1021 / bi002438h , citiți online )
- (în) Wojciech R. Rypniewski Hazel Holden și Ivan Rayment , „ Consecințele structurale ale metilării reductive a reziduurilor de lizină în lizozima de albuș de ou de găină: o analiză cu raze X la rezoluția de 1,8 Å ” , Biochimie , vol. 32, n ° 37,21 septembrie 1993, p. 9851-9858 ( PMID 8373783 , DOI 10.1021 / bi00088a041 , citiți online )
- (în) Tamir Gonen Yifan Cheng, Piotr Sliz, Yoko Hiroaki Yoshinori Fujiyoshi, Stephen C. Harrison și Thomas Walz , " Interacțiuni lipid-proteine în cristale bidimensionale cu două straturi AQP0 " , Nature , vol. 438, nr . 7068,1 st decembrie 2005, p. 633-638 ( PMID 16319884 , PMCID 1350984 , DOI 10.1038 / nature04321 , citiți online )
- (în) Daron M. Standley, Akira R. Kinjo, Kengo Kinoshita și Haruki Nakamura , " Protein structure bases de date cu noi servicii web pentru biologie structurală și cercetare biomedicală " , Briefings in Bioinformatics , vol. 9, n o 4,iulie 2008, p. 276-285 ( PMID 18430752 , DOI 10.1093 / bib / bbn015 , citiți online )
- (în) Peter Walian, Timothy A Cross K și Bing Jap , „ Structural genomics of membrane protein ” , Genome Biology , vol. 5, n o 4,2004, p. 215 ( PMID 15059248 , PMCID 395774 , DOI 10.1186 / gb-2004-5-4-215 , citiți online )
- (în) Roy D. Sleator , " Prediction of Protein Functions " , Methods in Molecular Biology , vol. 815,2012, p. 15-24 ( PMID 22130980 , DOI 10.1007 / 978-1-61779-424-7_2 , citiți online )
- Forchhammer K, Bock A, „ Selenocisteina sintază din Escherichia coli. Analiza secvenței de reacție ”, J. Biol. Chem. , vol. 266, nr . 10,1991, p. 6324–8 ( PMID 2007585 )
- (în) Yuhei Araiso, Sotiria Palioura, Ryuichiro Ishitani, R. Lynn Sherrer, Patrick O'Donoghue, Jing Yuan, Hiroyuki Oshikane, Naoshi Domae Julian DeFranco, Dieter Söll și Osamu Nureki , " Structural insights to RNA-dependent and eucaryal archaeal formarea selenocisteinei ” , Cercetarea acizilor nucleici , vol. 36, nr . 4,Martie 2008, p. 1187-1199 ( PMID 18158303 , PMCID 2275076 , DOI 10.1093 / nar / gkm1122 , citiți online )
- (în) Sotiria Palioura R. Lynn Sherrer, Thomas A. Steitz Dieter Söll și Miljan Simonovic , „ Complexul uman SepSecS-tRNA Sec dezvăluie mecanismul educației selenocisteinei ” , Știință , vol. 325, nr . 5938,17 iulie 2009, p. 321-325 ( PMID 19608919 , PMCID 2857584 , DOI 10.1126 / science.1173755 , Bibcode 2009Sci ... 325..321P , citiți online )
- (în) Alice B. Fulton și William B. Isaacs , „ Titin, o proteină sarcomerică uriașă, elastică, cu un rol probabil în morfogeneză ” , BioEssays , vol. 13, nr . 4,Aprilie 1991, p. 157-161 ( PMID 1859393 , DOI 10.1002 / bies.950130403 , citiți on - line )
- (în) " Titin (CE 2.7.11.1) (electri) Mus musculus (mouse - ul) " pe ProtParam pe ExPASy (accesat 09 mai 2015 )
- (în) Thomas Bruckdorfer Oleg Marder și Fernando Albericio , " De la producția de peptide în cantități de miligrame pentru cercetare la cantități multi-tonice pentru medicamentele viitorului " , Current Pharmaceutical Biotechnology , vol. 5, n o 1,Februarie 2004, p. 29-43 ( PMID 14965208 , DOI 10.2174 / 1389201043489620 , citiți online )
- (în) Dirk Schwarzer și Philip A Cole , " Protein semisynthesis and Expressed Protein Ligation: Chasing a protein's tail " , Current Opinion in Chemical Biology , vol. 9, n o 6,decembrie 2005, p. 561-569 ( PMID 16226484 , DOI 10.1016 / j.cbpa.2005.09.018 , citiți on - line )
- (în) Stephen BH Kent , „ sinteza chimică totală a proteinelor ” , Chemical Society Reviews , vol. 38, n o 2Februarie 2009, p. 338-351 ( PMID 19169452 , DOI 10.1039 / B700141J , citiți online )
- (în) R. Sankaranarayanan și D. Moras , „ Fidelitatea traducerii codului genetic ” , Acta Biochimica Polonica , Vol. 48, n o 22001, p. 323-335 ( PMID 11732604 , citiți online )
- (în) John A. Copland, Melinda Sheffield-Moore, Nina Koldzic-Zivanovic, Sean Gentry, George Lamprou, Fotini Tzortzatou-Stathopoulou Vassilis Zoumpourlis, Randall J. Urban și Spiros A. Vlahopoulos , „ Receptorii steroizilor sexuali în diferențierea scheletului și neoplazie epitelială: este posibilă intervenția specifică țesutului? ” , BioEssays , vol. 31, nr . 6,Iunie 2009, p. 629-641 ( PMID 19382224 , DOI 10.1002 / bies.200800138 , citiți online )
- (în) Stanislav Samarin și Asma Nusrat , „ Regulamentul complexului joncțional apical epitelial de către familia Rho GTPases ” , Frontiers in Bioscience , Vol. 14,ianuarie 2009, p. 1129-1142 ( PMID 19273120 , DOI 10.2741 / 3298 , citiți online )
- (în) Ida Schomburg Antje Chang, Sandra Placzek Carola Söhngen, Michael Rother, Maren Lang, Cornelia Munaretto Susanne Ulas, Michael Stelzer, Andreas Grote, Maurice Scheer și Dietmar Schomburg , " BRENDA în 2013: reacții integrate, date cinetice, funcția enzimei date, îmbunătățirea clasificării bolii: noi opțiuni și conținuturi în BRENDA ” , Cercetarea acizilor nucleici , vol. 41, n o D1,ianuarie 2013, D764-D772 ( PMID 23203881 , DOI 10.1093 / nar / gks1049 , citiți online )
- (în) A. și R. Radzicka Wolfenden , „ A proficient enzyme ” , Science , vol. 267, nr . 5194,6 ianuarie 1995, p. 90-93 ( PMID 7809611 , DOI 10.1126 / science.7809611 , citiți online )
- (în) Brian P. Callahan și Brian G. Miller , " OMP decarboxilaza-o enigmă persistă " , Bioorganic Chemistry , vol. 35, nr . 6, decembrie 2007, p. 465-469 ( PMID 17889251 , DOI 10.1016 / j.bioorg.2007.07.004 , citiți online )
- (în) Harold Rudiger, Hans-Christian Siebert, Dolores Solis, Jesus initial Jimenez-Barbero, Antonio Romero, Claus-Wilhelm von der Lieth, Teresa Diaz-Maurino și Hans-Joachim Gabius , „ Medicinal Chemistry Based on the Sugar Code: Fundamentele lectinologiei și strategiilor experimentale cu lectine ca ținte ” , Chimia curentă a medicamentelor , vol. 7, n o 4,aprilie 2000, p. 389-416 ( PMID 10702616 , DOI 10.2174 / 0929867003375164 , citiți online )
- De la Nobel, JG, Klis, FM, Priem, J., Munnik, T., & Van Den Ende, H. (1990) T el glucanaza-solubil manoproteine limita peretelui celular porozitate în Saccharomyces cerevisiae . Drojdie, 6 (6), 491-499.
- Zlotnik, HINDA, Fernandez, MP, Bowers, BLAIR și Cabib, ENRICO (1984). Manoproteinele Saccharomyces cerevisiae formează un strat de perete celular extern care determină porozitatea peretelui . Jurnalul de bacteriologie, 159 (3), 1018-1026.
- Caridi A (2006) Funcțiile enologice ale manoproteinelor de drojdie parietală. Antonie Van Leeuwenhoek, 89 (3-4), 417-422 ( rezumat )
- Harvey Lodish , Arnold Berk , Paul Matsudaira , Chris A. Kaiser , Monty Krieger , Matthew P. Scott , S. Laurence Zipursky și James Darnell ( trad. Pierre L. Masson și Chrystelle Sanlaville), Biologia moleculară a celulei ["Molecular Biologie celulară ”], Bruxelles, Universitatea De Boeck,2005, 3 e ed. , 1096 p. [ detaliu ediție ] ( ISBN 2-8041-4802-5 )
- (în) Julie Hey, Anton Posch, Andrew Cohen, Liu Ning și Adrianna Harbers , „ Fracționarea amestecurilor complexe de proteine prin focalizare iso -electrică în fază lichidă ” , Methods in Molecular Biology , vol. 424,2008, p. 225-239 ( PMID 18369866 , DOI 10.1007 / 978-1-60327-064-9_19 , citiți online )
- (în) K. Terpe , " Prezentare generală a fuziunilor de proteine de etichetă: de la fundamentele moleculare și biochimice la sistemele de tranzacționare " , Microbiologie aplicată și biotehnologie , Vol. 60, nr . 5,ianuarie 2003, p. 523-533 ( PMID 12536251 , DOI 10.1007 / s00253-002-1158-6 , citiți online )
- (în) Olesya V. Stepanenko, Vladislav V. Verkhusha Irina Kuznetsova Domnul Vladimir N. Uversky și KK Turoverov , " Proteine fluorescente ca biomarkeri și biosenzori: aruncarea luminilor colorate pe procesele moleculare și celulare " , Current Protein & Peptide Science , vol. . 9, n o 4,August 2008, p. 338-369 ( PMID 18691124 , PMCID 2904242 , DOI 10.2174 / 138920308785132668 , citiți online )
- (în) Rafael Yuste , „ Microscopia fluorescenței astăzi ” , Nature Methods , vol. 2, n o 12,decembrie 2005, p. 902-904 ( PMID 16299474 , DOI 10.1038 / nmeth1205-902 , citiți online )
- (în) William Margolin , " Proteina fluorescentă verde ca raportor pentru localizarea macromoleculară în celulele bacteriene " , Metode , vol. 20, n o 1,ianuarie 2000, p. 62-72 ( PMID 10610805 , DOI 10.1006 / meth.1999.0906 , citiți online )
- (în) Terry M. Mayhew și John M. Lucocq , „ Dezvoltări în biologia celulară pentru microscopia imunoelectronică cantitativă bazată pe secțiuni subțiri: o revizuire ” , Histochimie și biologie celulară , Vol. 130, n o 2August 2008, p. 299-313 ( PMID 18553098 , PMCID 2491712 , DOI 10.1007 / s00418-008-0451-6 , citiți online )
- (în) Angelika Görg, Walter Weiss și Michael J Dunn , „ Tehnologia actuală de electroforeză bidimensională pentru proteomică ” , Proteomics , vol. 4, n o 12,decembrie 2004, p. 3665-3685 ( PMID 15543535 , DOI 10.1002 / pmic.200401031 , citiți online )
- (în) P. și S. Conrotto Souchelnytskyi , " Abordări proteomice în știința biologică și medicală: principii și aplicații " , Oncologie experimentală , vol. 30, n o 3,septembrie 2008, p. 171-180 ( PMID 18806738 )
- (în) T. J. Joos și Bachmann , " Protein microarrays: potentials and limitations " , Frontiers in Bioscience , Vol. 14,ianuarie 2009, p. 4376-4385 ( PMID 19273356 , DOI 10.2741 / 3534 )
- (în) Manfred Koegl și Peter Uetz , „ Improving yeast two-hybrid screening systems ” , Briefings in Functional Genomics , vol. 6, n o 4,decembrie 2007( PMID 18218650 , DOI 10.1093 / bfgp / elm035 , bfg.oxfordjournals.org/content/6/4/302.full.pdf+html)
- (în) Dariusz și Krzysztof Ginalski Plewczyński , „ Interactomul: prezicerea interacțiunilor proteină-proteină în celule ” , Letters de biologie celulară și moleculară , vol. 14, n o 1,Martie 2009, p. 1-22 ( PMID 18839074 , DOI 10.2478 / s11658-008-0024-7 , citiți online )
- (în) Chao Zhang și Sung-Hou Kim , " Privire de ansamblu asupra genomicii structurale: de la structură la funcție " , Opinia curentă în chimia biologică , vol. 7, n o 1, Februarie 2003, p. 28-32 ( PMID 12547423 , DOI 10.1016 / S1367-5931 (02) 00015-7 , citiți online )
- (în) Yang Zhang , „ Progresul și provocările în predicția structurii proteinelor ” , Opinia curentă în biologia structurală , vol. 18, n o 3, iunie 2008, p. 342-348 ( PMID 18436442 , PMCID 2680823 , DOI 10.1016 / j.sbi.2008.02.004 , citiți online )
- (în) Zhexin Xiang , „ Progresele în omologia modelării structurii proteinelor ” , Current Protein & Peptide Science , vol. 7, n o 3, iunie 2006, p. 217-227 ( PMID 16787261 , PMCID 1839925 , DOI 10.2174 / 138920306777452312 # sthash.hup2vFsH.dpuf , citiți online )
- (în) Yang Zhang și Jeffrey Skolnick , „ Problema de predicție a structurii proteinelor ar putea fi rezolvată folosind biblioteca PDB actuală ” , Proceedings of the National Academy of Sciences din Statele Unite ale Americii , vol. 102, nr . 4, 25 ianuarie 2005, p. 1029-1034 ( PMID 15653774 , PMCID 545829 , DOI 10.1073 / pnas.0407152101 , citiți online )
- (în) Brian Kuhlman, Gautam Dantas, Gregory C. Ireton, Gabriele Varani, Barry L. Stoddard și David Baker , „ Design of a Novel Globular Protein Fold with Atomic-Level Accuracy ” , Știință , vol. 302, nr . 5649, 21 noiembrie 2003, p. 1364-1368 ( PMID 14631033 , DOI 10.1126 / science.1089427 , citiți online )
- (în) David W. Ritchie , „ Progresul recent și direcțiile viitoare în andocarea proteinei-proteine ” , Current Protein & Peptide Science , vol. 9, n o 1, Februarie 2008, p. 1-15 ( PMID 18336319 , DOI 10.2174 / 138920308783565741 , citiți online )
- (în) T. Herges și W. Wenzel , „ In Silico Folding of a Three Helix Protein and Characterization of the Free-Energy Landscape in a All-Atom Force Field ” , Physical dreater Letters , vol. 94, nr . 1, 14 ianuarie 2005, p. 018101 ( PMID 15698135 , DOI 10.1103 / PhysRevLett.94.018101 , Bibcode 2005PhRvL..94a8101H , citiți online )
- (în) Michael Hoffmann, Marius Wanko Paul Strodel, Peter H. König, Thomas Frauenheim Klaus Schulten, Walter Thiel, Emad Tajkhorshid și Marcus Elstner , „ Color Tuning in rhodopsins: The Mechanism for the Spectral Shift entre Bacteriorhodopsin and Sensory Rhodopsin II ” , Journal of the American Chemical Society , vol. 128, nr . 33, 23 august 2006, p. 10808-10818 ( PMID 16910676 , DOI 10.1021 / ja062082i , citiți online )
- Proteine
- „ Family Nutrition Guide ” (accesat la 26 noiembrie 2014 )
- (en-US) American Heart Association , „ Vegetarian, Vegan Diet & Heart Health ” , Go Red For Women® ,26 martie 2014( citiți online , consultat la 29 iulie 2017 )
- (în) „ Poziția Asociației Dietetice Americane: Dietele Vegetariene ” , Jurnalul Asociației Dietetice Americane ,iulie 2009, p. 1267–1268 ( citește online )
- Studiu de sănătate adventist-1 - Constatări despre cancer: câteva aspecte esențiale
- Comunicat de presă al OMS Carcinogenitatea consumului de carne roșie și carne procesată octombrie 2015]
- Formularul Dry Bean pe site-ul web Health Passport
- Consumul de leguminoase non-soia scade nivelul colesterolului: o meta-analiză a studiilor controlate randomizate
- Consumul de leguminoase și riscul bolilor coronariene la bărbați și femei din SUA: Studiu de urmărire epidemiologică NHANES I
- V. R. Young și PL Pellett , „ Proteine vegetale în raport cu nutriția proteinelor umane și a aminoacizilor ”, The American Journal of Clinical Nutrition , vol. 59, n o 5 supliment,Mai 1994, p. 1203S - 1212S ( ISSN 0002-9165 , PMID 8172124 , citit online , accesat la 29 iulie 2017 )
- (în) VR Young și PL Pellett , „ Proteine din grâu în raport cu necesitățile de proteine și disponibilitatea aminoacizilor ” , Jurnalul American de Nutriție Clinică , Vol. 41, nr . 5,1 st mai 1985, p. 1077–1090 ( ISSN 0002-9165 și 1938-3207 , DOI 10.1093 / ajcn / 41.5.1077 , citit online , accesat la 4 februarie 2020 )
- Sophie Landrin, „ În India, religia se invită în farfuria școlarilor ” , pe Le Monde ,4 februarie 2020(accesat pe 4 februarie 2020 )
- „ Câmpurile de aplicare a transgenezei ” , despre pedagogia gnis (accesat la 5 februarie 2020 )
- „ STATELE UNITE - Un porumb îmbogățit în lizină ” , pe inf'OGM ,noiembrie 2005(accesat la 5 februarie 2020 )
- Raport AFSSA / ANSES, paginile 232 și 233
- Conținutul de proteine al ciupercilor este dificil de măsurat precis, deoarece chitina și alți compuși ai azotului interferează cu analiza azotului total (de exemplu , metoda Kjeldahl ) utilizată anterior. Sursa: Danell E. și Eaker D. (1992), Aminoacizi și conținutul total de proteine ale ciupercilor comestibile Cantharellus cibarius (cartofi prăjiți) , Journal of the Science of Food and Agriculture , 60 (3), 333-337.
- Dıez VA și Alvarez A. (2001), Studii compoziționale și nutriționale pe două ciuperci sălbatice comestibile din nord-vestul Spaniei , Food Chemistry , 75 (4), 417-422 ( rezumat )
- Chang ST și Buswell JA (1996), Mushroom nutriceuticals , World Journal of Microbiology and biotechnology , 12 (5), 473-476 ( rezumat ).
- Peter CK Cheung (2009), Valoarea nutrițională și beneficiile pentru sănătate ale ciupercilor, Ciupercile ca alimente funcționale , (71-109).
- (ro) VA Dı́ez și A. Alvarez, Studii compoziționale și nutriționale pe două ciuperci comestibile sălbatice din nord-vestul Spaniei . În chimia alimentelor . Band 75, n o 4, decembrie 2001, S. 417-422, DOI : 10.1016 / S0308-8146 (01) 00229-1
- Chang ST și Miles PG (1991), Tendințe recente în producția mondială de ciuperci comestibile , The Mushroom Journal , 503, 15-18.
- Shah H., Khalil IA și Jabeen S. (1997), Compoziția nutrițională și calitatea proteinelor din ciuperca Pleurotus , Sarhad Journal of Agriculture (Pakistan) ( Rezumat Agris / FAO ).
- Hsieh, KY, Hsu, CI, Lin, JY, Tsai, CC și Lin, RH (2003), Administrarea orală a unei proteine comestibile derivate din ciuperci inhibă dezvoltarea reacțiilor alergice alimentare la șoareci , Alergie clinică și experimentală , 33 (11), 1595-1602 ( rezumat )
- Lin, JY, Lin, YJ, Chen, CC, Wu, HL, Shi, GY și Jeng, TW (1974), Proteină cardiotoxică din ciuperci comestibile , Nature , 252 (5480), 235 ( rezumat ).
- „ Tabel Ciqual al compoziției nutriționale a alimentelor ” , pe ciqual.anses.fr (accesat la 10 septembrie 2018 )
- Albert-François Creff și Daniel Layani, Manual de dietetică în practica medicală curentă , Paris, Masson,2004, 301 p. ( ISBN 978-2-294-01346-1 , citit online ) , p. 4
Vezi și tu
Bibliografie
- Gregory Petsko, Dagmar Ringe (trad. Chrystelle Sanlaville, Dominique Charmot-Bensimon), Structura și funcția proteinelor , De Boeck, Bruxelles, 2009. ( ISBN 978-2-8041-5888-0 ) .
- Lubert Stryer, Jeremy Mark Berg, John L. Tymoczko (trad. Serge Weinman), Biochimie , Flammarion, „Medicină-Științe”, Paris, 2008, ediția a 6- a . ( ISBN 978-2-257-00003-3 ) .
- Carl-Ivar Brändén, John Tooze (traducere. Bernard Lubochinsky, pref. Joël Janin), Introducere în structura proteinelor , Universitatea De Boeck, Bruxelles, 1996. ( ISBN 978-2-8041-2109-9 ) .
Articole similare
- Combinație de proteine (alimente - exemplu: orez / linte)
- Proteine recombinante
- Subfamilie de proteine
- Agregarea proteinelor
- Aquaporin
- Proteina Rieske
- Transportor de aminoacizi lizozomali
- Proteine fibroase
- Proteina globulară
- Viciline
- factori de transcriere
- Proteine CDX
- Proteine pentru schele
- Proteina Tau
- Tioproteina
- Selenoproteina
- Manoproteina
- Microproteine
linkuri externe
- ( fr ) Predictor Project Un software de calcul partajat care utilizează platforma BOINC pentru a studia plierea proteinelor.
- (ro) Server MRS Un server de bancă de date biologice, în care identificarea unei intrări în banca PDB face posibilă vizualizarea structurii pe ecran, în modul dinamic (a se vedea de exemplu ceea ce o căutare în bancă produce PDB de intrări corespunzătoare la tripsină).
- ( fr ) Proteins @ home Un proiect la scară largă pentru studierea plierii proteinelor, la care puteți participa cu computerul.