Acid ribonucleic
Acidul ribonucleic sau ARN (în limba engleză, ARN pentru acid ribonucleic ) este un acid nucleic prezent în aproape toate ființele vii , și , de asemenea , în unele virusuri . ARN-ul este foarte apropiat din punct de vedere chimic de ADN și este, de asemenea, sintetizat în celule dintr-un șablon de ADN al cărui copie este. Celulele folosesc ARN , în special , ca un purtător intermediar pentru gene pentru a sintetiza in proteinele care au nevoie. ARN-ul poate îndeplini multe alte funcții și, în special, poate interveni în reacțiile chimice ale metabolismului celular .
Din punct de vedere chimic, ARN-ul este un polimer liniar alcătuit dintr-un lanț de nucleotide . Fiecare nucleotidă conține o grupare fosfat , un zahăr ( riboză ) și o bază azotată (sau bază nucleică). Nucleotidele sunt legate între ele prin legături fosfodiesterice . Există patru baze nucleice găsite în ARN: adenină , guanină , citozină și uracil .
ARN-ul are multe asemănări cu ADN-ul , cu toate acestea unele diferențe importante: din punct de vedere structural, ARN conține reziduuri de riboză în care ADN conține dezoxiriboză , ceea ce face ca ARN-ul să fie chimic mai puțin stabil; în plus, timina din ADN este înlocuită acolo cu uracil, care are aceleași proprietăți de împerechere de bază cu adenina. Funcțional, ARN-ul se găsește cel mai adesea în celule într-o formă monocatenară , adică monocatenară, în timp ce ADN-ul este prezent ca două catene complementare care formează o helică dublă . În cele din urmă, moleculele de ARN prezente în celule sunt mai scurte decât ADN-ul genomului , dimensiunea lor variind de la câteva zeci la câteva mii de nucleotide, împotriva a câteva milioane până la câteva miliarde de nucleotide pentru acidul dezoxiribonucleic (ADN).
În celulă, ARN-ul este produs prin transcriere din ADN (care se află în nucleu în eucariote). ARN este deci o copie a unei regiuni a uneia dintre firele de ADN. Enzimele care produc ADN → ARN copiază se numesc ARN polimeraze . ARN-urile astfel produse pot avea trei tipuri principale de funcții: pot fi purtători ai informațiilor genetice ale uneia sau mai multor gene care codifică proteinele (se vorbește apoi de ARN mesager ), pot adopta o structură stabilă secundară și terțiară și pot îndeplini funcții catalitice ( de exemplu ARN ribozomal ), ele pot servi în cele din urmă ca ghid sau matrice pentru funcțiile catalitice efectuate de factorii proteici (care este cazul microARN-urilor, de exemplu ).
Structura ARN
Ribonucleotide
Structura chimicăARN-ul este un acid nucleic , adică o moleculă formată dintr-un lanț ( polimer ) de nucleotide . Fiecare nucleotidă unitară a ARN-ului constă dintr-o pentoză , riboză , ai cărei atomi de carbon sunt numerotați de la 1 ′ la 5 ′, o bază variabilă de azot sau bază nucleică și o grupare fosfat . Nucleobazei este conectat printr - un atom de azot la carbon unul dintre ribozei; iar gruparea fosfat a nucleotidei este legată de carbonul 5 '. Nucleotidele se leagă între ele prin grupări fosfat, gruparea fosfat a unui nucleotid (legat de carbonul 5 ') atașându-se prin legături fosfodiester la carbonii 3' ai nucleotidei următoare.
Cele patru baze principale ale ARN și singurele utilizate în ARN de transfer sunt adenina (notată A), uracil (notată U), citozină (notată C) și guanină (notată G). Comparativ cu ADN-ul, timina din ADN este înlocuită cu uracil în ARN. Diferența dintre aceste două baze este înlocuirea unei grupări metil în poziția 5 a timinei cu un atom de hidrogen în uracil. Această modificare structurală nu modifică proprietățile de asociere cu adenina.
Ribozomul , în special ARN ribosomal și transferul ARN includ alte nucleotide modificate, mai mult de o sută au fost identificate.
StereochimieStructural, prezența unui atom de oxigen în poziția 2 'a influențelor riboza conformație a inelului furanoză de riboză. Acest heterociclu cu cinci atomi nu este plan, ceea ce duce la doi principali conformeri ai zahărului, numiți C2′-endo și C3′-endo. În ARN, care are un atom de oxigen în poziția 2 ', este favorizată poziția C3'-endo, care modifică în profunzime structura elicelor duble cuprinzând firele de ARN. Aceste duplexuri de ARN formează o helică de tip A, diferită de cea observată predominant în ADN-ul convențional, care este o helică de tip B, unde dezoxiriboză se află în conformația C2′-endo.
ARN dublu helix
Helixul de tip A pe care îl adoptă ARN atunci când formează un duplex are proprietăți geometrice destul de diferite de cele ale helixului de tip B. În primul rând, numărul de perechi de baze pe rotație a elicei este de 11 în loc de 10 pentru ADN-ul de formă B. Planul perechilor de baze nu mai este perpendicular pe axa helixului, ci formează un unghi de aproximativ 75 ° cu acesta. Aceasta are ca rezultat o deplasare a axei helixului care nu mai trece prin centrul asocierii bazelor, ci în interiorul canelurii majore. Acest lucru induce o creștere a diametrului helixului care merge de la aproximativ 20 Å pentru ADN în forma B la aproximativ 26 Å pentru ARN în forma A. În cele din urmă, geometria celor două caneluri este profund afectată: canelura majoră devine foarte accesibilă, în timp ce canelura mică devine foarte adâncă, îngustă și ciupită. Acest lucru are un impact asupra modului în care ARN-ul dublu catenar poate interacționa cu proteinele, deoarece îngustimea canelurii minore este o barieră în calea accesibilității liganzilor proteici.
Structura in vitro
Majoritatea ARN-urilor naturale sunt prezente în formă monocatenară (monocatenară) în celulă, spre deosebire de ADN care este sub forma unei catene duble pereche. De toroane ARN ori mai mult pe ei înșiși, formând o structură intramoleculara care poate fi foarte stabil și foarte compact. Baza acestei structuri este formarea împerecherilor interne, între baze complementare ( A cu U , G cu C și, uneori, G cu U ). Descrierea perechilor interne dintre bazele unui ARN se numește structură secundară . Această structură secundară poate fi completată de interacțiuni la distanță care apoi definesc o structură tridimensională sau o structură terțiară .
Formarea structurii ARN este foarte adesea dependentă de condițiile fizico-chimice din jur și în special de prezența, în soluție , a cationilor divalenți , cum ar fi ionul de magneziu Mg 2+ . Acești cationi interacționează cu grupările fosfat ale coloanei vertebrale și stabilizează structura, în special prin protejarea repulsiei electrostatice între sarcinile negative ale acestor fosfați.
Structura terțiară a ARN - ului este baza bogăția sarcinilor lor și , în special , capacitatea lor de a cataliza a reacțiilor chimice ( ribozime ).
Structura secundară
Structura secundară a unui ARN este descrierea tuturor împerecherilor interne dintr-o moleculă monocatenară. Acest set de împerecheri induce o topologie particulară, alcătuită din regiuni elicoidale (tije) și regiuni nepereche (bucle). Prin extensie, structura secundară acoperă și descrierea acestei topologii.
Formarea structurilor secundare într-un ARN monocatenar rezultă din existența regiunilor care conțin secvențe palindromice , care se pot împerechea pentru a forma local o structură cu dublă helix. De exemplu, dacă ARN conține următoarele două secvențe : --GUGCCACG ------ CGUGGCAC-- , acestea formează o secvență palindromică, nucleotidele celui de-al doilea segment fiind complementare cu cele ale primului, după inversarea sensului lor de lectură; aceste două segmente se pot împerechea apoi într-un mod antiparalel pentru a forma o regiune duplex locală. Regiunea dintre cele două segmente formează o „buclă” care leagă cele două fire împerecheate, această împerechere formând o „tijă”. Aceasta este apoi denumită „ac de păr” sau o structură în buclă .
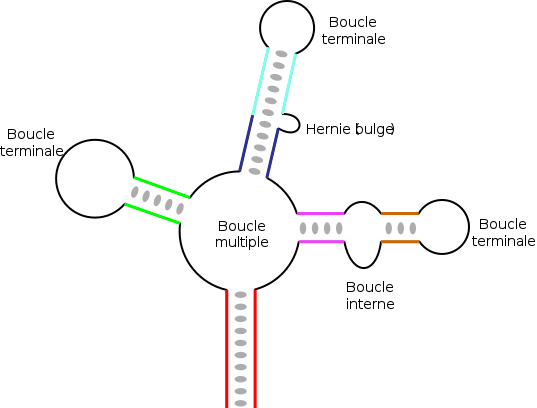
În ARN-urile de lungime mai mare, pot exista structuri mai complexe care rezultă din împerecherea mai multor regiuni complementare sau palindromice . În funcție de modul în care aceste diferite regiuni sunt „cuibărite”, se obțin diverse elemente topologice , cu tije sau regiuni împerecheate și diferite tipuri de bucle:
- cele buclele terminale , situate la capătul unei tije;
- cele buclele interioare , care leagă cele două tije;
- cele mai multe bucle care conecta trei sau mai multe tulpini și formează structura punctelor de racordare;
- hernia (limba engleză protuberanță ) sau bucle laterale , care se află pe una dintre cele două componente ale unei elice. Continuitatea helixului nu este în general afectată, iar bazele rămân stivuite coaxial, de ambele părți ale herniei.
Nu există întotdeauna o singură structură stabilă pentru o anumită secvență și se întâmplă ca anumite ARN să adopte mai multe conformații alternative în funcție de legarea unui ligand ( proteină , moleculă mică etc.) sau de condițiile fizico-chimice ( puterea ionică , pH ). În general, formarea sau fuziunea structurii secundare a unui ARN poate fi urmată de măsurători spectroscopice . Astfel, de exemplu, absorbția în ultraviolete a bazelor ARN este mai mare în starea desfăcută decât în starea pliată (fenomen de hipercromicitate ).
Structura terțiară
Împerecheri necanoniceDincolo de topologia buclelor și helicilor compuse din perechi de baze standard, un ARN poate adopta o structură compactă tridimensională sau o structură terțiară , ca o proteină . În cadrul acestei structuri, helicile canonice sunt completate de împerecheri necanonice, adică distincte de împerecherile clasice, ale lui Watson - Crick ( A = U și G ≡ C ) și wobble ( wobble , G = U ). O mare varietate de astfel de perechi au fost observate în structurile ARN tridimensionale rezolvate prin cristalografie cu raze X sau rezonanță magnetică nucleară . Există, de exemplu, perechile Hoogsteen și „forfecate“ împerecherilor . Există, de asemenea , interacțiuni bază - riboză , în special cu 2 ' hidroxil , care poate forma legături de hidrogen . O nomenclatură sistematică a tuturor acestor interacțiuni a fost propusă de Eric Westhof și colaboratorii săi. Au fost observate peste 150 de tipuri de împerechere și au fost grupate în douăsprezece familii mari. Aceste perechi necanonice implică întotdeauna legături de hidrogen între baze, care sunt coplanare , ca în perechile Watson-Crick.
Interacțiuni la distanță mareÎmperecherile canonice sau necanonice pot apărea între regiunile îndepărtate ale structurii secundare, adesea situate în bucle, ceea ce face posibilă stabilizarea unei plieri compacte a structurii.
Unele dintre aceste interacțiuni non-canonice la distanță lungă includ:
- a pseudoknots , structurile formate prin interacțiunea unei bucle cu o regiune situată în afara tijei care delimiteaza;
- triplex fir , care apar atunci când se introduce un singur catenar regiune în canelura majoră a unei regiuni elicoidale;
- a interacțiunilor tetraloop transceiver : interacțiunile hyperstable între buclele de patru nucleotide (tétraboucles) și structuri duplex sau cvasi-duplex.
Diferențele dintre ADN și ARN
Principalele diferențe dintre cele două molecule sunt că:
- ARN - ul pentru zahăr riboză unde ADN - ul deoxiriboză ;
- baza uracil îndeplinește în ARN funcția îndeplinită de timină în ADN;
- ARN-ul există, în general, în formă monocatenară (monocatenară), cu excepția câtorva viruși, cum ar fi reovirusurile, unde există ca ARN dublu catenar , în timp ce ADN-ul este dublu catenar (dublu catenar) cu o structură cu dublă helică;
- ARN este scurt: de la câteva zeci la câteva mii de nucleotide pentru ARN celular (ARNm sau ARN structurat), împotriva a câteva milioane până la câteva miliarde (trei miliarde la om ) în ADN-ul care constituie genomul celulei.
Primele trei diferențe conferă ARN-ului o stabilitate mult mai mică decât ADN-ul:
- gruparea riboză are un hidroxil în poziția 2 ', care este absent în dezoxiriboză a ADN - ului . Această funcție 2'-OH are implicații multiple pentru structura ARN-ului. În primul rând la nivel chimic, această funcție alcoolică face ARN-ul sensibil la hidroliza alcalină. Prezența celor doi cis oxigen în pozițiile 2 ′ și 3 ′ face posibilă ciclizarea fosfatului în pozițiile 2 ′ și 3 ′, care are loc foarte repede atunci când o bază rupe protonul din 2′-OH. Această ciclizare a nucleotidei provoacă o tăietură a lanțului riboză-fosfat și eliberează capetele 5’-OH și 2 ’, 3’ fosfat ciclic ;

- uracilul este mai puțin costisitor în producția de energie pentru organismele vii decât timina, deoarece necesită o etapă de sinteză mai mică decât metilarea prin timidilat sintază . Prezența timinei în ADN permite celulei să detecteze deteriorarea spontană a citozinei, care este sensibilă la oxidare . Dezaminare citozina spontană , în prezența oxigenului se transformă în uracil. Prezența deoxiuridinei în ADN este anormală, deoarece deoxiribonucleotida complementară a deoxiadenozinei este timidina . Cu această distincție între timină și uracil prin intermediul unei grupări metil, sistemul de bază de reparație excizională poate detecta și corecta defectul. În ARN, dezaminarea citozinelor produce uracili și nu este reparată. Deoarece ARN-ul are o durată de viață mult mai scurtă decât ADN-ul (de ordinul unui minut), acesta este degradat și reciclat;
- dacă un singur fir de ARN este deteriorat, leziunea nu este reparată și dauna este ireversibilă; pe de altă parte, dacă una dintre cele două catene de ADN este deteriorată, celula poate folosi informațiile transportate de catena complementară intactă pentru a repara leziunea .
Din punct de vedere evolutiv, anumite elemente ne permit să credem că ARN-ul ar fi anterior ADN-ului ca purtător de informații genetice, ceea ce ar explica funcțiile sale mai extinse și generalizarea acestuia. ADN-ul ar fi apărut mai târziu și ar fi înlocuit ARN-ul doar pentru rolul de stocare pe termen lung, datorită stabilității sale mai mari.
Sinteza ARN-ului din ADN
Sinteza unei molecule de ARN din ADN se numește transcripție . Este un proces complex care implică o enzimă din familia ARN polimerazei , precum și proteine asociate. Diferitele etape ale acestei sinteze sunt inițierea, alungirea și încetarea. Procesul de sinteză a ARN-ului este semnificativ diferit în organismele procariote și în celulele eucariote . În cele din urmă, după transcrierea efectivă, ARN-ul poate suferi o serie de modificări post-transcripționale ca parte a unui proces de maturare în timpul căruia secvența și structura sa chimică pot fi modificate (vezi mai jos).
Iniţiere
Începutul transcrierii unui ARN de către o ARN polimerază are loc la nivelul unei secvențe specifice pe ADN, numit promotor . Acest promotor cuprinde unul sau mai multe elemente de secvență conservate la care proteinele specifice, factorii de transcripție , sunt în general fixați . Chiar în amonte de locul de inițiere a transcripției, elementul proximal este în general bogat în nucleotide T și A și, prin urmare, este numit cutia TATA în eucariote sau cutia Pribnow în bacterii. Factorii de transcripție promovează recrutarea ARN polimerazei către promotor și deschiderea duplexului ADN. Ceea ce se numește bulă de transcripție se formează apoi cu ADN-ul deschis, una dintre catenele (șablonul) fiind hibridizată cu ARN-ul sintetizat.
Elongaţie
Odată ce ARN polimeraza este fixată pe promotor și se formează bula de transcripție, aceasta sintetizează primele nucleotide într-o manieră statică fără a părăsi secvența promotorului. Factorii de transcripție se rup și ARN polimeraza devine procesivă. Apoi transcrie ARN-ul în direcția 5 'până la 3' , folosind una dintre cele două catene de ADN ca șablon și trifosfații ribonucleotidici ( ATP , GTP , CTP și UTP ) ca precursori.
In vivo , în Escherichia coli , rata de extindere a ARN polimerazei este de aproximativ 50 până la 90 de nucleotide pe secundă.
Rezilierea
Încetarea transcripției ARN se desfășoară în conformitate cu mecanisme complet diferite la bacterii și la eucariote .
La bacterii, principalul mecanism de terminare implică o anumită structură a ARN-ului, terminatorul , constând dintr-o buclă stabilă a tulpinii, urmată de o serie de reziduuri de uridină (U). Când ARN polimeraza sintetizează această secvență, plierea tijei ARN face ca polimeraza să se întrerupă. ARN-ul, care nu mai este asociat cu ADN-ul șablon, decât printr-o serie de perechi slabe AU, se detașează, fără intervenția altor factori proteici. Încetarea se poate face și prin intervenția unui factor proteic specific, factorul Rho.
În eucariote, terminarea transcripției prin ARN polimeraza II este cuplată la poliadenilare . Două complexe proteice, CPSF (en) și CStF (en) recunosc semnalele de poliadenilare (5'-AAUAAA-3 ') și ARN. Ei scindează ARN-ul, induc detașarea ADN polimerazei și recrutează polimeraza poli-A care adaugă coada poli (A) (vezi mai jos).
Maturare
Procesarea ARN-ului cuprinde un set de modificări post-transcripționale observate în principal la eucariote și joacă un rol important în soarta ARN-ului maturizat. Principalele modificări sunt adăugarea unui capac de 5 ′, poliadenilarea de 3 ′, îmbinarea , introducerea modificărilor chimice la nivel de bază sau riboză și în cele din urmă editarea .
CapacCapac sau 5'-cap în limba engleză, este o modificare nucleotidă care este adăugat la capătul 5 ' al ARN - ului mesager în eucariote celule . Acesta constă dintr-un reziduu de guanozină metilat legat de o trifosfat de legătură 5'-5 'la prima nucleotidă transcrisă de ARN polimeraza . Această modificare este introdusă în nucleul celulei, prin acțiunea succesivă a mai multor enzime: polinucleotidă 5'-fosfatază , ARN guanililtransferază , metiltransferază .
Capacul joacă mai multe roluri: crește stabilitatea ARN-ului protejându-l de degradarea prin exonucleaze 5'-3 'și permite, de asemenea, recrutarea factorilor de inițiere a traducerii necesari pentru legarea ribozomului de ARN-uri. Mesagerii celulari. Capacul este, prin urmare, esențial pentru traducerea majorității mARN-urilor.
PoliadenilarePoliadenilarea este adăugarea unei extensii la capătul 3“al ARN - ului format exclusiv din ribonucleotide tip de adenozină (A). Din acest motiv, extensia se numește coadă poli (A) . Deși este compusă din nucleotide standard, această coadă poli (A) este adăugată post-transcripțional de către o enzimă specifică numită poli (A) polimerază și nu este codificată în ADN genomic . Coada poli (A) se găsește în principal la sfârșitul ARN-urilor mesager . În eucariote, poliadenilarea ARNm este necesară pentru translația lor de către ribozom și participă la stabilizarea lor. Coada poli (A) este recunoscută în special de PABP ( proteină de legare poli (A) , „ proteină de legare poli (A) ”).
La bacterii și în anumite mitocondrii , poliadenilarea ARN este, dimpotrivă, un semnal de degradare.
ÎmpletireaDespicare este o modificare post-transcripțional care implică îndepărtarea intronilor și sutura a exonilor din mARN și în unele ARN structurate , cum ar fi ARNt. Găsite în organismele eucariote, intronii sunt segmente de ARN care sunt codificate în genom și transcrise în ARN precursor, dar care sunt eliminate din produsul final. În majoritatea cazurilor, acest proces implică o mașinărie complexă specifică numită spliceozom . Splicarea are loc în nucleul celulelor eucariote, înainte de exportul ARN-ului maturat în citoplasmă.
Nucleotide modificateDupă transcrierea lor de către ARN polimeraza, unii ARN suferă modificări chimice sub acțiunea unor enzime specifice. ARN-uri cheie care suferă modificări sunt ARN -urile de transfer și ARN-urile ribozomale . Se poate considera, de asemenea, că metilațiile implicate în sinteza capacului sunt modificări ale anumitor nucleotide . În cazul general, modificările se pot referi fie la bază, fie la riboză . Principalele modificări întâlnite sunt:
- pe riboză: O- metilări ale poziției 2'-OH;
- pe bază:
- izomerizarea uridinelor care dă pseudouridine ,
- metilații, fie pe atomi de carbon ( ribotimidină ), fie pe atomi de azot ( 7-metilguanozină ...),
- o reducere , care transformă uridines în dihydrouridines ,
- tiolări,
- modificări mai complexe ( prenilare , treonil-carbamoilare etc.).
În ARN-urile de transfer, introducerea nucleotidelor modificate contribuie la creșterea stabilității moleculelor.
EditareaEditarea ARN constă într-o modificare a secvenței acidului ribonucleic, ulterior transcripției prin ARN polimerază. La sfârșitul procesului de editare, secvența ARN este, prin urmare, diferită de cea a ADN-ului. Modificările făcute pot fi modificarea unei baze, înlocuirea unei baze sau adăugarea uneia sau mai multor baze. Aceste modificări sunt efectuate de enzime care acționează asupra ARN-ului, cum ar fi citidina deaminază , care transformă reziduurile chimice ale citidinei în uridină .
Funcția în celulă
În celule, ARN-urile îndeplinesc patru roluri distincte și complementare:
- suport temporar pentru informații genetice : ARN-ul mesager îndeplinește acest rol, este utilizat de celulă pentru a transmite informațiile corespunzătoare unei gene date în afara nucleului, apoi pentru a sintetiza proteinele din aceste informații;
- catalizator enzimatic : La fel ca proteinele , ARN-urile se pot plia în trei dimensiuni pentru a forma structuri complexe. Aceste structuri permit anumitor ARN-uri să se comporte ca niște enzime , aceasta se numește ribozimă . Ribozomului , The P ribonuclează și unele introni sunt ribozomi . Există argumente indirecte care indică faptul că mecanismul de îmbinare ARN mesager ( spliceozomul ) este, de asemenea, un ribozim, deși acest lucru nu a fost încă demonstrat în mod formal;
- ghid pentru enzime : unele ARN-uri sunt utilizate ca cofactori de către proteine pentru a permite direcționarea lor către secvențe specifice. Printre acestea sunt mici RNAs nucleolari (snoRNAs), care ghidează ribozomale ARN - enzime modificatoare , ARN telomeric, care este un cofactor al telomerazei , enzima care face capetele de cromozomi, sau RNAs de interferență ;
- regulatori ai expresiei genice : anumiți ARN necodificatori joacă un rol în reprimarea expresiei anumitor gene sau grupuri de gene. Acesta este cazul, de exemplu, cu ARN-urile antisens care se împerechează cu un ARN țintă și blochează translația acestuia de către ribozom.
O clasă specială de ARN, ARN-uri de transfer, se găsește la interfața multora dintre aceste funcții prin ghidarea aminoacizilor în timpul traducerii .
În cele din urmă, genomul unor viruși este alcătuit exclusiv din ARN și nu din ADN. Acesta este în special cazul virusurilor gripale , SIDA , hepatitei C , poliomielitei și virusului Ebola . În funcție de caz, replicarea acestor viruși poate trece printr-un intermediar ADN ( retrovirus ), dar se poate face și direct de la ARN la ARN.
ARN este o moleculă versatilă, care l-a determinat pe Walter Gilbert , co-inventator al secvențierii ADN - ului , să propună în 1986 o presupunere că ARN-ul ar fi cel mai vechi dintre toate macromoleculele biologice. Această teorie, cunoscută sub numele de RNA world hypothesis („ RNA world hypothesis ”), face posibilă depășirea unui paradox al oului și al puiului care apare atunci când cineva caută să știe care dintre proteine ( catalizatori ) și care dintre ADN (genetic) informație) a apărut mai întâi. În acest model, ARN-ul, capabil să combine ambele tipuri de funcții în același timp, ar fi precursorul universal.
ARN Messenger
Informația genetică conținută în interiorul ADN - ul nu este utilizat în mod direct de către celula pentru a sintetiza proteinei . Pentru aceasta, folosește copii tranzitorii ale informațiilor genetice care sunt ARN-uri mesagere sau ARNm. Fiecare ARN mesager poartă unul sau, uneori, mai multe cistroni , adică instrucțiunile pentru formarea unei singure proteine. Prin urmare, corespunde copiei doar a uneia dintre genele genomului (se vorbește atunci de ARNm monocistronic) sau uneori de câteva ( ARNm policistronic ).
ARN Messenger conține o copie a uneia dintre cele două catene de ADN, cea codificatoare, și nu secvența complementară. Comparativ cu secvența de genă conținută în ADN - ul genomului, care a ARNm corespunzător poate conține modificări, în special datorită splicing (vezi mai sus) care elimină regiunile necodificatoare . ARN mesager sintetizat în nucleul celulei este exportat în citoplasmă pentru a fi tradus în proteină. Spre deosebire de ADN, care este o moleculă perenă, prezentă pe tot parcursul vieții celulei, ARN-urile mesagere au o durată de viață limitată, de la câteva minute la câteva ore, după care sunt degradate și reciclate.
Un ARN mesager are trei regiuni distincte: o regiune 5 'netradusă numită 5'-UTR, situată în amonte de cistronul sau cistronii pe care îi poartă; o regiune de codare corespunzătoare acestui sau acestor cistroni; și în cele din urmă, o regiune netradusă de 3 ′ numită 3′-UTR. ARN-urile mesager sunt traduse în proteine de către ribozomi . Regiunea 5 'netradusă conține în general semnalele de translație care permit recrutarea ribozomului pe cistron. Procesul de traducere implică, de asemenea, ARN-uri de transfer care furnizează ribozomului aminoacizii necesari biosintezei proteinelor . În interiorul ribozomului, prin anticodonul lor , ARNt se împerechează succesiv cu tripletele de bază sau codonii secvenței ARNm. Când asocierea codon-anticodon este corectă, ribozomul adaugă aminoacidul transportat de ARNt la proteina care este sintetizată. Corespondențele dintre codoni și aminoacizi constituie codul genetic .
Funcția ARN-urilor de mesagerie este multiplă. Pe de o parte, fac posibilă păstrarea șablonului ADN original, care nu este utilizat direct pentru traducere, celula funcționând doar pe copia care este ARNm. Mai presus de toate, existența ARN-urilor mesager oferă celulei un mecanism crucial pentru reglarea ciclului de producție a proteinelor din genom. Nevoia celulară pentru o anumită proteină poate varia în funcție de mediu, tipul de celulă, stadiul de dezvoltare. Prin urmare, sinteza proteinelor trebuie activată sau oprită în funcție de condițiile celulare. Reglarea transcrierii ADN-ului în ARNm răspunde acestei nevoi și este controlată de factori de transcripție specifici care acționează asupra promotorilor genelor țintă. Când cantitatea unei proteine date este suficientă, transcripția ARNm este inhibată, este degradată treptat și producția de proteine încetează. Prin urmare, este important ca ARNm să fie o moleculă tranzitorie, pentru a putea realiza această reglare esențială.
Transfer de ARN
Transfer de ARN , sau ARNt sunt ARN scurt, lung aproximativ 70 până la 100 ribonucleotida implicate în abordarea aminoacizilor la ribozomului în timpul traducere .
ARN-urile de transfer au o structură caracteristică a frunzei de trifoi, formată din patru tulpini împerecheate. Una dintre aceste tulpini este terminată de o buclă care conține anticodonul , tripletul de nucleotide care se împerechează cu codonul în timpul translației unui ARNm de către ribozom . La celălalt capăt, ARNt poartă aminoacidul corespunzător atașat printr-o legătură ester la capătul său 3'-OH. Această esterificare este catalizată de enzime specifice, aminoacil-tARN AR sintetaze . În trei dimensiuni, structura frunzei de trifoi se pliază într-o formă "L", cu anticodonul la un capăt și aminoacidul esterificat la celălalt capăt.
Toate celulele vii conțin un set de ARNt diferiți care poartă aminoacizi diferiți și capabili să citească codoni diferiți.
ARN-urile de transfer sunt uneori denumite „adaptoare” între secvența genetică și secvența proteică . A fost Francis Crick , care a propus existența acestor adaptoare, chiar inainte de descoperirea lor în 1958.
ARN-uri catalitice sau ribozime
Descoperirea ARN - ului , cu o capacitate de catalizator a fost făcută în 1980, în special de echipa Thomas Cech , care a lucrat la introni ai genei de ARN ribozomal de protozoarul ciliate Tetrahymena și Altman Sidney , care a studiat P ribonuclează , enzimă de maturare a ARNt . Cech și Altman au primit Premiul Nobel pentru chimie în 1989 pentru această descoperire.
În ambele cazuri, ARN-ul singur este capabil să catalizeze o clivare specifică (clivaj) sau o reacție de transesterificare în absența proteinelor . Aceste ARN-uri catalitice au fost numite ribozime deoarece sunt enzime formate din acid ribonucleic. În cazul intronului Tetrahymena , acesta este un auto-splicing , intronul fiind propriul său substrat , în timp ce ribonucleaza P este o enzimă care acționează în trans , pe mai multe substraturi.
De la aceste descoperiri inițiale, au fost identificate și alte ribozime naturale:
- ARN-uri de la viroizi sau viruși prin satelit (virusoizi) care sunt capabili să se despice;
- în prezent , există argumente foarte puternice, bazate pe rezoluția structurii sale 3D, pentru a afirma că ribozomului , complexul ribonucleoproteina responsabil pentru traducerea de ARNm în proteine , este ea însăși o ribozimă. Cele două situri active ale ribozomului, centrul de decodare de pe subunitatea mică și centrul peptidiltransferazei care formează legăturile peptidice , sunt de fapt compuse exclusiv din segmente de ARN ribozomal;
- spliceosome , care catalizează despicare de citoplasmatice mRNAs de eucariotelor , este , probabil , de asemenea , o ribozimă;
- anumite riboswitches , care sunt regiuni de reglare structurate purtate de ARN mesager, au activitate de clivaj catalitic în prezența unui ligand ;
- În cele din urmă, există ribozime sintetice, care au fost izolate prin metode evolutive in vitro , cum ar fi tehnica SELEX . Au fost astfel izolate ARN-uri catalitice sintetice capabile să catalizeze o mare varietate de reacții chimice și să lege o mare varietate de liganzi, ceea ce a fost interpretat ca un argument în favoarea ipotezei lumii ARN . Astfel de ARN-uri sintetice sunt uneori numite aptameri , deoarece sunt „apți” pentru a îndeplini o sarcină dată.
În general, în toate aceste ribozime, plierea lor specifică este cea care le permite să recunoască substratul și cataliza lor, ca în cazul enzimelor proteice.
Ghiduri ARN
Ghidul RNAs sunt RNAs care se combina cu enzime proteice și servesc pentru a ghida acțiunea lor asupra complementare ale secvenței RNAs sau ADNurile . ARN-ul ghid se împerechează cu acidul nucleic substrat și ajută la direcționarea activității enzimei. Au fost identificate mai multe tipuri:
- mici ARN nucleolar sau snoARN : în nucleol celulelor eucariote, ele directe actiunea de modificare enzime ARN ribozomal, în particular 2'-O-metilarea prin snoARN C / D și de pseudouridylations H / ACA snoRNAs. Acest mecanism permite celulei să modifice în mod specific mai multe poziții ale ARNr, cu o singură enzimă folosind diferite snoRNA-uri ca ghiduri. SnoARN-urile sunt adesea codificate de secvențe intronice ;
- microARN - urile sunt, de asemenea, ARN-uri de ghid implicate în procesul de interferență a ARN-ului : asociate cu un complex proteic numit RISC ( complexul de mutare indus de ARN ), acești ARN mici determină o deteriorare a mARN-ului țintă cu care se împerechează, fie o reprimare a traducerii acestuia ;
- TERC ( componenta ARN telomerază ), subunitatea ARN a telomerazei : acest ARN structurat este asociat cu transcriptaza inversă care sintetizează telomerii , capetele cromozomilor . Conține o secvență care servește ca substrat pentru telomerază pentru a sintetiza ADN telomeric de secvență complementară. Prin urmare, ghidează activitatea enzimei, dar servind ca șablon, mai degrabă decât formând o pereche cu substratul;
- lincARN prezent la mamifere sunt mari RNAs noncoding intergenicâ dar transcriu ca ARNm prin ARN polimeraza II. Lungimea lor le permite să adopte o structură tridimensională complexă. Aceste structuri permit interacțiunea lor cu diferiți cofactori transcripționali, cum ar fi hnRNP-K sau PRC2 (în principal inhibitori ai transcripției). Acești complecși sunt apoi ghidați de lincRNA pe secvențele reglatoare ale genelor pentru a inhiba exprimarea lor. Legarea lincRNA-urilor cu ADN-ul ar presupune o împerechere a bazelor ARN cu bazele ADN corespunzătoare după nepotrivirea dublei spirale ADN sau chiar formarea triplului helix ADN-ADN-ARN.
Regulatori de ARN
Anumiți ARN joacă un rol de regulatori direcți ai expresiei genelor. Acesta este în special cazul ARN-urilor necodificatoare care posedă regiuni complementare ARN-urilor de mesagerie celulară și care, prin urmare, se pot împerechea cu aceștia pentru a forma local o catenă dublă de ARN. Acești ARN antisens pot fi derivați din același locus genetic cu ARN-ul lor țintă, prin transcrierea catenei complementare, acesta fiind denumit apoi ARN cis- regulator. Ele pot fi, de asemenea, derivate din transcrierea unei alte regiuni a genomului, acestea fiind apoi ARN-uri de reglare trans .
Împerecherea ARN-ului de reglementare cu ARN-ul său mesager țintă poate acționa asupra capacității acestuia din urmă de a fi tradusă de ribozom sau asupra stabilității acestuia, ceea ce duce la o reglare a traducerii genei (genelor) purtate de ARN. . La bacterii, există astfel multe exemple de cis anti-sens - sau ARN trans- reglator care blochează locul de pornire a traducerii. De exemplu, gena care codifică proteinele porin OmpF este reglată de un ARN antisens numit MicF.
În eucariote , există și ARN-uri de reglare mari, care sunt implicate în procesele de reglare epigenetice . Cel mai cunoscut exemplu este cel al ARN - ului Xist la mamifere. Acest lucru inactivează nu o genă, ci un întreg cromozom. Xist acoperă unul dintre cei doi cromozomi X ai fiecărei celule la indivizii de sex feminin care astfel devin inactivi. Doar unul dintre cei doi cromozomi ai perechii XX este astfel activ, ceea ce face posibil să existe același nivel de expresie a genelor purtate de cromozomul X ca la indivizii masculi, care au doar unul. Inactivarea X este un proces aleatoriu, care poate duce la exprimarea diferitelor fenotipuri de către celule diferite, la aceeași femeie. Acesta este de exemplu cazul culorii hainei la pisici.
Utilizări terapeutice și biotehnologice
ARN-ul este utilizat astăzi într-o serie de aplicații în biologia moleculară, în special datorită procesului de interferență a ARN-ului , care constă în introducerea în celule eucariote a fragmentelor scurte de ARN bicatenar denumite „ ARN-uri cu interferență mică ”. Aproximativ douăzeci de perechi de baze lungi, acești ARN-uri mici interferente (ARNp) sunt utilizate de o mașinărie celulară capabilă să degradeze ARNm într-un mod specific. Numai mARN-urile care conțin o secvență corespunzătoare celei de pRNAi sunt degradate, ceea ce face posibilă scăderea selectivă a expresiei unei proteine date. Această abordare tehnologică este mult mai simplă și mai rapidă decât stabilirea liniilor de șoarece inactivate ( knock-out ) și se numește knock-down .
Încercările de utilizare a acestei tehnici în scopuri terapeutice sunt avute în vedere, de exemplu, prin direcționarea genelor virale pentru combaterea infecțiilor sau a oncogenilor , în cazul cancerelor. Cu toate acestea, acestea necesită stabilizarea ARN-urilor mici care interferează (pRNAi) pentru a evita degradarea lor de către ribonucleaze și pentru a-și viza acțiunea către celulele în cauză.
Istoric
Cele Acizii nucleici au fost descoperite în 1868 de către Friedrich Miescher . Miescher a numit noua substanță „nucleină”, deoarece a fost găsită în nucleul celulelor. Prezența acizilor nucleici în citoplasma drojdiei a fost identificată în 1939 și a fost stabilită natura ribonucleică a acestora, spre deosebire de cromozomii care conțin ADN cu dezoxiriboze.
În jurul anului 1940 , biologul belgian Jean Brachet a studiat moleculele până atunci puțin caracterizate, care erau încă numite la acea vreme „acizi timonucleici și zimonucleici” (ADN și respectiv ARN). El descoperă că acidul timonucleic este o componentă a cromozomilor și că este sintetizat atunci când celulele se divid după fertilizare . El evidențiază existența acizilor zononucleici (ARN) în toate tipurile de celule: în nucleu , nucleol și citoplasmă a tuturor celulelor (în timp ce la momentul respectiv se credea că aceste molecule erau caracteristice celulelor vegetale și ale eucariotelor inferioare, cum ar fi drojdiile ). În cele din urmă, arată că acești acizi sunt deosebit de abundenți în celule (mai ales în ergastoplasmă ) care sunt foarte active în ceea ce privește sinteza proteinelor . Au fost stabilite bazele fundamentale ale biologiei moleculare . Anul era 1940. În perioada postbelică, lui Brachet i s-a alăturat biologul molecular belgian Raymond Jeener, care va participa activ la cercetarea rolului ARN-ului în biosinteza proteinelor .
La sfârșitul anilor 1950, Severo Ochoa a reușit să sintetizeze moleculele de ARN in vitro cu ajutorul unei enzime specifice, polinucleotidul fosforilază, care a făcut posibilă studierea proprietăților chimice și fizice ale ARN-ului.
Rolul ARN-ului ca „mesager” intermediar între informațiile genetice conținute în ADN și proteine a fost propus în 1960 de Jacques Monod și François Jacob în urma unei discuții cu Sydney Brenner și Francis Crick . Demonstrația existenței ARN mesager a fost făcută de François Gros . Apoi, descifrarea codului genetic a fost efectuată de Marshall Nirenberg în prima jumătate a anilor 1960. Pentru aceasta, el a folosit ARN-uri sintetice de secvență de nucleotide cunoscute, ale căror proprietăți de codare le-a studiat.
Ribozomii au fost observați pentru prima dată de biologul belgian Albert Claude la începutul anilor 1940. Folosind tehnici de fracționare subcelulară și microscopie electronică , el a dezvăluit „particule mici” de natură ribonucleoproteică, prezente în toate tipurile de celule. Celule vii. El le-a numit „microsomi”, redenumiți ulterior ribozomi.
Structura secundară a ARNt a fost stabilită de Robert Holley , care a reușit să purifice și să analizeze secvența ARNt specifică alaninei în 1964. Acesta a fost un progres major în înțelegerea descifrării mesajului genetic purtat de aceștia. ARN mesager. Structura tridimensională a unui ARNt a fost rezolvată în 1974, independent, de către echipele lui Aaron Klug și Alexander Rich, arătând pentru prima dată structura complexă a unui ARN. Existența proprietăților catalitice ale ARN-urilor a fost stabilită în mod independent de Sidney Altman și Tom Cech în 1982, pe ribonucleaza P pe de o parte și pe intronii de auto-îmbinare pe de altă parte. Rezoluția structurii subunităților individuale ale ribozomului în 2000 de către echipele lui Tom Steitz , Ada Yonath și Venki Ramakrishnan , apoi cea a întregului ribozom de către echipa lui Harry Noller în 2001, a constituit un progres esențial în înțelegerea mecanismul central al biologiei care este translația ARNm în proteine. În plus, a permis să se arate, printre altele, că ribozomul a fost, de asemenea, un ribozim.
În anii 1970, Timothy Leary , în lucrarea sa Politica extazului , a văzut în ARN promisiunea unei viitoare modificări a conștiinței (posibil prin intermediul unor noi medicamente și / sau exerciții spirituale), inclusiv ar fi o componentă care crește capacitățile de învățare ale unul care s-ar angaja în astfel de experiențe.
Ipoteza lumii ARN
Ipoteza ARN mondial este o ipoteză conform căreia ARN - ul este precursorul tuturor biologice macromolecule și în special a ADN - ului și a proteinelor care ar fi permis într - un abiotic mediu (caracterizat printr - o chimie prebiotic , care este parțial ipotetic) l apariție“al primului vii celule, adică formând un compartiment și cuprinzând informații și subsisteme metabolice.
În contextul studiului originilor vieții , această ipoteză permite o explicație a apariției diferitelor funcții biologice prin constituirea anumitor blocuri biomoleculare din intermediari și molecule prebiotice plauzibile pe bază de carbon. În 2009 , echipa lui John Sutherland a arătat că precursorii plauzibili ai ribonucleotidelor, aminoacizilor și lipidelor pot fi obținuți prin omologarea reductivă a cianurii de hidrogen și a unora dintre derivații săi. Fiecare dintre subsistemele celulare cunoscute ar putea fi, prin urmare, explicat prin chimia carbonului, cu reacții catalizate de lumină ultravioletă a priori foarte prezente înainte de apariția stratului de ozon , din hidrogen sulfurat ca agent reducător. Ciclul fotoreductiv ar putea fi el însuși accelerat de cupru [Cu (I) -Cu (II)].
Note și referințe
- (în) Rebecca K. Montange și Robert T. Batey , „ Structura elementului de reglare a ARNm riboswitch S-adenosilmetionină ” , Nature , vol. 441, nr . 7097,29 iunie 2006, p. 1172-1175 ( PMID 16810258 , citiți online )
- H. Lodish , A. Berk , P. Matsudaira , CA Kaiser , M. Krieger , MP Scott , L. Zipursky și J. Darnell , Biologia moleculară a celulei , Bruxelles, de Boeck,2005, 3 e ed. ( ISBN 978-2804148027 )
- (ro) Wolfram Saenger , Principiile structurii acidului nucleic , Springer,1984( ISBN 0-387-90762-9 )
- (în) ianuarie Barciszewski și Brian Frederick Carl Clark , ARN biochimie și biotehnologie , Springer,1999, 73-87 p. ( ISBN 0-7923-5862-7 , OCLC 52403776 )
- Modificarea și editarea Rna. Henri Grosjean, Rob Benne. ASM Press, 1998.
- Marie-Christine Maurel, Anne-Lise Haenni: Lumea ARN: ipoteze, fapte și rezultate experimentale.
- (în) Domnul Sudaralingam , „ Stereochimia acizilor nucleici și a constituenților lor. IV. Conformații permise și preferate ale nucleozidelor, nucleozidelor mono-, di-, tri-, tetrafosfaților, acizilor nucleici și polinucleotidelor ” , Biopolimeri , vol. 7, n o 6,1969, p. 821-860 ( citește online )
- (în) R. Langridge și PJ Gomatos , „ Structura ARN-ului. ARN-ul reovirusului și ARN-ul de transfer au structuri tridimensionale similare, care diferă de ADN. » , Știință , vol. 141, nr . 4,1963, p. 694-698 ( PMID 13928677 )
- (ro) HR Drew , RM Wing , T. Tanako , C Broka , S Tanaka , K Itakura și RE Dickerson , „ Structura unui dodecamer B-ADN: conformație și dinamică. » , Proc. Natl. Acad. Știință. SUA , vol. 78, nr . 4,Aprilie 1981, p. 2179-2183 ( PMID 6941276 , citiți online )
- (în) Peter S. Klosterman , Sapan A. Shah și Thomas A. Steitz , „ Structurile cristaline a două duplexuri ARN control de copiere plasmidice legate: Un duplex cu 18 perechi de baze la rezoluție 1,20 A și un duplex cu pereche de 19 baze la rezoluție 1,55 A . ” , Biochimie , vol. 38, n ° 45,1999, p. 14784-14792 ( PMID 10555960 , DOI 10.1021 / bi9912793 , citiți online )
- (ro) JM Rosenberg , NC Seeman , JJ Kim , FL Suddath , HB Nicholas și A. Rich , „ Double Helix at atomic resolution. » , Natura , vol. 243, nr . 5403,1973, p. 150-154 ( PMID 4706285 , citiți online )
- (în) RO Day , NC Seeman , MJ Rosenberg și A. Rich , " Un fragment cristalin al helixului dublu: structura fosfatului dinucleozidic Guanylyl-3 ', 5'-Citidine. » , Proc. Natl. Acad. Știință. SUA , vol. 70, n o 3,Martie 1973, p. 849-853 ( PMID 4514996 , citiți online )
- (în) Alexander Rich și David R. Davies , „ O nouă structură elicoidală cu două fire: acidul poliadenilic poliaridilic și acidul ” , J. Am. Chem. Soc. , vol. 78, nr . 14,1956, p. 3548-3549 ( DOI 10.1021 / ja01595a086 , citiți online )
- (în) OF Draper , „ Recunoașterea proteinei-ARN ” , Annu. Rev. Biochimie. , vol. 64,1995, p. 593-620 ( PMID 7574494 , citiți online )
- (în) SA Woodson , " Ionii metalici și plierea ARN: un subiect foarte încărcat cu un viitor dinamic " , Curr. Opin. Chem. Biol. , vol. 9, n o 2Aprilie 2005, p. 104-9 ( PMID 15811793 , citiți online )
- (în) P. Doty , H. Boedtker , JR Fresco , R. Haselkorn și M. Litt , " Structura secundară în acizi ribonucleici " , Proc. Natl. Acad. Știință. SUA , vol. 45, nr . 4,1959, p. 482-499 ( PMID 16590404 )
- F. Dardel și F. Képès , Bioinformatică: genomică și post-genomică , Editions de l'École Polytechnique,2002, 153-180 p. ( ISBN 978-2730209274 )
- (în) AM Michelson , „ Hipercromicitate și acizi nucleici. » , Natura , vol. 182, nr . 4648,1958, p. 1502-1503 ( PMID 13613306 )
- (în) K. Hoogsteen , „ Structura cristalină și moleculară a complexului legat de hidrogen între 1 și 9-metiltimină metiladenină. » , Acta Cryst. , vol. 16,1963, p. 907-916 ( DOI 10.1107 / S0365110X63002437 )
- (în) HA Heus și A. Pardi , „ Caracteristici structurale care dau naștere la stabilitatea neobișnuită a agrafelor de ARN care conțin bucle NRMA. » , Știință , vol. 253, nr . 50161991, p. 191-194 ( PMID 1712983 )
- (în) NB Leontis și E. Westhof , „ Perechile de baze non-Watson-Crick și matricile lor asociate izostericității. ” , Acizi nucleici Res. , vol. 30, nr . 16,2002, p. 3497-3531 ( PMID 12177293 )
- (în) DW Staple și SE Butcher , " Pseudoknots: Structuri de ARN cu funcții diverse. » , PloS Biol. , vol. 3, n o 6,2005, e213 ( PMID 15941360 , citiți online )
- (în) domnul Costa și F. Michel , „ Folosirea frecventă a modelului terțiar sami de către ARN-uri auto-pliabile ” , EMBO J. , Vol. 14,1995, p. 1276–1285 ( PMID 7720718 , citiți online )
- (în) PJ Gomatos și I. Tamm , „ Structura secundară a ARN-ului reovirusului ” , Proc. Natl. Acad. Știință. SUA , vol. 49, nr . 5,1963, p. 707-714 ( PMID 16591092 )
- (în) R. Markham și JD Smith , „ Structura acizilor ribonucleici 1. nucleotide ciclice și produse prin ribonuclează prin hidroliză alcalină ” , Biochem. J. , voi. 52, nr . 4,1952, p. 552-557 ( PMID 13018277 , citiți online )
- Walter Gilbert, „ The RNA World ”, Nature 319, 1986, p. 618
- Biochimia lui Harper, Harold A Harper, A Harold
- (în) ST Smale și JT Kadonaga , " Promotorul nucleului ARN polimerazei II " , Ann. Rev. Biochimie. , vol. 72,2003, p. 449-479 ( PMID 12651739 , citiți online )
- (în) RP Lifton , L. Goldberg , RW Karp și DS Hogness , „ Organizarea genelor histonice în Drosophila melanogaster: implicații funcționale și evolutive ” , Cold Spring Harb. Grozav. Cant. Biol. , vol. 42,1978, p. 1047-1051 ( PMID 98262 , citiți online )
- (în) D. Pribnow , " Secvența nucleotidică a site-ului web de legare a ARN polimerazei la un promotor timpuriu T7 " , Proc. Natl. Acad. Știință. SUA , vol. 72,1975, p. 784-788 ( PMID 1093168 , citiți online )
- (în) BA Hamkalo și OL Miller , „ electronmicroscopia activității genetice ” , Annu. Rev. Biochimie. , vol. 42,1973, p. 376-396 ( PMID 4581229 )
- (în) WR McClure și Y. Chow , " Cinetica și procesivitatea polimerazelor cu acid nucleic " , Metode Enzimol. , vol. 64,1980, p. 277-297 ( PMID 6990186 , citiți online )
- (în) H. Bremer și PP Dennis, "Modularea compoziției chimice și a altor parametri ai celulei prin rata de creștere" în Neidhardt FC, R Curtiss, III, JL Ingraham ECC Lin KB Low, B Magasanik WS Reznikoff, M Riley, M Schaechter și HE Umbarger, Escherichia coli și Salmonella typhimurium Biologie celulară și moleculară , Washington, DC, ASM Press,1996( ISBN 0-914826-89-1 , citit online ) , p. 1553-1569
- (în) S. Adhya și domnul Gottesman , „ Control of transcription termination ” , Annu. Rev. Biochimie. , vol. 47,1978, p. 967-996 ( PMID 354508 , citiți online )
- (în) MS Ciampi , " Terminatoarele și determinarea transcripției dependente de Rho " , Microbiology , vol. 152,2006, p. 2515-2528 ( PMID 16946247 , citiți online )
- (în) domnul Edmonds , " O istorie a secvențelor poli A: de la formare la factori la funcție " , Prog. Acid nucleic res. Mol. Biol. , vol. 71,2002, p. 285-389 ( PMID 12102557 , citiți online )
- (ro) AK Banerjee , " structura terminală 5'-cap în acizii ribonucleici mesageri eucariotici " , Microbiol. Rev. , vol. 44, n o 21980, p. 175-205 ( PMID 6247631 , citiți online )
- (în) domnul Edmonds și R. Abrams , „ biosinteza polinucleotidelor: formarea unei secvențe de unități de adenilat din adenozin trifosfat de către o enzimă din nucleii timusului ” , J. Biol. Chem. , vol. 235,1960, p. 1142-1149 ( PMID 13819354 , citiți online )
- (în) domnul Dreyfus și P. Regnier , „ Coada poli (A) a ARNm: bodyguard în eucariote, bacterii în scavenger ” , Cell , vol. 111,2002, p. 611-613 ( PMID 12464173 , citiți online )
- (în) JP Staley și C. Guthrie , „ Dispozitive mecanice ale spliceozomului: motoare, ceasuri, arcuri și lucruri ” , Cell , vol. 92,1998, p. 315-326 ( PMID 9476892 , citiți online )
- (în) WE Cohn , " Pseudouridina, o ribonucleozidă legată de carbon-carbon în acizi ribonucleici: izolare, structură și caracteristici chimice " , Journal of Biological Chemistry , vol. 235,1960, p. 1488-1498 ( PMID 13811056 , citiți online )
- (în) JA Kowalak JJ Dalluge , JA McCloskey și KO Stetter , „ Rolul modificării posttranscripționale în stabilizarea ARN-ului de transfer de la hipertermofil. ” , Biochimie , vol. 28,1994, p. 7869-7876 ( PMID 7516708 )
- (ro) S. Valadkhan , A. Mohammadi , Y. Jaladat și S. Geisler , „ ARN-urile nucleare mici fără proteine catalizează o reacție de îmbinare în doi pași. » , Proc. Natl. Acad. Știință. SUA , vol. 106,2009, p. 11901-11906 ( PMID 19549866 )
- (în) S. Brenner , F. Jacob și M. Meselson , „ Un intermediar instabil care transportă informații de la gene la ribozomi pentru sinteza proteinelor. » , Natura , vol. 190,1961, p. 576-581
- (în) BN Ames și RG Martin , „ Aspecte biochimice ale geneticii: operonul. » , Annu. Rev. Biochimie. , vol. 33,1964, p. 235-258 ( PMID 14268834 )
- (în) C. Yanofsky , „ Stabilirea naturii codului genetic triplet. ” , Cell , vol. 128,2007, p. 815-818 ( PMID 17350564 )
- (în) Huijing Shi și Peter B. Moore , " Structura cristalină a ARNt fenilalaninei de drojdie la rezoluție 1,93 Å: O structură revizuită clasic " , ARN , Vol. 6, n o 8, august 2000, p. 1091-1105 ( PMID 10943889 , PMCID 1369984 , DOI 10.1017 / S1355838200000364 , citiți online )
- (în) MB Hoagland , ML Stephenson , JF Scott , HI Hecht și PC Zamecnik , „ Un acid ribonucleic solubil intermediar în sinteza proteinelor ” , J. Biol. Chem. , vol. 231,1958, p. 241-257 ( PMID 13538965 )
- (în) RW Holley , J. Apgar , GA Everett , JT Madison , M. Marquisee , SH Merrill , JR Penswick și A. Zamir , " Structura unui acid ribonucleic " , Știință , vol. 147,1965, p. 1462-1465 ( PMID 14263761 )
- (en) JD Robertus , JE Ladner , JT Finch , D. Rhodes , RS Brown , BF Clark și A. Klug , „ Structura de ARNt de fenilalanină de drojdie la o rezoluție de 3 A. » , Natura , vol. 250,1974, p. 546–551 ( PMID 4602655 ), (ro) SH Kim , FL Suddath , GJ Quigley , A. McPherson , JL Sussman , AH Wang , NC Seeman și A. Rich , „ Structura terțiară terțiară a ARN-ului de transfer de fenilalanină de drojdie. » , Știință , vol. 250,1974, p. 546–551 ( PMID 4601792 )
- (în) Francis H. Crick , „ We protein synthesis ” , Symp. Soc. Exp. Biol. , vol. 12,58, p. 138-163 ( PMID 13580867 , citiți online )
- (ro) K. Kruger , PJ Grabowski , AJ Zaug , J. Sands , DE Gottschling și TR Cech , „ ARN auto-splicing: autoexcizie și autociclizare a secvenței de intervenție a ARN ribozomal al Tetrahimenei. ” , Cell , vol. 31,1982, p. 147-157 ( PMID 6297745 )
- (ro) C. Guerrier-Takada , K. Gardiner , T. Marsh , N. Pace și S. Altman , „ Porțiunea ARN a ribonuclează P este subunitatea catalitică a enzimei. ” , Cell , vol. 35,1983, p. 849-857 ( PMID 6197186 )
- (în) AC Forster și Davies , „ Caracterizarea auto-clivării ARN-ului viroid și virusoid. " , Metode Enzymol. , vol. 181,1990, p. 583-607 ( PMID 2199768 )
- (în) TR Cech , „ Biologie structurală. Ribozomul este un ribozim. » , Știință , vol. 289,2000, p. 878-879 ( PMID 10960319 )
- (în) I Barrick , KA Corbino , WC Winkler , A. Nahvi , Mr. Mandal , J. Collins , Mr. Lee , A. Roth , N. Sudarsan I. Jona , JK Wickiser și RR Breaker , „ Noi motive ARN sugerează un domeniu extins pentru riboswitches în controlul genetic bacterian. » , Proc. Natl. Acad. Știință. SUA , vol. 101,2004, p. 6421-6426 ( PMID 15096624 )
-
(în) AD Ellington și JW Szostak , " Selecția in vitro a moleculelor de ARN care leagă liganzi specifici. » , Natura , vol. 346,1990, p. 818-822 ( PMID 1697402 )
(ro) C. Tuerk și L. Gold , „ Evoluția sistematică a liganzilor prin îmbogățire exponențială: liganzi ARN la bacteriofagul T4 ADN polimerază. » , Știință , vol. 249,1990, p. 505-510 ( PMID 2200121 ) - (în) Z. Kiss-László , Y. Henry , JP Bachellerie , Mr. Caizergues Ferrer și T. Kiss , " Metilarea ribozei specifice site-ului ARN preribosomal: o funcție nouă pentru ARN-urile nucleolare mici. ” , Cell , vol. 85,1996, p. 1077-1088 ( PMID 8674114 )
- (ro) J. Liu , „ ARN nucleolare mici codificate intron noi. ” , Cell , vol. 75,1993, p. 403-405 ( PMID 8221882 )
- (în) B. Sollner-Webb , „ Controlul sintezei proteinelor și al degradării ARNm de către microARN. " , Curr. Opin. Cell Biol. , vol. 20,2008, p. 214-221 ( PMID 18329869 )
- (în) D. Shippen-Lentz și EH Blackburn , „ Dovezi funcționale pentru un șablon de ARN în telomerază. » , Știință , vol. 247,1990, p. 546-552 ( PMID 1689074 )
- (în) domnul Huarte , T. Jacks și JL Rinn , „ Un ARN intergenic mare necodificat indus de p53 mediază reprimarea genetică globală în răspunsul p53 ” , Cell , vol. 142,2010, p. 409-419 ( PMID 20673990 )
- (în) EG Wagner și RW Simons , „ Controlul ARN antisens în bacterii, fagi și plasmide. » , Annu. Rev. Microbiol. , vol. 48,1994, p. 713-742 ( PMID 3685996 )
- (ro) E. Heard , „ Progrese recente în inactivarea cromozomilor X. " , Curr. Opin. Cell Biol. , vol. 16,2004, p. 247-255 ( PMID 15145348 )
- (în) A. Fire , S. Xu , domnul Montgomery , S. Kostas S. Driver și C. Mello , „ Interferența genetică puternică și specifică de ARN dublu catenar în Caenorhabditis elegans . » , Natura , vol. 391, 1998, p. 806-811
- Claude Hélène , „ Promisiunile ARN terapeutic = interferența genetică de către ARN. », Le Concours Médical , vol. 124,2002, p. 2550-2552
- (în) R Dahm , „ Friedrich Miescher și descoperirea ADN - ului ” , Dev. Biol. , vol. 278, nr . 22005, p. 274–88 ( PMID 15680349 , DOI 10.1016 / j.ydbio.2004.11.028 )
- (în) T. Caspersson și J. Schultz , " Pentozei nucleotide în citoplasma țesuturilor în creștere " , Nature , vol. 143,1939, p. 602–3 ( DOI 10.1038 / 143602c0 )
- https://www.ulb.ac.be/ibmm/histoire.html
- (în) F. Jacob și J. Monod , „ Mecanisme de reglare genetică în sinteza proteinelor. ” , Journal of Molecular Biology , vol. 3,1961, p. 318–356 ( PMID 13718526 )
- François Jacob , Statuia interioară , Gallimard, col. „Folio” ( nr . 2156)1990, 438 p. ( ISBN 978-2-070-38246-0 și 2-070-38246-X , notificare BnF n o FRBNF35085459 )
- (în) F. Gros , H. Hiatt , W. Gilbert , CG Kurland , RW Risebrough și JD Watson , " Acid ribonucleic instabil dezvăluit prin marcarea pulsată a Escherichia coli " , Nature , vol. 190, 1961, p. 581-585 ( PMID 13708983 )
- (în) A. Claude , „ Constituția protoplasmei ” , Știință , vol. 97, nr . 25251943, p. 451–456 ( PMID 17789864 , DOI 10.1126 / science.97.2525.451 )
- (în) N. Ban , P. Nissen J. Hansen , PB Moore , TA Steitz , „ Structura atomică completă a subunității ribozomale este largă la o rezoluție de 2,4 A. » , Știință , vol. 289, 2000, p. 905-920 ( PMID 10937989 )
- (în) F. Schluenzen , A. Tocilj R. Zarivach , J. Harms , Mr. Gluehmann , D. Janell , A. Bashan , H. Bartels , I. Agmon , F. Franceschi și A. Yonath , " Structura funcțională s-a activat subunitatea ribozomală mică la rezoluția de 3,3 angstromi. ” , Cell , vol. 102, 2000, p. 615–623 ( PMID 11007480 )
- (în) OF Brodersen , „ Structura subunității ribozomale 30S. » , Natura , vol. 407,2000, p. 1143-1154 ( PMID 11014182 )
- (ro) MM Yusupov , GZ Yusupova , A. Baucom , K. Lieberman , TN Earnest , JH Cate și HF Noller , „ Structura cristalină a ribozomului la o rezoluție de 5,5 A. » , Natura , vol. 292,2001, p. 883-896 ( PMID 11283358 )
- Politica extazului, Timothy Leary, 1974, Ed. Fayard, Paris, p. 115-120
- Bhavesh H. Patel, Claudia Percivalle, Dougal J. Ritson, Colm D. Duffy și John D. Sutherland (2015), Origini comune ale precursorilor de ARN, proteine și lipide într-un protometabolism cianosulfidic ; Chimia naturii ( rezumat )
Vezi și tu
Articole similare
- Lista tipurilor de ARN
- Messenger acid ribonucleic
- Ribozom
- Ribozimă
- ARN bicatenar
- microARN
- ARN interferent
- Lista abrevierilor de biologie moleculară și celulară
- fir transcris
- ARN-Seq
- Lista acizilor
linkuri externe
- Lumea ARN la Institutul Fritz Lipman Colecția de linkuri despre „lumea ARN” (structuri, secvențe, instrumente, publicații)
