Piruvat kinaza
Piruvat kinaza este o fosfotransferazei care catalizează reacția :
fosfoenolpiruvat + ADP → ATP + piruvat .Această enzimă este implicată în a 10- a și ultima etapă a glicolizei în direcția reacției de mai sus pentru a cataliza fosforilarea unei molecule de ADP în ATP dintr-o moleculă fosfoenolpiruvat (PEP) convertită în piruvat , folosind un cation de magneziu Mg 2+ ca cofactor .
Acest tip de reacție se numește fosforilare la nivelul substratului . Este posibilă prin variația mare a entalpiei libere standard a hidrolizei grupării fosfat a fosfoenolpiruvatului, aproape de ΔG ° '= - 61,9 kJ · mol -1 . Prin urmare, este ireversibil, deoarece numele său nu indică: kinazele catalizează în mod normal fosforilarea substratului și nu transferul unei grupări fosfat de la substrat la o altă moleculă:

|
+ ADP → ATP + |

|
| PEP | Piruvat |
Izoforme, reglare și gluconeogeneză
Piruvat kinaza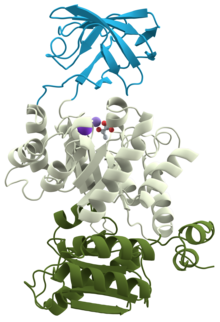 Mușchiul piruvat kinazic al iepurelui complexat cu Mn 2+ , K + și piruvat , prezentând cele trei zone în albastru, alb și verde ( PDB 1PKN )
Mușchiul piruvat kinazic al iepurelui complexat cu Mn 2+ , K + și piruvat , prezentând cele trei zone în albastru, alb și verde ( PDB 1PKN )
| CE nr. | CE |
|---|---|
| numar CAS | |
| Cofactor (i) | Mg 2+ , K + |
| IUBMB | Intrare IUBMB |
|---|---|
| IntEnz | Vizualizare IntEnz |
| BRENDA | Intrarea BRENDA |
| KEGG | Intrare KEGG |
| MetaCyc | Calea metabolică |
| PRIAM | Profil |
| PDB | Structuri |
| MERGE | AmiGO / EGO |
La mamifere , s-au demonstrat trei tipuri principale de piruvat kinaze - izoenzime - care diferă prin modul lor de reglare:
- Piruvat kinaza de tip L ( ficat ), găsită în ficat ; este inhibat alosteric de ATP și alanină și activat de fructoză-1,6-bifosfat ; este reglată prin fosforilare-defosforilare, astfel controlat hormonul folosind proteinkinazei A sub efectul adrenalinei și glucagon , enzima fosforilat este inactivată.
- piruvat kinaza M ( PKM1 și PKM2 ), prezentă în mușchi , care nu este reglementată de fosforilare-defosforilare,
- piruvat kinaza A, prezentă în alte țesuturi, a căror reglare este intermediară și depinde de țesuturi.
O mutatie genetica in aceasta enzima poate provoca deficit de piruvat kinaza , o boala genetica care afecteaza in special metabolismul de celule lipsite de mitocondrii , in care glicolizei este esențială pentru producerea energiei în absența unui ciclu Krebs . Acesta este în special cazul globulelor roșii din sânge , care pot duce la anemie hemolitică .
Piruvat kinaza este, de asemenea, implicată ca enzimă de schimbare pentru gluconeogeneză , o cale metabolică în ficat pentru a produce glucoză din piruvat și din alte substraturi. Atunci când piruvat kinaza este inhibată de fosforilare , de exemplu în timpul postului sub efectul glucagonului , aceasta previne conversia fosfoenolpiruvatului în piruvat și, prin urmare, promovează conversia acestuia în glucoză prin glucagonogeneză.
Relația cu piruvatul fosfat dikinazic
In unele bacterii exista o enzima care îndeplinește o funcție similară, piruvat fosfat dikinază (PPDK), care catalizează reacția :
fosfoenolpiruvat + AMP + PP i P i + ATP + piruvat .Această enzimă, care, spre deosebire de piruvat kinaza, catalizează o reacție reversibilă, este prezentă și în plantele de anaerobe eucariotelor precum Streblomastix (en) , Giardia , Entamoeba și Trichomonas , care probabil dobândit corespunzătoare genei prin transfer. Genic orizontal pe cel puțin două ocazii; unele dintre aceste organisme folosesc atât piruvat kinază, cât și piruvat fosfat dikinazic.
Butoi piruvat kinazic| Pfam | PF00224 |
|---|---|
| Clanul Pfam | CL0151 |
| PROSITATE | PDOC00101 |
| SCOP | 1pkn |
| SUPERFAMILIE | 1pkn |
Note și referințe
- Valorile pentru masa și numărul de resturi indicate aici sunt cele ale precursorului de proteină care rezultă din traducerea a genei , inainte de modificări post-translaționale și pot diferi în mod semnificativ de valorile corespunzătoare pentru proteina funcțională.
- (în) schimbarea energiei gratuite , pe site-ul lui Marc Kirschner (în) , Harvard Medical School .
- (în) Todd Larsen, Timothy L. Laughlin, Hazel M. Holden, Ivan Rayment și George H. Reed , „ Structura iepurei piruvat kinazei musculare complexate cu Mn 2+, K + și piruvat ” , Biochimie , vol. 33, n o 20, Mai 1994, p. 6301-6309 ( PMID 8193145 , DOI 10.1021 / bi00186a033 , citiți online )
- (în) David J. Pocalyko, Lawrence J. Carroll, Brian Martin, Patricia C. Babbitt și Debra Dunaway-Mariano , " Analiza omologiilor de secvență în piruvat de plante și bacterii, fosfat dikinază, enzima I a fosfoenolpiruvatului bacterian: fosfotransferaza zahărului și alte enzime care utilizează PEP. Identificarea potențialelor motive catalitice și de reglementare ” , Biochimie , vol. 29, n ° 48, Decembrie 1990, p. 10757-10765 ( PMID 2176881 , DOI 10.1021 / bi00500a006 , citiți online )

