Boala somnului
Tripanosomiaza africană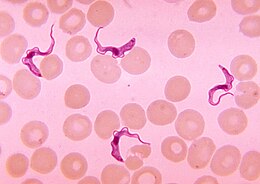 Trypanosoma brucei în sângele unui pacient cu tripanosomioză africană, cunoscută în mod obișnuit ca boală a somnului.
Trypanosoma brucei în sângele unui pacient cu tripanosomioză africană, cunoscută în mod obișnuit ca boală a somnului.
| Specialitate | Boală infecțioasă |
|---|
| ICD - 10 | B56 |
|---|---|
| CIM - 9 | 086.5 |
| BoliDB | 29277 13400 |
| MedlinePlus | 001362 |
| eMedicină | 228613 |
| eMedicină | med / 2140 |
| Plasă | D014353 |
| Incubatie min | 7 zile |
| Incubație maximă | 21 d |
| Simptome | Semn Winterbottom ( en ) , febră periodică ( d ) , cefalee , stare generală de rău , anemie , artralgie , tulburări de somn , amețeli , focalizarea primară a infecției ( d ) , tahicardie , umflături , cașexie și sopor ( en ) |
| Boala transmisă | Transmisie vectorială ( d ) |
| Cauze | Trypanosoma brucei , Trypanosoma gambiense ( d ) și Trypanosoma brucei rhodesiense ( d ) |
| Medicament | (RS) -eflornitină , Nifurtimox , suramină și pentamidină |
| Pacient din Marea Britanie | Afro-tripanosomiaza |
Trypanosomiasis africane , cunoscut sub numele de boala somnului , este o formă de tripanosomiaza , o boala parazitara cauzata de trypanosomes ( protozoar flagelat ), care se transmite prin muscatura de tsetse sau țețe muscă și care afectează animale și oameni. Două subspecii ale unui tripanosom ( Trypanosoma brucei ) generează diferite patologii la om: Trypanosoma brucei ssp. gambiense ( Africa de Vest ) și Trypanosome brucei ssp. rhodensiense ( Africa de Est ).
Boala este endemică în părți din Africa subsahariană , acoperind aproximativ 36 de țări și amenințând 60 de milioane de oameni. Se estimează că între 50.000 și 70.000 de persoane sunt infectate în prezent pe an, numărul acestora scăzând ușor în ultimii ani.
Trei epidemii majore s-au produs în ultima sută de ani, una în 1896 - 1906 (despre care se spune că a ucis aproximativ un milion de oameni în bazinul Congo ) și celelalte două în 1920 și 1970 . Tripanosomiaza bovinelor se numește nagana („a fi deprimat” sau „slăbiciune” în zulu ).
Caracteristici clinice
Pe lângă mușcătura mușcii tsetse, boala poate fi contractată după cum urmează:
- De la mamă la copil: tripanosomul poate traversa bariera placentară și infecta fătul , cu un risc de deces perinatal.
- În laborator: infecții accidentale, de exemplu, în timpul manipulării sângelui unei persoane infectate sau printr-un transplant de organe, deși acest lucru este rar.
- Sexual: a avea relații sexuale neprotejate cu o persoană afectată, dar cazurile dovedite sunt anecdotice.
Simptomele încep cu febră, de obicei intermitentă, dureri de cap și dureri articulare. Un șancru (umflare la punctul de inoculare) este văzut în unul din cinci cazuri în forma rodeziană, dar este excepțional în forma gambiană. Pe măsură ce paraziții intră în organism atât prin sânge, cât și prin sistemul limfatic , ganglionii limfatici se umflă adesea și cresc la dimensiuni enorme. Pot apărea semnul Winterbottom , limfadenopatie cervicală posterioară (ganglioni limfatici în spatele gâtului). Lăsată netratată, boala depășește treptat apărarea persoanei infectate și apar noi simptome, inclusiv anemie , probleme endocrine , cardiace și renale . Boala intră apoi în faza sa de tulburări neurologice atunci când parazitul traversează bariera hematoencefalică . Simptomele acestei a doua faze dau numele bolii; pe lângă confuzia mentală și tulburările de coordonare, ciclul somnului este perturbat, rezultând accese de oboseală care alternează cu perioade de neliniște maniacală care apar în timpul zilei cu somnolență și noaptea cu insomnie . Lăsată netratată, boala este fatală, cu deteriorarea mentală progresivă care duce la comă și moarte. Daunele provocate în faza neurologică pot fi ireversibile.
Durata bolii variază în funcție de parazitul implicat. Evoluția este mai rapidă în cazul Trypanosomia rhodesiense (peste câteva săptămâni până la câteva luni). Poate ajunge la câțiva ani în cazul Trypanosomia gambiense .
Implicarea cardiacă poate fi văzută sub forma gambiană, în esență ca o anomalie a electrocardiogramei fără consecințe. Acest atac rămâne în fundal, spre deosebire de forma americană de tripanosomioză ( boala Chagas ). Forma gambiană poate fi, de asemenea, complet asimptomatică.
Distribuția geografică și epidemiologică
Boala apare în două forme, în funcție de parazitul implicat, Trypanosoma brucei gambiense sau Trypanosoma brucei rhodesiense . TBgambiense se găsește în Africa Centrală și de Vest; provoacă leziuni cronice care pot continua într-o formă pasivă luni sau ani înainte de apariția simptomelor. Rhodesian TB , cauzează o formă acută a bolii , dar produce efecte mult mai limitate. Se găsește în sudul și estul Africii; infecția începe în câteva săptămâni, este mai virulentă și se dezvoltă mai repede. Conform estimărilor recente , Boala somnului este responsabilă pentru pierderea speranței de viață (9-10 ani) pentru 2 milioane de persoane. Evaluări recente Se indică faptul că peste 60 de milioane de persoane din aproximativ 250 de gospodării sunt expuse riscului de a contracta boala și că există în jur de 300.000 de cazuri noi în fiecare an. În 2011, un raport CDC a prezis că, în ritmul încălzirii globale actuale, unele regiuni temperate ar putea deveni zone cu risc de contaminare; dacă în prezent sunt expuse 75 de milioane de persoane, estimează că în 2090, cu 40 până la 77 de milioane mai multe persoane vor fi expuse riscului de transmitere a bolilor.
Boala a fost depistată în 36 de țări, toate din Africa subsahariană . Oamenii sunt rezervorul principal pentru Trypanosoma brucei gambiense , dar alte specii pot fi găsite și la porci și alte animale. Animalele sălbatice și animalele sunt principalul rezervor al tuberculozei rhodesiense .
The tăunii ( Tabanidae ) și Stomoxydinae poate juca , probabil , un rol în transmiterea pasivă (în situații speciale) nu numai pentru Nagana (forma de animale de boala somnului) , ci și a formei umane a bolii.
Ciclul parazit
Mustei tete este mare, maro, și pe furiș. Înțepătura se simte ca un ac fierbinte înfipt în carne. În timpul unei mese de sânge pe mamiferul gazdă, o muscă tsetse infectată (din genul Glossina ) injectează trypomastigote metaciclice în țesutul pielii. Paraziții intră în sistemul limfatic și trec în fluxul sanguin (1). În interiorul gazdei, aceștia se transformă în tripomastigote care circulă în sânge (2) și sunt transportate în alte locații pe tot corpul, ajungând la alte fluide biologice (de exemplu, limfă , lichid cefalorahidian ) și continuă să se replice prin scissiparitate (3). Ciclul parazit al tripanosomului african este reprezentat de etape extracelulare. O muscă tsetse se infectează cu tripomastigote circulante prin luarea unei mese de sânge de la o mamă infectată gazdă (4) (5). În intestinul zbura, paraziții se transformă în tripomastigote prociclice, se înmulțesc prin fissiparitate (6), părăsesc intestinul și se dezvoltă în epimastigote (7). Epimastigotele ajung la glandele salivare ale muștei și continuă să se înmulțească prin fisiune (8). Ciclul în zbor durează aproximativ 3 săptămâni.
Diagnostic de laborator
Diagnosticul se bazează pe dovezi ale tripanosomilor prin examinarea microscopică a lichidului dintr-un șancru, lichid de la o puncție a ganglionilor limfatici , sânge, măduvă osoasă sau, în etapele ulterioare ale infecției, lichid cefalorahidian colectat prin puncție lombară . De tripanosomele mobile sunt căutate pe un preparat umed și în continuare un preparat este fixat și colorate cu metoda Giemsa . Tehnicile de concentrare pot fi utilizate înainte de examinarea microscopică. Pentru probele de sânge, se folosește centrifugarea, pentru alte probe, cum ar fi lichidul cefalorahidian , tehnicile de concentrare includ centrifugarea urmată de examinarea sedimentului. Izolarea parazitului prin inoculare la șobolani sau șoareci este o metodă sensibilă, dar utilizarea sa este limitată la tuberculoză rhodesiense . Detectarea anticorpilor are o sensibilitate și specificitate prea variabile pentru a trage concluzii clinice. În plus, în infecțiile cu tuberculoză rhodesiense , seroconversia are loc după apariția simptomelor clinice și, prin urmare, are un beneficiu limitat.
Trei teste serologice similare sunt disponibile pentru detectarea parazitului gambian: micro-CATT, wb-CATT și wb-LATEX. Primul folosește sânge coagulat, în timp ce ceilalți folosesc probe de sânge integral. Aceste teste constau în reacționarea unei picături de sânge pe un reactiv de pe un card. Sunt ușor de utilizat și constituie un mijloc eficient de screening. Serologia este, pe de altă parte, de puțin folos în formele rodeziene, diagnosticul parazitologic trebuind privilegiat și mai ușor, din cauza unei concentrații mai mari de paraziți.
În formele neurologice, puncția lombară arată, pe lângă parazit, o creștere a nivelului de proteine, precum și prezența celulelor albe din sânge .
Tratament
Tratamentul standard curent pentru prima etapă a bolii este pentamidina intravenos (pentru Tb gambiense ) sau intramuscular, pe parcursul unei săptămâni, principalele efecte secundare fiind hipoglicemia și durerea la locul injectării; urmată de suramină intravenoasă (pentru Tbrhodesiense ) pe o perioadă mai lungă.
Tratamentul standard curent pentru a doua etapă a bolii (faza neurologică) este melarsoprolul intravenos la 2,2 mg / kg pe zi timp de 10 zile consecutive.
Prima linie de terapie alternativă include melarsoprol intravenos 0,6 mg / kg în ziua 1, melarsoprol IV 1,2 mg / kg în ziua 2 și 1,2 / zi IV combinat cu 7,5 mg / kg pe cale orală nifurtimox de două ori pe zi în zilele 3-10 sau eflornitină intravenos 50 mg / kg la fiecare șase ore timp de 14 zile.
În zonele rezistente la melarsoprol sau la pacienții care au recidivat după monoterapie cu melarsoprol, tratamentul trebuie să fie melarsoprol și nifurtimox sau eflornitină.
Următoarele protocoale tradiționale nu ar mai trebui utilizate:
- „Regim” terapeutic vechi de 26 de zile de melarsoprol (3 seturi de 3,6 mg / kg / zi intravenos timp de 3 zile, cu o pauză de șapte zile între seturi) (acest protocol este mai puțin ușor și pacienții sunt mai puțin dispuși să finalizeze tratamentul complet );
- Tratament gradual cu melarsoprol: curs de zece zile de melarsoprol (0,6 mg / kg IV în ziua 1, 1,2 mg / kg IV în ziua 2 și 1,8 mg / kg în zilele 3-10 ). Acest protocol trebuia să reducă riscul de encefalopatie indusă de tratament, dar acum se știe că este asociat cu un risc mai mare de recidivă și o incidență mai mare a encefalopatiei ;
Toți pacienții trebuie urmăriți timp de doi ani cu puncții lombare semestriale pentru a detecta recidivele.
Istoricul tratamentului
În 1910, chiar anul descoperirii lui Bruce, a fost introdus primul medicament activ împotriva bolii somnului, Salvarsan ( arfenamină ), dezvoltat de Paul Ehrlich și Sahachiro Hata . Cu toate acestea, utilizarea acestui derivat din arsenic prezintă riscuri grave, inclusiv orbire . Împreună cu o toxicitate care îl face dificil, eficacitatea Salvarsan încurajează cercetări suplimentare în direcția derivaților de arsenic, iar alte molecule vor fi obținute prin derivarea acidului aminofenolarsinos: tryparsamid (it) și melarsen, acizi arsinici, cu un nucleu de arsenic pentavalent. ; arseno-fenilglicina, melarsen-oxid și melarsoprol, oxizi de acizi arsinici, cu un inel trivalent.
Cu toate acestea, abia în 1919 a fost finalizată lucrarea lui Walter Jacobs și Michael Heidelberger , ceea ce i-a permis lui Wade Brown și Louise Pearce să introducă tryparsamid. De atunci, în timpul anilor 1920 au apărut trei trypanocide , suramin (non- arsenical ), orsanină și tryparsamid, sunt utilizate în campanii vaste de detectare și tratament în masă. Suramin (Bayer 205), sintetizat în 1917, dar a cărui formulă, păstrată secretă, nu a fost elucidată de Ernest Fourneau până în 1924 la Institutul Pasteur , a fost introdusă în 1920. A fost utilizată în prima etapă a bolii. Sau în caz de arseno-rezistență. Administrarea sa pe cale intravenoasă și în doze mari limitează utilizarea acestuia. Cu toate acestea, și în ciuda toxicității sale semnificative, a fost încă în uz în 2001 în faza limfatic-sanguină. Tryparsamide (EA) , derivat din atoxyl este introdus în 1921 și comercializat în 1930 sub numele de Tryponarsil. Este primul medicament activ în faza cefalorahidiană. Cu toate acestea, chiar și redusă cu o doză progresivă, toxicitatea oculară afecteaza 2% dintre pacienții tratați în timpul campaniei conduse de Jean Laigret în Republica Congo la mijlocul anilor 1920, și 4,4% dintre cei tratați cu Eugène Jamot în Camerun. În aceeași epocă. Și la pacienții administrați într-un stadiu avansat, rata de fatalitate iatrogenă este de 6,6%. Orsanina sodică (Fourneau 270) a fost utilizată din 1925 și timp de aproximativ cincisprezece ani, fie singură la pacienții „în perioadă îndoielnică”, fie în combinație cu tryparsamid la pacienții din etapa a doua.
De la începutul anilor 1930, în Congo Belgian , au apărut primele cazuri de arseno-rezistență și, din 1934, tryparsamidul a fost asociat cu alte molecule, inclusiv suramină și orsanină sodică.
Orsanine a fost abandonat odată cu descoperirea, în 1939, de pentamidină , o molecula foarte eficient în prima fază a bolii, utilizate în mod obișnuit în Africa de Vest ca un agent profilactic și care în anii 1950 a redus ratele de infectare. Atât de important ca noi cred că este posibilă eradicarea bolii. Suramin, la rândul său, asociat în general cu tryparsamida, a rămas medicamentul cel mai utilizat în tratamentul bolii somnului până la sfârșitul anilor 1960, înlocuit treptat din 1949 de melarsoprol , dezvoltat de Friedheim. Și care are o toxicitate mai mică decât toate arsenicalele. folosit până atunci.
În cele din urmă, eflornitina (difluorometilornitina sau DFMO), cel mai modern tratament, a fost dezvoltat în anii 1970 de Albert Sjoerdsmanot și a făcut obiectul studiilor clinice în anii 1980. Molecula a fost permisă în Statele Unite de către Food and Drug Administration în 1990, dar Aventis , compania farmaceutică responsabilă de fabricarea sa, a încetat producția în 1999. Cu toate acestea, în 2001, Aventis, în asociere cu Medicii Fără Frontiere și Organizația Mondială a Sănătății , a semnat un acord pe termen lung pentru fabricarea și distribuirea medicamentului. Eficacitatea sa a fost demonstrată, toleranța sa este mai bună decât cea a melarsoprolului. Cu toate acestea, există recidive sub acest tratament, în puțin sub 10% din cazuri, dar cel mai adesea letale. Fexinidazole ar putea fi o alternativă la acest tratament.
Tratamentele combinate ar putea reduce acest risc de recidivă, printre care combinația eflornitină - nifurtimox pare deosebit de promițătoare.
Megazolul, o moleculă biologic activă cu activitate tripanocidă, a făcut obiectul unor studii științifice în urmă cu câțiva ani. Într-adevăr, această moleculă, activă sub formă de pilule (cale orală) elimină 100% din parazit în două zile ( teste in vitro și in vivo la cimpanzei și porci). Această moleculă este totuși suspectată de a fi cancerigenă și dezvoltarea sa a fost oprită.
Perspective și căi de cercetare
Genomul parazitului a fost decodificat și mai multe proteine au fost identificate ca potențiale ținte pentru tratamentul medicamentos. Decodarea ADN-ului a arătat, de asemenea, de ce a fost atât de dificilă producerea unui vaccin pentru această boală. T brucei are peste 800 de gene care produc proteine pe care le folosește pentru a evita detectarea de către sistemul imunitar. (Berriman, și colab. , 2005)
O echipă internațională de cercetare care lucrează în Republica Democrată Congo , Sudan și Angola, implicând Immtech International și Universitatea din Carolina de Nord din Chapel Hill, a efectuat studiile clinice de fază I și a început un studiu de fază III în 2005 pentru a testa eficacitatea primelor tratament oral pentru boala somnului, cunoscut în prezent ca „DB289”.
Rezultatele recente indică faptul că parazitul nu poate supraviețui în fluxul sanguin fără flagelul său . Această descoperire oferă cercetătorilor un nou unghi de atac pentru a elimina parazitul.
Cercetătorii au descoperit un mecanism imun pe care cred că îl folosesc pentru a crea noi tratamente. O proteină Hpr ( proteină legată de haptoglobină ) descoperită în 2006 și legată de lipidele din sistemul sanguin poate capta hemoglobina și o poate transporta către corpul gras de care sunt legate, care conține o toxină fatală pentru tripanosom. Acest mecanism ar putea fi o soluție imună folosind dependența tripanosomilor de hemoglobină. Când aceasta din urmă a fost capturată anterior de o proteină Hpr, tripanosomii se atașează și ei de particula grasă care apoi otrăvește parazitul.
Prevenire și control
Nu există vaccin sau prevenire a medicamentelor. Prevenirea și controlul se concentrează, acolo unde este posibil, pe extirparea gazdei parazite, musca tsetse . Două strategii au fost utilizate alternativ în încercările de a reduce tripanosomiaza africană. Una dintre tactici este în primul rând medicală sau veterinară și vizează direct boala folosind profilaxie, tratament și supraveghere pentru a reduce numărul de organisme purtătoare de boli. A doua strategie este în general entomologică și implică întreruperea ciclului de transmisie prin reducerea numărului de muște.
Există exemple de reducere a bolii somnului prin utilizarea tehnicilor de sterilizare a insectelor. Supravegherea activă regulată, care implică detectarea și tratarea cazurilor, în plus față de controlul zbura tsetse, este coloana vertebrală a strategiei de control al bolii somnului. Screeningul sistematic în comunitățile în care au fost identificate focare este cea mai bună abordare, deoarece screeningul de la caz la caz nu este practic posibil în zonele extrem de endemice. Screeningul sistematic poate lua forma unor clinici mobile sau a unor centre fixe de screening în care echipele se deplasează zilnic la case. Natura bolii Gambiense este de așa natură încât pacienții nu solicită tratament suficient de devreme deoarece simptomele din această etapă nu sunt evidente sau suficient de grave pentru a justifica un consult medical, datorită îndepărtării celor câteva zone afectate. În plus, diagnosticul bolii este dificil și majoritatea lucrătorilor din domeniul sănătății nu sunt în măsură să o detecteze. Screeningul sistematic permite detectarea și tratarea precoce a bolii înainte ca boala să progreseze și scade rezervorul uman.
Pentru călător, este recomandată purtarea îmbrăcămintei de acoperire, precum și a substanțelor impermeabile împotriva mustei responsabile.
Istorie și epidemiologie
În Africa, prezența bolii somnului este atestată încă din secolul al XIV- lea .
Cu toate acestea , nu a fost până la începutul XX - lea secol , în 1901 și 1903 , că Sir David Bruce descoperă și confirmă Agentul parazit al acestei boli, la care a dat numele său: Bruce tripanoso- ( Trypanosoma brucei ), și în 1910 că el și-a identificat cu precizie vectorul de insecte, musca Glossina palpalis
Au existat trei epidemii grave în Africa în secolul trecut. Primul, între 1896 și 1906, a afectat în principal Uganda și bazinul Congo .
O epidemie majoră are loc după începerea colonizării în trecere XX - lea secol, probabil , omorând aproximativ un milion de oameni din bazinul Congo , contribuind la depopuleze țării din bazinul african; în plus, este probabil ca mișcările crescute și adesea forțate din acest bazin, promiscuitatea dintre copiii adunați în școli, între purtătorii din triburi și medii diferite (voluntari sau recrutați cu forța, dacă doreau să-și găsească soțiile ținute în lagărele de detenție de francezi autoritate , tabere în care condițiile de viață foarte dificile au dus și la scăderea imunității și a epidemiilor). O asistență medicală nativ și unitățile sanitare mobile sunt stabilite de administrația colonială la toate coloniile sale, inclusiv Maroc și Algeria, Africa de Vest franceză , inclusiv Camerun, incredintate rapid la medici militari .
O a doua epidemie a luat naștere din 1920 în mai multe țări africane. Este oprit de echipele mobile care examinează sistematic milioane de oameni aflați în pericol. Boala fiind aproape dispărută între 1960 și 1965, detectarea și supravegherea s-au încetinit după plecarea autorităților coloniale și, în 1970, a izbucnit a treia epidemie majoră.
De atunci, boala a continuat să progreseze sub formă endemică în mai multe focare.
Variat
Din 1951 până în 1953 , în timp ce s-au făcut progrese semnificative în farmacologie și în cunoașterea psihozelor , profesorul Pierre Gallais, șeful departamentului de psihiatrie al spitalului Lévy din Marsilia , a experimentat o metodă terapeutică inspirată de malariaterapie , pe care el o numește trypanoterapie, face farmacologie testează direct la 12 pacienți timp de doi ani, estimând că "faza nervoasă a bolii ar putea fi un moment salutar pentru pacienții psihotici și schizofrenici, în eșec terapeutic , găzduiți în serviciul său"
Molecula secretată de parazitul responsabil de repercusiunile simptomatice asupra stării de veghe este triptofolul .
Note și referințe
- Medici militari documentari în timpul coloniilor , Arté France, 2011, în regia lui Farnçois Caillat și Silvia Radelli.
- Științe Futura [1]
- (în) G. Rocha , A. Martins , G. Gama , F. Brandão și J. Atouguia , " Posibile cazuri de transmitere sexuală și congenitală a bolii somnului " , Lancet , Vol. 363,17 ianuarie 2004, p. 247 ( PMID 14738812 , citiți online [PDF] )
- (en) R. Brun, J. Blum J, F. Chappuis și C. Burri, " Tripanosomiaza africană umană " , Lancet , vol. 375,2010, p. 148-159 ( citește online )
- Odiit M, Kansiime F, Enyaru JC, Durata simptomelor și fatalitatea cazurilor de boală a somnului cauzate de Trypanosoma brucei rhodesiense în Tororo, Uganda , East Afr Med J, 1997; 74: 792-795
- Checchi F, Filipe JA, Haydon DT, Chandramohan D, Chappuis F, Estimări ale duratei etapei timpurii și târzii a bolii somnului gambiense , BMC Infect Dis, 2008; 8:16
- Blum JA, Zellweger MZ, Burri C, Hatz C, implicare cardiacă în tripanosomiaza africană și americană , Lancet Infect Dis, 2008; 8: 631-641.
- Date și statistici OMS privind mortalitatea și sănătatea , accesat la 10 februarie 2009.
- (în) Organizația Mondială a Sănătății (Geneva) , World Report Sanatatii 2000: Sisteme de sănătate Îmbunătățirea performanței ,2000( citește online )
- (în) Comitetul de experți al OMS pentru controlul și supravegherea tripanosomiazei africane (Geneva) , seria de rapoarte tehnice a OMS, nr.881 ,1998( citește online )
- (în) Sean Moore, Surya Shrestha, Kyle W. Tomlinson și Holly Vuong, Prezicerea efectului schimbărilor climatice asupra tripanosomiazei africane: Integrarea epidemiologiei cu paraziți și biologia vectorială . Citeste online
- (în) T. Cherenet , RA Sani , JM Panandam S. Nadzr N. Speybroeck și Pé van den Bossche , „ Prevalența sezonieră a tripanosomozei bovine într-o zonă infestată de tsetse și o zonă fără tsetse din regiunea Amhara, nord- vestul Etiopiei ” , Revista Onderstepoort de cercetare veterinară , vol. 71, nr . 4,2004, p. 307–312 ( citește online )
- Lutumba P, Robays J, Miaka C și Als. Eficiența diferitelor strategii de detectare a tripanosomiozei africane umane în T. b. gambiense , Trop Med Int Health, 2005; 10: 347-356
- (în) C. Burri , S. Nkunku , A. Merolle și colab. , „ Eficacitatea unui program nou și concis pentru melarsoprol în tratamentul bolii de somn cauzate de Trypanosoma brucei gambiense: un studiu randomizat ” , Lancet , vol. 355, nr . 9213,2000, p. 1419–25 ( PMID 10791526 )
- (en) Sylvie Bisser , François-Xavier N'Siesi , Veerle Lejon și colab. , „ Procesul de echivalență al monoterapiei cu Melarsoprol și Nifurtimox și terapia combinată pentru tratamentul Trypanosoma brucei gambiense în stadiul al doilea Boala de somn ” , Jurnalul bolilor infecțioase , vol. 195,2007, p. 322–29 ( citește online ).
- (ro) S. van Nieuwenhove , PJ Schechter , J. Declercq și colab. , „ Tratamentul bolii somnului gambiense în Sudan cu DFMO oral (DL-alfa-difluorometil ornitină) un inhibitor al ornitinei decarboxilazei: primul studiu de teren ” , Trans R Soc Trop Med Hyg , vol. 79, nr . 5,1985, p. 692–8.
- (en) J. Pepin și B. Mpia , „ Studiu controlat randomizat a trei regimuri de melarsoprol în tratamentul Trypanosoma brucei gambiense trypanosomiasis ” , Trans R Soc Trop Med Hyg , vol. 100,2006, p. 437-41.
- La 19 aprilie 1910, la Congresul de medicină internă din Wiesbaden , Ehrlich și Hata raportează despre descoperirea arfenaminei și rezultatele încurajatoare ale primelor studii clinice.
- „Chimioterapia infecțiilor cu tripanosom și spirochete. Chemistry of N-Phenylglycineamide-p-Arsonic Acid ”, Journal of Experimental Medicine , vol. 30, n ° 5, 1 st luna noiembrie 1919 p. 411 ; L. Pearce și WH Brown, „Acțiunea terapeutică în tripanosomiaza experimentală a șoarecilor, șobolanilor și cobaiilor”, ibid. , p. 437 ; „Acțiune toxică”, ibid. , p. 417 ; „Acțiune terapeutică în tripanosomiaza experimentală a iepurilor”, ibid. , p. 455 ; „Acțiune asupra infecțiilor cu spirochete”, ibid. , p. 483 .
- H. Jonchère "Chimioprofilaxia tripanosomiozei umane în AOF", în Buletinul Societății de Patologie Exotică , 44 (1951), 83-93.
- S. Abbatucci, „Cu privire la tratamentul bolii somnului cu tryparsamid”, în Bulletin de la Société de pathologie exotique , 19 (1926), 271-279.
- Ernest Fourneau , „ Despre utilizarea acidului oxiaminofenilarsinic și a acizilor arilarsinici în general în tratamentul spirilozei și al tripanosomiazei ”, Annales de Institut Pasteur , vol. 35,1921, p. 571-574.
- Ernest Fourneau , Jacques și Thérèse Tréfouël și Yvonne de Lestrange-Trévise , „ Derivați ai acidului fenilarsenic (ca pentavalent) în tratamentul tripanosomiazei. II ”, Ann. Inst. Pastor , vol. 40,1926, p. 933.
- Ernest Fourneau , Jacques și Thérèse Tréfouël și Germaine Benoit , " Pe izomerii para-oxi-3-amino-fenil-arsinic acidului și derivatul său acetil ( stovarsol ) ", Buletin de la Societe Chimique de France , 4 th serie, vol. 41,1927, p. 499-514.
- J. Dutertre și R. Labusquière, "Terapia tripanosomiazei", în Medicina tropicală , 26 (1966), 342-356.
- J. Burke, "Istoria luptei împotriva bolii somnului în Congo", în Annales de la Société belge de medicine tropique , 51 (1971), 465-477.
- EAHFriedheim, „Mel B în tratamentul tripanosomiazei umane”, Am. J. Trop. Med. Hyg. , 29 (1949) 173-180.
-
J. Hardenberg, N. Claverie GP Tell, "Tratamentul cu eflornitină (Ornidyl) al bolii somnului Trypanosoma brucei gambiense: raportul a 711 pacienți tratați până în martie 1991", a 21- a reuniune a Consiliului științific internațional pentru cercetare și lupta împotriva tripanosomozelor (CSILRT), Yamoussoukro, Côte d'Ivoire , 1991;
FJ Louis, J. Keizer, PP Simarro, C. Schmid, J. Jannin, „Eflornitină în tratamentul bolilor de somn”, Med. Prea mult. , 63 (2003), 559-563. - Priotto G., Pinoges L., Fursa IB și colab., „Siguranța și eficacitatea eflornitinei de primă linie pentru Trypanosoma brucei gambiense boala somnului în Sudan: studiu de cohortă” , BMJ , 2008, 336 , 705-708.
- Kande Betu Ku Mesu V, Mutombo Kalonji W, Bardonneau C și colab. Fexinidazol oral pentru Trypanosoma brucei gambiense trypanosomiasis african în stadiu târziu: un studiu pivot multicentric, randomizat, de non-inferioritate , Lancet, 2018; 391: 144–154
- Priotto G., Kasparian S., Ngouama D. și colab., „Terapia combinată Nifurtimox-eflornitină pentru boala somnului Trypanosoma brucei gambiense în etapa a doua: un studiu clinic randomizat în Congo” , Clin. Infecta. Spune. , 2007, 45 , 1435-42.
- Gérard Chauvière, Bernard Bouteille, Bertin Enanga, Cristina de Albuquerque, Simon L. Croft, Michel Dumas, Jacques Périe, Journal of medicinal chemistry , vol. 46, n o 3, 2003, p. 427-440 .
- (în) David Williamson , „ Compusul ar putea învinge boala de somn din Africa, studiu clinic începând cu această lună ” , Universitatea din Carolina de Nord Serviciul de Știri ,25 august 2005( citește online )
- (în) personal , „ Actualizare studii clinice ” , Știri despre inginerie genetică ,15 septembrie 2005, p. 5
- " Descoperirea africană a bolii de dormit " (accesat la 7 aprilie 2006 )
- echipa de la Aarhus University și Université Libre de Bruxelles, studiu publicat în revista Science la mijlocul anului 2008
- B. Vanhollebeke și colab., „ Un receptor de haptoglobină-hemoglobină transmite imunitate înnăscută la Trypanosoma brucei la om ”, Știință , vol. 320,2008( rezumat )
- " Direcția strategică pentru țările din Africa Trypanosomiasis de cercetare " ( Arhiva • Wikiwix • archive.is • Google • Ce să fac? ) , Programul special de cercetare si formare in tropicala Boli (accesat la 1 st martie 2006 )
-
D. Bruce, „Notă despre descoperirea unui nou tripanosom”, Proceedings of the Royal Physical Society of Edinburgh , IXIX, 1902, p. 496 ;
„ Etiologia bolii de somn (cu farfurie specială). Trypanosome and its insect carrier ”, raport al prelegerii susținute de colonelul D. Bruce către Liverpool Biological Society despre boala somnului în Uganda, British Medical Journal , 21 noiembrie 1903, p. 1343-1350 . - D. Bruce, AE Hamerton, HR Bateman, FP Mackie, „ The natural food of Glossina palpalis ”, Proceedings of the Royal Society of London, Seria B (publicații biologice), 15 iunie 1910.
- Vassal J. (1923). Prezentare generală a asistenței medicale indigene în Africa . Rev. med. Angola, 1, 205-206.
- Chatinières P (1919) În Marele Atlas marocan: extrase din jurnalul unui medic autohton de asistență medicală 1912-1916 . Plon-Hrănește.
- Cilleuls, JD (1959). Participarea medicilor din grupurile mobile de sănătate la asistența medicală indigenă și la cucerirea Marocului. Istorie medicală, 9, 5-39.
- Raynaud L, Soulié H & Picard P (1932) Igiena și patologia nord-africană: Asistență medicală pentru europeni în Algeria, de P. Picard . Asistență medicală pentru nativii din Algeria, de H. Soulié. Considerații generale privind organizarea și funcționarea serviciilor de asistență și igienă ale coloniei , de H. Soulié, L. Raynaud, P. Picard (Vol. 2). Masson.
- Heckenroth F. (1923). Activitatea asistenței medicale indigene în Africa de Vest franceză. Rev. med. Angola, 1, 207-219
- (în) Centrul media al OMS , Fișa informativă nr . 259: tripanosomiaza africană sau boala somnului ,2001( citește online )
- http://www.chs-savoie.fr/france/MENU5/news/index.html/quand-1317420000 vedea , de asemenea: Suveniri (JDTR)
- Blanc F (2012) Trypanoterapie, contribuție la istoria psihiatriei biologice ; PSN 2012/1 (Volumul 10); Ediții materiale ; ( ISBN 9782919694150 ) p. 77 - 94.
- (ro) EM Cornford, WD Bocash, Braun LD, PD Crane, WH și Oldendorf MacInnis AJ. „Distribuția rapidă a triptofolului (3-indol etanol) către creier și alte țesuturi” J Clin Invest. 1979; 63 (6): 1241-8.
Anexe
Bibliografie
- Gaëlle Ollivier și Dominique Legros , „ History of human African tripanosomiasis ”, Tropical Medecine International Health , vol. 6, n o 11,Noiembrie 2001, p. 855-863 ( citește online )
- ( fr ) MP Barrett și colab. , " Tripanosomiasele " , Lancet , vol. 362, nr . 9394,1 st noiembrie 2003, p. 1469-80 ( PMID 14602444 , citiți online )
- (ro) M. Berriman și colab. , „ Genomul tripanosomului african Trypanosoma brucei ” , Știința , vol. 309, nr . 5733,2005, p. 416–22 ( PMID 16020726 , citiți online )
Articole similare
- Zbura tsetse
- Lista bolilor infecțioase
- Boala Chagas , o altă boală umană cauzată de Trypanosome
- DNDi (Inițiativa privind drogurile pentru bolile neglijate)
- Epidemie de boală a somnului în bazinul Congo
linkuri externe
- Medici fără frontiere / Medici fără frontiere Pagina de informații despre boala somnului
- Institutul de Cercetare pentru Dezvoltare
- Ultima actualizare a OMS „Tripanosomiaza africană (boala somnului)” Martie 2014, http://www.who.int/mediacentre/factsheets/fs259/fr/