Acid lactic
| Acid lactic | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
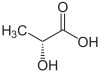
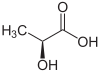
| Enantiomerul R al acidului lactic (sus, stânga), acid S-lactic (sus, dreapta) și structura tridimensională a acidului S-lactic (jos). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificare | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Numele IUPAC | Acid 2-hidroxipropanoic | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS |
(RS) (S+ sau L) (R- sau D) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.000.017 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 200-018-0 209-954-4 ( RS ) 201-196-2 ( S ) 233-713-2 ( R ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Codul ATC | G01 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E270 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 2611 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ZÂMBETE |
CC (O) C (= O) O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = InChI = 1 / C3H6O3 / c1-2 (4) 3 (5) 6 / h2,4H, 1H3, (H, 5,6) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspect | lichid vâscos incolor până la galben sau cristale incolore până la galben (DL) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietăți chimice | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formulă |
C 3 H 6 O 3 [Izomeri] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masă molară | 90,0779 ± 0,0037 g / mol C 40%, H 6,71%, O 53,29%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| pKa | 3,86 ( 20 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietăți fizice | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fuziune |
D / L : 16,8 ° C L : 53 ° C D : 53 ° C |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fierbere | 122 ° C ( 12 mmHg ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilitate | usor macinat. în eter ; insol. în cloroform , eter de petrol , disulfură de carbon |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscibilitate | miscibil cu apă , alcool , glicerol și furfuraldehidă , un sol. alcool-eter | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa volumică | 1,248 5 g cm −3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punct de aprindere | 110 ° C (cupă închisă) (DL) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochimie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
ecuaţie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietati optice | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Indicele de refracție | 1,4414 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Puterea rotativă |
−2,6 ° ( 80 g l −1 , R) + 2,6 ° ( 25 g l −1 , S) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauții | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Acid lactic: Produs neclasificatClasificarea acestui produs nu a fost încă validată de divulgarea serviciului directorului toxicologic la 1,0%, conform listei de divulgare a ingredientelor. Acid lactic, (dl-): E,  E : Material corosiv acid puternic (pH calculat = 1,9 pentru o soluție de 9%) Dezvăluire la 1,0% conform listei de divulgare a ingredientelor |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Directiva 67/548 / CEE | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Xi Simboluri : Xi : Iritant Fraze R : R38 : Iritant pentru piele. R41 : Risc de leziuni oculare grave. Fraze S : S26 : În caz de contact cu ochii, clătiți imediat cu multă apă și solicitați sfatul medicului. S39 : Purtați protecție pentru ochi / față. Expresii R : 38, 41, Fraze S : 26, 39, |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Compuși înrudiți | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izomer (i) | Acid 3-hidroxipropanoic | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unități de SI și STP, cu excepția cazului în care se prevede altfel. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Acidul lactic este un acid organic , care joacă un rol în diferite procese biochimice . Lactatul este baza conjugată a acestui acid (adică, forma ionizată de acid lactic). Contrar a ceea ce ar putea sugera numele său, acidul lactic nu este prezent doar în laptele din care a fost extras pentru prima dată de chimistul suedez Carl Wilhelm Scheele . Se mai găsește în vin , în anumite fructe și legume , în celulele animale unde este disociată și prezentă sub formă de lactat precum și în anumite preparate ( varză acră etc.).
Acidul lactic este un acid α hidroxi , ei formula brută este C 3 H 6 O 3 iar structura sa se reflectă în denumirea sa sistematică, acidul 2-hidroxipropanoic.
Chimie
Atomului de carbon 2 care poartă grupa hidroxi este asimetrici face molecula de acid lactic chiral . Prin urmare, este sub forma a doi enantiomeri :
- Acid ( R ) -lactic sau D (-) - acid lactic;
- Acid ( S ) -lactic sau L (+) - acid lactic.
În soluție , grupa carboxil -COOH poate pierde un ion H + . Astfel acidul lactic (C 3 H 6 O 3 ) este transformat în ion lactat : CH 3 CHOHCOO -.
Pe de altă parte, în mușchi, doi ioni H + sunt adăugați la piruvat (C 3 H 3 O 3 ) pentru a forma lactat (C 3 H 5 O 3 2+ ) .
Acidul lactic este solubil în apă și considerat a fi un acid slab ( pKa = 3,90), adică reacția de disociere în apă nu este completă:
CH 3 CHOHCOOH+ H 2 O⇄ CH 3 CHOHCOO -+ H 3 O +Prin urmare, acidul lactic se găsește atât în soluție, cât și în forma sa bazică, ionul lactat, în proporții variabile în funcție de pH .
Efort muscular și fermentație lactică
Acidul lactic este unul dintre produsele cheie în producția de energie în special a mușchilor. Respirația celulară (consumul de zaharuri pentru a produce energie) poate fi descompusă în două etape principale, prima este glicoliza , partea citoplasmatică a procesului, care are loc în absența oxigenului. Furnizează piruvat, care furnizează a doua parte mitocondrială a respirației celulare ( ciclul Krebs și fosforilarea oxidativă), ceea ce duce la reducerea oxigenului din apă. La un capăt al lanțului, glucoza este oxidată, iar la cealaltă, oxigenul este redus. Energia eliberată este recuperată de celulă.
Dacă aportul de oxigen este mai mare decât consumul de zahăr, atunci tot acidul piruvic produs este consumat imediat în partea mitocondrială.
Dacă consumul de zahăr devine mai mare decât aportul de oxigen (eforturi intense), atunci o parte din acidul piruvic produs în prima parte a procesului se reduce la acid lactic, ceea ce permite ciclului oxidativ al glicolizei să continue. Este o fermentație . Partea mitocondrială este saturată și randamentul energetic este mult redus. Cu toate acestea, această teorie a consumului de zahăr / a consumului de oxigen este pusă în discuție. În ceea ce privește randamentul energetic anaerob, acesta pare proporțional mai mare decât randamentul energetic aerob, contrar a ceea ce este general acceptat.
Lactatul trece prin membrana celulară pentru a pătrunde în sânge. Ficatul , mușchii scheletici, inima si creierul poate folosi acest substrat pentru energie. Ficatul îl reciclează în ceea ce se numește gluconeogeneză, care va resinteza glucoza, în timp ce o altă parte este oxidată de miocard, precum și de mușchii mai puțin solicitați de efortul sportiv. Lactatul este metabolizat la aproximativ o oră după exercițiu, fără nicio activitate sportivă post-exercițiu, adică cu mult înainte de apariția rigidității musculare , pentru care, prin urmare, nu este responsabil.
Fermentarea bacteriană
Există două tipuri principale de fermentație bacteriană care produc acid lactic: în vin și produse lactate.
- În vin , aceasta este fermentația malolactică : acidul malic, conținut în mod natural în vin, este descompus în acid lactic sub acțiunea bacteriilor.
- În lapte și produse lactate, acidul lactic provine din descompunerea lactozei de către bacterii. Cu cât laptele este mai proaspăt, cu atât conține mai puțin acid lactic. Concentrația de acid lactic în lapte este exprimată în grad dornic (° D): 1 ° D corespunde la 0,1 g de acid lactic pe litru de lapte. Un lapte proaspăt conține de la de 15 până la 18 ani ° D , este prepelița la 60 la - 70 la ° D .
Organismele responsabile de apariția acidului lactic sunt lactobacilii . Când acționează în gură, acidul lactic produs poate duce la cavități .
Această metodă de fermentare lactică apare și pe anumite legume ( varză = varză murată și alte așa-numite legume „lacto-fermentate”). Acidul lactic folosit ca AHA în produsele cosmetice nu este extras din lapte dar, de exemplu, zahar din sfecla , afine , etc.
Utilizări
Sursă.
Direct în hrana umană
Acidul lactic este utilizat în industria alimentară ca aditiv (E270) ca antioxidant , acidifiant sau intensificator de aromă . Acidul lactic este prezent și sub formă de săruri: sare de sodiu ( E325 ), potasiu ( E326 ) și calciu ( E327 ). Aceste săruri sunt sub formă de pulbere și sunt, de asemenea, solubile în apă. Acționează ca agent bacteriostatic , în special asupra bacteriilor patogene, cum ar fi salmonella (sau listeria ) și, de asemenea, un efect depresiv asupra activității apei .
Potrivit cercetărilor care au avut loc în Quebec, s-ar părea că acidul lactic este unul dintre cele mai naturale mijloace de prevenire a cancerului de vezică , dar și cel al pielii .
În cosmetică
Acest acid este uneori utilizat ca parte a unei coji estetice, în special pentru pielea colorată (gamele de produse de decolorare estetică sunt compuse din acid lactic); cu toate acestea, acest acid trebuie aplicat sub supravegherea unui dermatolog și în condiții de dozare și diluare specifică în funcție de tipul de tonus al pielii pacientului.
Ca agent de decontaminare și detergent
Acidul lactic a câștigat importanță în industria detergenților după anii 2000. Este un bun detartrat , detergent de săpun și agent antibacterian. De asemenea, este avantajos din punct de vedere economic și face parte dintr-o tendință către ingrediente mai sigure și mai naturale pentru mediu. Prin urmare, acidul lactic este utilizat în Statele Unite pentru decontaminarea bacteriană a carcaselor de bovine în abatoare . De carne de vită care face obiectul acestei practici la început interzise de Uniunea Europeană , deoarece utilizarea de acid lactic este aici pentru a corecta o lipsă de igienă legate de practicile de logare laxe. Ca parte a compromisului privind importul de carne de vită nord-americană în Europa în urma embargoului cu carne de vită hormonală , această utilizare a fost în cele din urmă autorizată după publicarea regulamentului european 101/2013 de la început.februarie 2013. În Europa, această practică este, în principiu, trasabilă.
Precursor din plastic
Acidul lactic este polimerizat pentru a da acid polilactic (PLA), un material plastic biodegradabil utilizat în special pentru imprimante 3D , pentru ambalarea alimentelor și în chirurgie .
Istoric
Acidul lactic a fost descoperit de Carl Wilhelm Scheele (1742-1786).
Comerț
Franța, în 2014, este un importator net de acid lactic, conform obiceiurilor franceze. Prețul mediu de import pe tonă a fost de 1.400 EUR.
Note și referințe
- ACID LACTIC, fișă (e) de siguranță a Programului internațional de siguranță chimică , consultată la 9 mai 2009
- " Număr de înregistrare CAS: 50-21-5 " , la ntp.niehs.nih.gov (accesat la 14 februarie 2010 )
- calculate în masă moleculară de „ masele atomice ale elementelor 2007 “ pe www.chem.qmul.ac.uk .
- (ro) JG Speight și Norbert Adolph Lange, Lange's Handbook of Chemistry , New York, McGraw-Hill ,2005, Ediția a 16- a . , 1623 p. ( ISBN 978-0-07-143220-7 , LCCN 84643191 ) , p. 2.289
- (în) Carl L. Yaws, Manual de diagrame termodinamice , vol. 1, Huston, Texas, Gulf Pub. Co,1996( ISBN 978-0-88415-857-8 , LCCN 96036328 )
- (ro) Maryadele J. O'Neil, Ann Smith, Patricia E. Heckelman și Susan Budavari, The Merck Index: An Encyclopedia of Chemicals, Drugs and Biologicals , Statele Unite ale Americii, Merck,2001, Ed. A 13- a . , 2564 p. ( ISBN 978-0-911910-13-1 )
- „ Acid lactic ” în baza de date cu produse chimice Reptox a CSST (organizația din Quebec responsabilă de securitatea și sănătatea în muncă), accesată la 24 aprilie 2009
- „ Acid lactic, (dl-) ” în baza de date cu produse chimice Reptox a CSST (organizația din Quebec responsabilă de securitatea și sănătatea în muncă), accesată la 25 aprilie 2009
- „ Acid lactic ” , pe societechimiquedefrance.fr (accesat la 18 septembrie 2019 )
- (în) George A. Brooks , " The Science and Translation of Lactate Shuttle Theory " , Cell Metabolism , Vol. 27, nr . 4,aprilie 2018, p. 757–785 ( ISSN 1550-4131 , DOI 10.1016 / j.cmet.2018.03.008 , citit online , accesat la 30 mai 2018 )
- Luc Léger , Georges Cazorla , Cyril Petibois și Laurent Bosquet , „ Lactat și exercițiu: mituri și realități ”, Staps , vol. Nr. 54, nr . 1,2001, p. 63–76 ( ISSN 0247-106X , DOI 10.3917 / sta.054.0063 , citit online , accesat la 30 mai 2018 )
- Pascal Prevost, „ Courbatures ” , pe Sciensport ,2006(accesat la 8 ianuarie 2008 )
- UN Wiesmann , S. DiDonato și NN Herschkowitz , „ Efectul clorochinei asupra fibroblastelor cultivate: eliberarea hidrolazelor lizozomale și inhibarea absorbției lor ”, Comunicări de cercetare biochimică și biofizică , vol. 66, nr . 4,27 octombrie 1975, p. 1338-1343 ( ISSN 1090-2104 , PMID 4 , citite online , accesat 1 st aprilie 2018 )
- C. Chêne (2002), Acizi organici [PDF] , Centrul de resurse tehnologice pentru întreprinderile agroalimentare, http://www.adrianor.com .
- http://sante.canoe.com/channel_health_news_details.asp?channel_id=2001&relation_id=3483&news_channel_id=2001&news_id=3695
- Întrebări și răspunsuri în Senat
- „ Indicator al comerțului de import / export ” , la Direcția Generală Vamă. Indicați NC8 = 29181100 (accesat la 7 august 2015 )
Vezi și tu
Articole similare
- Aditiv alimentar
- Aromă
- Lapte și vin
- Acid polilactic , polimer biodegradabil
linkuri externe
- [video] „Molecular Mojito - Molecular Cocktail - Molecular Cuisine - Molecular Gastronomy” pe YouTube ,15 noiembrie 2016.
Bibliografie
- Ackerman SH și Sachar EJ (1974), The lactate theory of anxious: a review and reevaluation , Psychosom. Med. , Ianuarie-februarie 1974, 36 (1), 69-81.





