Acetil-coenzima A
| Acetil-coenzima A | |
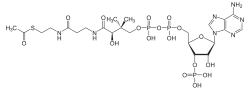  Structura acetil-coenzimei A |
|
| Identificare | |
|---|---|
| N o CAS | |
| N o ECHA | 100.000.719 |
| N o EC | 200-790-9 |
| PubChem | 444493 |
| ChEBI | 15351 |
| ZÂMBETE |
CC (= O) SCCNC (= O) CCNC (= O) C (C (C) (C) COP (= O) (O) OP (= O) (O) OCC1C (C (C (O1) N2C = NC3 = C2N = CN = C3N) O) OP (= O) (O) O) O , |
| InChI |
InChI: InChI = 1 / C23H38N7O17P3S / c1-12 (31) 51-7-6-25-14 (32) 4-5-26-21 (35) 18 (34) 23 (2,3) 9- 44-50 (41.42) 47-49 (39.40) 43-8-13-17 (46-48 (36.37) 38) 16 (33) 22 (45-13) 30-11-29- 15-19 (24) 27-10-28-20 (15) 30 / h 10-11,13,16-18,22,33-34H, 4-9H2,1-3H3, (H, 25,32) (H, 26,35) (H, 39,40) (H, 41,42) (H2,24,27,28) (H2,36,37,38) / t13-, 16-, 17-, 18 +, 22- / m1 / s1 / f / h25-26,36-37 , 39,41H, 24H2 InChIKey: ZSLZBFCDCINBPY-XZFIVJFQDF Std. InChI: InChI = 1S / C23H38N7O17P3S / c1-12 (31) 51-7-6-25-14 (32) 4-5-26-21 (35) 18 (34) 23 (2,3) 9- 44-50 (41.42) 47-49 (39.40) 43-8-13-17 (46-48 (36.37) 38) 16 (33) 22 (45-13) 30-11-29- 15-19 (24) 27-10-28-20 (15) 30 / h 10-11,13,16-18,22,33-34H, 4-9H2,1-3H3, (H, 25,32) (H, 26,35) (H, 39,40) (H, 41,42) (H2,24,27,28) (H2,36,37,38) / t13-, 16-, 17-, 18 +, 22- / m1 / s1 Std. InChIKey: ZSLZBFCDCINBPY-ZSJPKINUSA-N |
| Proprietăți chimice | |
| Formula brută |
C 23 H 38 N 7 O 17 P 3 S [Izomeri] |
| Masă molară | 809,571 ± 0,033 g / mol C 34,12%, H 4,73%, N 12,11%, O 33,6%, P 11,48%, S 3,96%, |
| Unități de SI și STP, cu excepția cazului în care se prevede altfel. | |
Acetil-coenzima A , de obicei scrise acetil-CoA , este forma „activat“ de acid acetic , adică cu alte cuvinte, tioesterul format de acesta din urmă cu CC . Este o moleculă cu potențial ridicat de hidroliză localizată la intersecția mai multor căi metabolice importante. Acetil-CoA , astfel , poate avea ca rezultat, sub acțiunea piruvat dehidrogenază complexe , de oxidare decarboxilarea a piruvatului , care rezultă , de exemplu , de la glicoliză sau din degradarea de acizi grași prin β-oxidare ( Lynen helix ) , în cadrul lipoliza ( degradarea lipidelor ). Acționează în principal ca un substrat al ciclului Krebs pentru a fi oxidat la CO 2și coenzime reduse precum NADH + H + și ubiquinol ( CoQ 10 H 2), precum și ca substrat pentru căile anabolice , cum ar fi biosinteza acizilor grași , în urma unei serii de reacții similare cu reciprocitatea β-oxidării. În timpul postului prelungit, când gluconeogeneza a redus concentrația de oxaloacetat disponibilă pentru a permite acetil-CoA să intre în ciclul Krebs, acetil-CoA duce la formarea corpurilor cetonice - acetilacetat (H 3 C - CO - CH 2 –COO -), β- D- hidroxibutirat (H 3 C - CHOH - CH 2 –COO -) și acetonă (H 3 C - CO - CH 3) - care sunt folosite ca surse de energie metabolică de către mușchi , inimă și creier . Acetil-CoA este de asemenea implicată în biosinteza de acetilcolinei , un neurotransmitator , prin acetilarea de colină sub efectul colinacetiltransferazei .
Funcții biochimice
Conversia piruvatului în acetil-CoA
Oxidativă Decarboxilarea a piruvatului la acetil-CoA este catalizată de piruvat dehidrogenază complex . Există și alte reacții care fac posibilă formarea acetil-CoA din piruvat, cum ar fi dismutarea piruvatului în acetil-CoA și formatul prin piruvat formatul liasa .
Sinteza directă
Acetil-CoA poate fi format prin acetilarea directă a coenzimei A sub acțiunea acetil-CoA sintază din metan CH 4și dioxid de carbon CO 2. Această reacție apare, de exemplu, în modularea expresiei genelor prin formarea histonei acetiltransferazelor permițând acetilarea histonelor, precum și în calea Wood-Ljungdahl de fixare a carbonului în condiții anaerobe folosind o enzimă al cărei loc activ conține nichel .
Intrarea în ciclul Krebs
Acetil CoA este produsă atât prin degradarea de carbohidrat prin glicoliză și degradarea acizilor grași , care constituie lipida prin β-oxidare . Acesta intră în ciclul Krebs a mitocondriilor prin reacția cu oxaloacetat pentru a forma citrat , cu eliberarea unui liber coenzima A. Unitatea de acetil vândută este oxidată acolo la CO 2și coenzime reduse precum NADH + H + și ubiquinol ( CoQ 10 H 2) Care , la rândul lor , sunt complet oxidate la H 2 Oprin lanțul respirator ; energia eliberată de aceste oxidari generează un gradient de electrochimică a lungul membranei mitocondriale care permite fosforilarea de ADP la ATP sub acțiunea ATP sintaza prin chemiosmotic de cuplare .
Formarea cetonelor
In ficat , oxaloacetat poate fi utilizat pentru biosinteza a glucozei prin gluconeogenezei când posteau extins la dieta saraca in carbohidrati, efort fizic intens și prelungit, și diabet zaharat de tip 1 necontrolate. În aceste condiții, marcate de un nivel ridicat de glucagon și un foarte scăzut nivel de insulină în sânge , oxaloacetat este redus la malat , care lasă mitocondriile să fie convertite în glucoză în citoplasmă a hepatocitelor , de unde este produsă. câștigă circulația sângelui . În consecință, oxaloacetatul încetează să mai fie disponibil în ficat pentru condensarea cu acetil-CoA, astfel încât acesta din urmă să se condenseze cu el însuși pentru a forma acetoacetil-CoA H 3 C - CO - CH. 2 –COS - CoAși β- D- hidroxibutirat H 3 C - CHOH - CH 2 –COO -, care dau spontan acetonă H 3 C - CO - CH 3 : acești trei compuși sunt denumiți în general corpuri cetonice . Ele sunt eliberate în fluxul sanguin de unde pot fi absorbite de orice celulă din corp cu mitocondrii : aceste celule reformează acetil-CoA din aceste corpuri cetonice și descompun acest acetil-CoA în mitocondriile lor pentru a extrage energia metabolică.
Spre deosebire de acizii grași , cetonele pot traversa bariera hematoencefalică și, prin urmare, sunt disponibile și ca compuși energetici pentru utilizare de către creier și sistemul nervos central în locul glucozei.
Producția de cetone ca răspuns la stresul fiziologic (post, dietă săracă în carbohidrați, efort intens prelungit) se numește cetoză ; excesul de cetone rezultat din diabetul de tip 1 se numește cetoacidoză .
Biosinteza acizilor grași
Când rata de sânge a insulinei este ridicată și cea a glucagonului este scăzută (de obicei după mese), acetil-CoA derivat din glicolitic și oxaloacetat se condensează pentru a forma citrat , care în loc să fie degradat ciclul Krebs părăsește mitocondriile pentru a se alătura citoplasmei unde este scindat în oxaloacetat și acetil-CoA de citrat lias ATP . Oxaloacetatul revine în mitocondrie sub formă de malat . Acetil-CoA citosolic poate fi apoi utilizat pentru biosinteza acizilor grași prin carboxilarea acetil-CoA în malonil-CoA de acetil-CoA carboxilază . Această reacție are loc în principal în ficat , țesut gras și glande mamare , unde acizii grași se leagă de glicerol pentru a forma trigliceride , principalii compuși de stocare a energiei metabolice la majoritatea animalelor. Acizii grași sunt, de asemenea, constituenți ai fosfolipidelor , cea mai mare parte a straturilor lipidice ale membranelor biologice .
La plante , sinteza de novo a acizilor grași are loc în plastide . Multe semințe acumulează rezerve mari de uleiuri vegetale pentru a promova germinarea și dezvoltarea plantelor până când planta se poate susține singură prin fotosinteză .
Producția de colesterol
Acetil-CoA citosolic poate, de asemenea, să se condenseze cu acetoacetil-CoA pentru a forma 3-hidroxi-3-metilglutaril-CoA (HMG-CoA) prin acțiunea HMG-CoA sintază , care este etapa limitativă în biosinteza colesterolului prin mevalonat . Colesterolul actioneaza ca fiind membranele biologice , în biosinteza hormonilor steroizi , la acizii biliari și vitaminele D .
Alte utilizări
Acetil-CoA este, de asemenea, implicat în diferite alte căi metabolice :
- ca donator de grup acetil în timpul acetilării anumitor reziduuri de lizină de către acetiltransferazele în timpul modificărilor posttranslaționale ale histonelor și proteinelor non-histonice;
- ca precursor al malonil-CoA prin carboxilare în citosol sub efectul acetil-CoA carboxilazei , care deschide calea producției de flavonoide și polichide asociate, alungirea acizilor grași pentru a produce ceruri , cuticule și ulei în Brassicaceae și pentru malonizarea proteinelor și a altor fitochimicale, cum ar fi sesquiterpene , brassinosteroizi și steroli cu membrană.
Note și referințe
- calculate în masă moleculară de „ masele atomice ale elementelor 2007 “ pe www.chem.qmul.ac.uk .
- (în) Hidekazu Takahashi, J. Michael McCaffery, Rafael A. Irizarry și Jef D. Boeke , " Acetil-coenzima nucleozitosolică este necesară o sintetază pentru acetilarea histonei și transcrierea globală " , Molecular Cell , Vol. 23, n o 2 21 iulie 2006, p. 207-217 ( PMID 16857587 , DOI 10.1016 / j.molcel.2006.05.040 , citiți online )
- (în) Javier Seravalli, Manoj Kumar și Stephen W. Ragsdale , " Rapid Kinetic Studies of Acetyl-CoA Synthesis: Evidence Supporting the Catalytic Intermediacy of a NiFeC Paramagnetic Species in the Wood-Ljungdahl Pathway autotrophic " , 41 , vol. 6, 12 februarie 2002, p. 1807-1819 ( PMID 11827525 , DOI 10.1021 / bi011687i , citiți online )
- (în) Eric L. Hegg , „ Dezlegarea structurii și mecanismului acetil-coenzimei A Synthase ” , Accounts of Chemical Research , Vol. 37, n o 10, octombrie 2004, p. 775-783 ( PMID 15491124 , DOI 10.1021 / ar040002e , citiți online )
- (en) P. Ferré și F. Foufelle , „ SREBP-1c factor de transcripție și homeostazie lipidică: perspectivă clinică ” , Hormone Research , vol. 68, n o 2 2007, p. 78-82 ( PMID 17344645 , DOI 10.1159 / 000100426 , citiți online )
- (în) Beth L. Fatland, Basil J. Nikolau și Eve Syrkin Wurtele , " Reverse Genetic Characterization of Cytosolic Acetyl-CoA Generation by ATP-citrate lyase in Arabidopsis " , The Cell Cell , Vol. 17, n o 1, ianuarie 2005, p. 182-203 ( PMID 15608338 , PMCID 544498 , DOI 10.1105 / tpc.104.026211 , JSTOR 4130763 , citiți online )