Glutation reductaza
| Glutation reductaza | |||||||||||||||||||
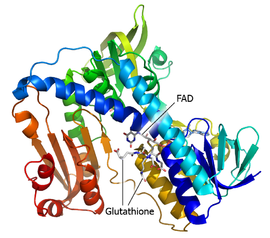 Structura unei glutation reductază cristalizată care prezintă FAD și cele două molecule de glutation ( PDB 1GRE ) | |||||||||||||||||||
| Caracteristici principale | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Numele aprobat | Glutation disulfură reductază | ||||||||||||||||||
| Simbol | GSR | ||||||||||||||||||
| CE nr. | 1.8.1.7 | ||||||||||||||||||
| Homo sapiens | |||||||||||||||||||
| Locus | 8 pag. 12 | ||||||||||||||||||
| Greutate moleculară | 56 257 Da | ||||||||||||||||||
| Număr de reziduuri | 522 aminoacizi | ||||||||||||||||||
| Linkuri accesibile din GeneCards și HUGO . | |||||||||||||||||||
| |||||||||||||||||||
A glutation reductaza este o oxidoreductaza care catalizează reacția :
2 glutation + NADP + disulfură de glutation + NADPH + H + .Această enzimă reduce disulfura de glutation în glutation folosind NADPH, în special din calea pentozei fosfat în bacterii , plante și animale pentru a regenera molecula de glutation, esențială pentru rezistența împotriva stresului oxidativ și conservarea pH-ului intracelular.
Glutationul reductază este conservat în toate regatele vii . Există o singură genă care codifică glutation reductaza la bacterii , drojdii și animale . Genomului a plantelor cod cu toate acestea două izoenzimelor . Drosophila și tripanosomele lipsa de glutation reductaza , dar realiza reducerea glutation folosind respectiv tioredoxină și tripanotion . La om , este codificată de gena GSR de pe cromozomul 8 .
Glutation disulfură reductază| CE nr. | EC |
|---|---|
| numar CAS | |
| Cofactor (i) | ADF |
| IUBMB | Intrare IUBMB |
|---|---|
| IntEnz | Vizualizare IntEnz |
| BRENDA | Intrarea BRENDA |
| KEGG | Intrare KEGG |
| MetaCyc | Calea metabolică |
| PRIAM | Profil |
| PDB | Structuri |
| MERGE | AmiGO / EGO |
Note și referințe
- (în) P. Andrew Karplus și Georg E. Schulz , „ Substrat de legare și cataliză prin glutation reductază enzimă ca derivat din rafinat: Structuri de cristal substrat la rezoluție 2A ” , Journal of Molecular Biology , vol. 210, n o 1, 5 noiembrie 1989, p. 163-180 ( PMID 2585516 , DOI 10.1016 / 0022-2836 (89) 90298-2 , citiți online )
- Valorile pentru masa și numărul de resturi indicate aici sunt cele ale precursorului de proteină care rezultă din traducerea a genei , inainte de modificări post-translaționale și pot diferi în mod semnificativ de valorile corespunzătoare pentru proteine funcționale.
- (în) Marcel Deponte , " Cataliza glutationului și mecanismele de reacție ale enzimelor dependente de glutation " , Biochimica și Biophysica Acta (BBA) - Subiecte generale , Vol. 1830 nr . 5, Mai 2013, p. 3217-3266 ( PMID 23036594 , DOI 10.1016 / j.bbagen.2012.09.018 , citiți online )
- (în) Alton Meister , „ Metabolismul glutationului și modificarea sa selectivă ” , Journal of Biological Chemistry , vol. 263, nr . 33, 25 noiembrie 1988, p. 17205-17208 ( PMID 3053703 , citiți online )
- (în) B. Mannervik , " Enzimele metabolismului glutationului: o privire de ansamblu " , Biochemical Society Transactions , Vol. 15, n o 4, August 1987, p. 717-718 ( PMID 3315772 , citiți online )
- (în) Stefan M. Kanzok Anke Fechner Holger Bauer, Julia K. Ulschmid Hans-Michael Müller, Jose Botella-Munoz, Stephan Schneuwly, R. Heiner Schirmer și Katja Becker , „ Înlocuirea sistemului Thioredoxin pentru glutation reductază în Drosophila melanogaster ” , Știință , vol. 291, nr . 5504, 26 ianuarie 2001, p. 643-646 ( PMID 11158675 , DOI 10.1126 / science.291.5504.643 , citiți online )
- (în) R. Luise Krauth-Siegel și Marcelo A. Comini , " control redox în tripanosomatide, protozoare parazitare cu metabolism pe bază de tipanotion tiol " , Biochimica et Biophysica Acta (BBA) - General Subjects , Vol. 1780 n o 11, Noiembrie 2008, p. 1236-1248 ( PMID 18395526 , DOI 10.1016 / j.bbagen.2008.03.006 , citiți online )
