Aziridină
| Aziridină | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificare | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Numele IUPAC | aziridină | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sinonime |
azaciclopropan |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.005.268 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 205-793-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 9033 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 30969 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ZÂMBETE |
C1CN1 , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C2H5N / c1-2-3-1 / h3H, 1-2H2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspect | lichid uleios incolor și limpede | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietăți chimice | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formula brută |
C 2 H 5 N [Izomeri] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masă molară | 43,0678 ± 0,0022 g / mol C 55,78%, H 11,7%, N 32,52%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Momentul dipolar | 1,90 ± 0,01 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietăți fizice | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fuziune | −78 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fierbere | 56 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa volumică | 0,8321 g · cm -3 până la 20 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura de autoaprindere | 320 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punct de aprindere | −13 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Limite explozive în aer |
3,6 - 46 % vol 64 - 820 g · cm -3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Presiunea saturată a vaporilor |
213 mbar la 20 ° C 333 mbar la 30 ° C 780 mbar la 50 ° C |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochimie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 lichid | 91,9 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
ecuaţie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | -1 591,36 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauții | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   B2, D1A, D2A, E, |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 4 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Directiva 67/548 / CEE | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 T +  F  NU Număr index : Clasificare : F; R11 - Carc. Pisică. 2; R45 - Muta. Pisică. 2; R46 - T +; R26 / 27/28 - C; R34 - N; R51-53 Simboluri : T + : Foarte toxic F : Foarte inflamabil N : Periculos pentru mediu Fraze R : R11 : Foarte inflamabil. R34 : Provoacă arsuri. R45 : Poate provoca cancer. R46 : Poate provoca daune genetice ereditare. R26 / 27/28 : Foarte toxic prin inhalare, în contact cu pielea și în caz de înghițire. R51 / 53 : Toxic pentru organismele acvatice, poate provoca efecte adverse pe termen lung asupra mediului acvatic. Fraze S : S45 : În caz de accident sau dacă vă simțiți rău, solicitați imediat sfatul medicului (arătați eticheta acolo unde este posibil). S53 : Evitați expunerea - obțineți instrucțiuni speciale înainte de utilizare. S61 : Evitați eliberarea în mediu. Consultați instrucțiunile speciale / fișa cu date de siguranță. Fraze R : 11, 26/27/28, 34, 45, 46, 51/53, Fraze S : 45, 53, 61, |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
663 : material foarte toxic și inflamabil (punct de aprindere egal sau mai mic de 60 ° C ) Număr ONU : 1185 : ETILENEIMINĂ, STABILIZATĂ Clasa: 6.1 Etichete: 6.1 : Substanțe toxice 3 : Lichide inflamabile Ambalare: Grupa de ambalare I : foarte materiale periculoase;   |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Clasificarea IARC | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupa 2B: posibil cancerigenă pentru oameni | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ecotoxicologie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 |
15 mg · kg -1 (șobolan, oral ) 3,5 mg · kg -1 (șobolan, ip ) 4 mg · kg -1 (șoareci, ip ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pragul mirosului | scăzut: 2 ppm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unități de SI și STP, cu excepția cazului în care se prevede altfel. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Aziridinei (nf) sau azacyclopropane este compus organic ciclic cu formula empirică C 2 H 5 N. De asemenea , compusul părinte și aziridine grup funcțional corespunzător unui heterociclu în trei părți compuse dintr - o amină și două metilen grupe .
Producție și sinteză
Aziridinele pot fi preparate în chimie organică în multe feluri.
Ciclizarea haloaminelor și amino alcoolilor
O grupare amină poate deplasa o halogenură adiacentă (la β) într-o reacție de substituție nucleofilă intramoleculară pentru a forma o aziridină. Aminoalcoolii au aceeași reactivitate, dar grupurile hidroxid trebuie mai întâi convertite în grupuri mai bine părăsite, de exemplu tosilat . Ciclizarea unui amino alcool este numit sinteza Wenker (in) (1935) și unul dintre haloamine, etilenimină-metoda lui Gabriel (1888)
Adăugarea de azot
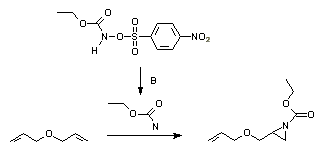
Adăugarea unui nitren la o alchenă este o metodă bine stabilită pentru sinteza aziridinelor. Fotoliză sau thermolyses de azide sunt o modalitate buna de a genera nitrene. Acestea pot fi, de asemenea, generate in-situ din diacetat de iodobenzen și sulfonamide sau sulfamați sau din etoxicarbonil nitrenul unui precursor de N-sulfoniloxi:
Descompunerea triazolinelor
Sub tratament termic sau prin fotoliza unei triazoline , azotul este expulzat și rămâne o aziridină. Triazolina necesară este obținută dintr-o reacție de cicloadiție a unei azide la o alchenă.

Prin deschiderea unui epoxidic
O metodă constă într-o reacție de deschidere a inelului unui epoxid cu azidă de sodiu urmată de o reducere organică a azidei obținută cu trifenilfosfină prin expulzarea azotului gazos:

O altă metodă constă în reacția de deschidere a unui epoxid de o amină urmată de reînchiderea inelului printr-o reacție Mitsunobu .
Reacția unei oxime cu un reactiv Grignard
Sinteza etileniminei Hoch-Campbell descrie sinteza aziridinelor prin reacția anumitor oxime cu reactivii Grignard :

Caracteristici fizico-chimice
Structura
Unghiurile de legătură din aziridină sunt în jur de 60 °, ceea ce este considerabil mai mic decât unghiul de 109,5 ° care se găsește în mod normal în hidrocarburile sau aminele liniare și nelimitate. Aceste unghiuri sunt totuși comparabile cu cele găsite în ciclopropan sau inele oxiran și corespund acelorași constrângeri unghiulare din inel: legăturile din acest tip de inel pot fi explicate prin invocarea unui model de legătură banană. Aziridina este mai puțin bazică decât o amină aciclică și alifatică cu un pKa de 7,9 pentru acidul conjugat, care se datorează unei creșteri a caracterului s în perechea liberă de azot . Tensiunile unghiulare crescute în aziridină sunt, de asemenea, responsabile de bariera energetică crescută pentru inversarea azotului . Această barieră este suficient de mare în aziridine pentru a putea separa invertomerii, cum ar fi invertomerii cis și trans ai N-cloro-2-metilaziridinei.
Reacții
Deschiderea inelului nucleofilAziridinele sunt substraturi sensibile la reacțiile de deschidere a inelului cu mulți nucleofili datorită constrângerilor moleculare din inel. Alcoolizele și amoniacele sunt de obicei reacțiile inverse ale ciclizărilor. Alți nucleofili eficienți sunt carbonii nucleofili, cum ar fi în reactivi organolitici sau organocuprați, cum ar fi reactivul Gilman .
O aplicație importantă a unei reacții de deschidere a inelului în sinteza asimetrică este aceea cu trimetilsililazida TMSN 3 și un ligand asimetric:
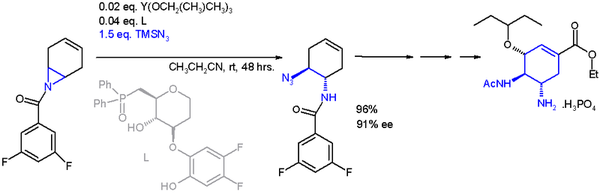
Catalizatorul este construit pe ytriu și trei substituenți izopropiloxi, ligandul este un oxid de fosfină. Cu un exces enantiomeric de 91% ee, această reacție permite sinteza totală a oseltamivirului ( Tamiflu ).
Alte reacțiiAziridinele nesubstituite pot fi deschise prin alchene în prezența unui acid Lewis puternic precum B (C 6 F 5 ) 3 Unele aziridine N-substituite și cu grupuri de retragere de electroni pe ambii atomi de carbon formează ilide azometină prin reacție deschiderea inelului electrociclic (en) . Acești ilizi pot fi prinși cu un dipolarofil adecvat printr-o cicloadiție 1,3-dipolară .
Securitate
Toxicologia fiecărui aziridine specific depinde de propria structură și activitate care participă la caracteristicile generale ale grupului aziridină. Fiind electrofile , aziridinele sunt capabile să atace și să aibă ciclul deschis de nucleofili endogeni, cum ar fi bazele nucleice ale ADN-ului , care corespunde unui potențial mutagen și poate induce, de asemenea, în anumite cazuri, o activitate antitumorală.
Astfel, inhalarea și contactul direct cu aziridine sunt interzise. Unele rapoarte menționează că nici mănușile utilizate în mod normal în chimie nu împiedică infiltrarea pielii cu aziridine. Prin urmare, este important ca utilizatorii să verifice timpii de îmbibare a mănușii și să aibă mare grijă să evite contaminarea atunci când scoate mănușile.
Agenția Internațională pentru Cercetarea Cancerului (IARC ) a analizat compușii aziridinici și i-a clasificat ca un posibil cancerigen uman (grupa 2B). În efectuarea unei evaluări generale, Grupul de lucru IARC a luat în considerare faptul că aziridinele sunt agenți de alchilare directă, care sunt mutageni într-o gamă largă de sisteme de testare și formează aducti ADN care sunt promutagenici.
Aziridinele provoacă efecte iritante asupra membranelor mucoase, cum ar fi ochii, nasul, sistemul respirator și chiar pielea. Aziridinele pătrund rapid în piele la contact. Ele pot provoca boli alergice ale pielii și urticarie sau pot duce la astm .
Note
- Aziridine.pdf pe IARC
- (în) David R. Lide, Manual de chimie și fizică , Boca Raton, CRC,16 iunie 2008, 89 th ed. , 2736 p. ( ISBN 978-1-4200-6679-1 și 1-4200-6679-X ) , p. 9-50
- calculate în masă moleculară de „ masele atomice ale elementelor 2007 “ pe www.chem.qmul.ac.uk .
- (ro) „Etilenimină” , pe NIST / WebBook , accesat la 22 iulie 2009
- Manual CRC de chimie și fizică, ed. 59, ( ISBN 978-0-8493-0549-8 )
- Intrarea „Etilenimină” în baza de date chimice GESTIS a IFA (organism german responsabil cu securitatea și sănătatea în muncă) ( germană , engleză ), accesat la 22 iulie 2009 (JavaScript necesar)
- (în) Carl L. Yaws, Manual de diagrame termodinamice , vol. 1, Huston, Texas, Gulf Pub. Co,1996( ISBN 0-88415-857-8 )
- Grupul de lucru IARC pentru evaluarea riscurilor cancerigene pentru oameni, „ Evaluations Globales de la Carcinogenicité pour l'Homme, Groupe 2B: Possibil cancerigen pentru oameni ” , pe http://monographs.iarc.fr , IARC,16 ianuarie 2009(accesat la 22 august 2009 )
- „Etilen imină” în baza de date cu produse chimice Reptox a CSST (organizația din Quebec responsabilă de securitatea și sănătatea în muncă), accesată la 22 iulie 2009
- Universitatea UCB din Colorado
- (în) „ aziridină ” pe ChemIDplus , accesat la 22 iulie 2009
- " etilenimină, " la hazmap.nlm.nih.gov (accesat 14 noiembrie 2009 )
- Chimie heterociclică , TL Gilchrist. ( ISBN 0-582-01421-2 )
- Epoxizi și aziridine - O mini recenzie , Albert Padwaa și S. Shaun Murphreeb; Arkivoc (JC-1522R), p. 6-33 . articol online
- Metoda Gabriel Ethylenimine
- Reacții suplimentare de etoxicarbonilnitren și ion etoxicarbonil nitreniu la eteri alilici M. Antonietta Loreto și colab.; Tetrahedron Letters, 1984, vol. 25 (38), p. 4271-4274 . rezumat
- Fotodecompoziție triazolină: Prepararea aziridinelor , P. Scheiner; Tetraedru, 1968, vol. 24 (6), p. 2757-2765 . DOI : 10.1016 / S0040-4020 (01) 82547-3 .
- Aminoaldehidele neprotejate disponibile , Ryan Hili și Andrei K. Yudin; J. Am. Chem. Soc. , 2006, vol. 128 (46), p. 14772-14773 . DOI : 10.1021 / ja065898s .
- Aravinda B. Pulipaka, Stephen C. Bergmeier.; Sinteza, 2008, vol. 9, p. 1420-1430
- Hoch, Compt. rend., 196, 1865 (1934); (a), ibid., aOS, 799 (1936); (e), ibidem, 204, 358 (1937).
-
Acțiunea reactivilor Grignard asupra oximelor. I. Acțiunea bromurii de fenilmagneziu asupra cetoximelor mixte , Kenneth N. Campbell, James F. Mckenna; J. Org. Chem., 1939, vol. 4 (2), p. 198-205 . DOI : 10.1021 / jo01214a012 .
Reacția reactivilor Grignard cu oxime. II. Acțiunea reactivilor aryl grignard cu ketoxime mixte , Kenneth N. Campbell, Barbara Knapp Campbell, Elmer Paul Chaput; J. Org. Chem., 1943, vol. 8 (1), p. 99-102 . DOI : 10.1021 / jo01189a015 .
Acțiunea reactivilor Grignard asupra oximelor. III. Mecanismul acțiunii halogenurilor de arilmagneziu asupra ketoximelor mixte. O nouă sinteză a etileniminelor , Kenneth N. Campbell, Barbara K. Campbell, James F. Mckenna și Elmer Paul Chaput; J. Org. Chem., 1943, p. 103-109 . DOI : 10.1021 / jo01189a016 - De Novo Synthesis of Tamiflu via a Catalytic Asymmetric Ring-Opening of mezo-Aziridines with TMSN3 , Yuhei Fukuta et al.; J. Am. Chem. Soc. , 2006, vol. 128 (19), p. 6312-6313 . DOI : 10.1021 / ja061696k .
- Aravinda B. Pulipaka și Stephen C. Bergmeier.; J. Org. Chem., 2008, vol. 73, p. 1462-1467
- Sensibilizarea respiratorie și a pielii ocupațională cauzată de întăritorul polifuncțional aziridinic , L. Kanerva și colab. Alergie clinică și experimentală, 1995, vol. 25 (5), p. 432–439 .
- Boală alergică a pielii și a căilor respiratorii cauzată de aziridina polifuncțională , Sartorelli P și colab. Med Lav., 2003, vol. 94 (3), p. 285-95 .
- Agenți, vechi și noi, care provoacă astm profesional , Mapp CE; Ocupa. Despre. Med., 2001, vol. 58, p. 354-60
- Giorgi-Renault, S., Renault J., Baron M., Gebel-Servolles, P., Delic, J., Cros S., Paoletti C., Heterocyclic quinones XIII. Dimerizarea în seria 5,8-chinazolinedionelor: Sinteza și efectele antitumorale ale bis (4-amino-5,8-chinazolinediunilor), Chem. Pharm. Bull., 36 (10), 3933-3947 (1988).
- Volumul 9.pdf, Unele aziridine, ...
- ( fr ) Acest articol este preluat parțial sau în totalitate din articolul Wikipedia în limba engleză intitulat „ Aziridine ” ( vezi lista autorilor ) .
Link extern
- Desimetriția mezo aziridinelor în special de la 1.2.



