2,4-Dinitrofenol
| 2,4-Dinitrofenol | |||
 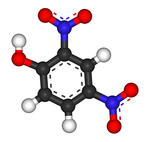 Structura probei DNP pure 2,4-dinitrofenol  |
|||
| Identificare | |||
|---|---|---|---|
| Numele IUPAC | 2,4-dinitrofenol | ||
| Sinonime |
1-hidroxi-2,4-dinitrobenzen |
||
| N o CAS | |||
| N o ECHA | 100.000.080 | ||
| N o EC | 200-087-7 | ||
| DrugBank | DB04528 | ||
| PubChem | 1493 | ||
| ChEBI | 918 | ||
| ZÂMBETE |
C1 = CC (= C (C = C1 [N +] (= O) [O -]) [N +] (= O) [O -]) O , |
||
| InChI |
InChI: InChI = 1S / C6H4N2O5 / c9-6-2-1-4 (7 (10) 11) 3-5 (6) 8 (12) 13 / h1-3.9H |
||
| Proprietăți chimice | |||
| Formula brută |
C 6 H 4 N 2 O 5 [Izomeri] |
||
| Masă molară | 184.1064 ± 0,007 g / mol C 39,14%, H 2,19%, N 15,22%, O 43,45%, |
||
| pKa | 4,09 la 25 ° C | ||
| Proprietăți fizice | |||
| T ° fuziune | 115 ° C | ||
| T ° fierbere | 113 ° C | ||
| Solubilitate | 2,79 g · l -1 ( apă , 20 ° C ) | ||
| Masa volumică | 1,68 g · cm -3 | ||
| Temperatura de autoaprindere | |||
| Termochimie | |||
| Δ f H 0 solid | -235,5 kJ · mol -1 | ||
| Δ fus H ° | 24,174 kJ · mol -1 până la 114,85 ° C | ||
| PCI | -2 697,2 kJ · mol -1 | ||
| Precauții | |||
| SGH | |||
   Pericol H301, H311, H331, H373, H400, H301 : Toxic în caz de înghițire H311 : Toxic în contact cu pielea H331 : Toxic prin inhalare H373 : Poate provoca leziuni ale organelor (enumerați toate organele afectate, dacă sunt cunoscute) după expunere repetată sau expunere prelungită (indicați calea de expunere dacă este dovedit în mod nici o altă cale de expunere nu provoacă același pericol) H400 : Foarte toxic pentru organismele acvatice |
|||
| WHMIS | |||
|
Produs neclasificatClasificarea acestui produs nu a fost încă validată de divulgarea serviciului directorului toxicologic la 0,1% conform listei de divulgare a ingredientelor. |
|||
| Transport | |||
46 :, toxic solid inflamabil sau auto - încălzire Numărul ONU : 1320 : dinitrofenol umidifica cu cel puțin 15 procente (masa) de apă Clasa: 4.1 Etichete: 4.1 : Substanțe solide inflamabile, solide explozive autoreactive și desensibilizate 6.1 : Toxic substanțe Ambalare: Grupa de ambalare I : substanțe foarte periculoase;   |
|||
| Ecotoxicologie | |||
| LogP | 1,54 | ||
| Unități de SI și STP, cu excepția cazului în care se prevede altfel. | |||
2,4-dinitrofenol ( DNP ) este un compus aromatic cu formula chimică C 6 H 4 N 2 O 5 . Este unul dintre cei șase izomeri ai dinitrofenolului .
Este o otravă a metabolismului celular . Se decuplează fosforilarea oxidativă prin transportarea protoni peste membrana mitocondrial , ceea ce conduce la o creștere rapidă a consumului de oxigen , în paralel cu o formare redusă ATP .
Proprietăți chimice
2,4-Dinitrophenol este un solid cristalin galben, care are un miros dulce, mucegăit. Este foarte volatil, se sublimează când este ușor încălzit și apoi degajă abur. Este moderat solubil în apă (sărurile sale de sodiu sunt cristale solubile în apă), acetat de etil , acetonă , cloroform , piridină , tetraclorură de carbon , toluen , etanol , benzen și soluții alcaline apoase. Formează săruri explozive cu alcalii și amoniac și emite vapori toxici de oxizi de azot atunci când sunt încălziți până la descompunere. Este incompatibil cu metalele grele și compușii lor.
Sinteză
Utilizări industriale
2,4-Dinitrofenolul este utilizat comercial în principal în cercetarea științifică și industria prelucrătoare. A fost folosit la un moment dat pentru a face coloranți , alte produse utilizate în chimia organică și produse pentru tratarea lemnului. De asemenea, a fost folosit pentru a produce produse pentru a dezvolta fotografii, explozivi și pesticide.
Utilizări în cercetare
Dinitrofenolul este, de asemenea, utilizat pentru identificarea cetonelor. DNP se combină cu cetone și punctul de topire rezultat al compusului ajută la determinarea cetonei.
Acțiune farmacologică
În celulele vii, dinitrofenolul acționează ca un transportor de protoni ( ionofori ), un agent care poate transporta protoni (ioni de hidrogen) prin membranele biologice. Acesta contracarează gradientul de protoni din membranele mitocondriilor și cloroplastelor și face ca gradientul electrochimic pe care celula îl folosește pentru a produce energia chimică a majorității moleculelor ATP să se prăbușească . În loc să producă ATP, energia gradientului de protoni se pierde sub formă de căldură . Celulele compensează producția scăzută de ATP prin oxidarea suplimentară a depozitelor depozitate sub formă de carbohidrați și grăsimi .
Dinitrofenolul este adesea folosit în cercetarea în biochimie pentru a explora funcționarea osmozei chimice și a altor mecanisme ale proteinelor de transport ale membranelor.
Toxicitate asupra mediului
Dinitrofenolul este considerat un contaminant semnificativ pentru mediu de către Agenția Statelor Unite pentru Protecția Mediului (EPA). Acesta a fost găsit în 61 din cele 1.400 de locații prioritare care trebuie curățate de deșeurile industriale. Poate contamina atmosfera din gazele de eșapament ale automobilelor, arderea anumitor substanțe industriale și reacția azotului în aerul atmosferic cu alte substanțe chimice. Principalul loc de degradare este solul, unde este metabolizat de microorganisme.
Dar efectele dinitrofenolului asupra microorganismelor anaerobe sunt încă slab înțelese. Unele studii sugerează că există toxicitate pentru organismele anaerobe din cauza producției reduse de metan.
Toxicologie profesională
La locul de muncă, 2,4-dinitrofenolul este ingerat pe cale respiratorie (praf, vapori) și în special prin piele. Efectele otrăvirii dermice acute și prin inhalare nu au fost studiate.
Se utilizează ca tratament de slăbire
În anii 1930 , dinitrofenolul a fost utilizat pe scară largă în pastilele dietetice, după ce Cutting and Tainter de la Universitatea Stanford a făcut primul lor studiu cu privire la capacitatea medicamentelor de a-și crește dramatic activitatea metabolică. Dinitrofenolul acționează ca un transportor de protoni în membrana mitocondrială , inhibând fosforilarea oxidativă a ATP și făcând producția de energie mai puțin eficientă. Acest lucru se datorează faptului că o parte din energia care este produsă în mod normal din respirația celulară este irosită ca căldură. Această lipsă de eficacitate este proporțională cu doza de dinitrofenol care este absorbită. Astfel, atunci când doza crește, producția de energie devine mai puțin eficientă: metabolismul este apoi activat - se ard mai multe grăsimi - pentru a compensa ineficiența și a satisface cererea de energie. Interesant, factorul care limitează cel mai mult creșterea dozelor de dinitrofenol nu este lipsa producției de energie de către ATP, ci mai degrabă o creștere excesivă a temperaturii corpului datorită căldurii produse. Ca urmare, o supradoză de dinitrofenol va provoca o febră fatală. Efectele secundare periculoase și, în special, cataracta care s-au dezvoltat, au condus rapid la interzicerea dinitrofenolului în Statele Unite în cursul anului 1938. Cu toate acestea, dinitrofenolul continuă să fie folosit de unii culturisti și sportivi pentru a pierde rapid în greutate. Supradozajele letale sunt rare, dar sunt încă raportate ocazional. În 2007, o germană a murit după ce a ingerat DNP. Confruntat cu aceste otrăviri, inclusiv una fatală în Regatul Unit, Interpol publică înMai 2015o alertă la nivel mondial, o „notificare portocalie”, în fața acestui produs ilicit, cu utilizare potențial fatală. Numai în Anglia și Țara Galilor, între 2007 și 2016, dinitrofenolul a fost menționat pe certificatul de deces ca fiind implicat în 15 decese.
În timp ce dinitrofenolul este considerat de mulți ca fiind prea periculos pentru uz uman, mecanismul său de acțiune rămâne obiectul studiului ca o abordare potențială de tratament pentru obezitate. În prezent, cercetarea se concentrează pe proteinele inhibitoare care apar în mod natural la om.
Note și referințe
- (în) ' 2.4- Dinitrophenol " pe ChemIDplus , accesat pe 9 iulie 2009
- calculate în masă moleculară de „ masele atomice ale elementelor 2007 “ pe www.chem.qmul.ac.uk .
- (în) „Fenol, 2,4-dinitrofenol” pe NIST / WebBook , accesat la 9 iulie 2009
- 2, 4 - DINITROFENOL UMIDIFICAT , fișă (e) de siguranță a Programului internațional de siguranță chimică , consultată la 9 mai 2009
- Număr index din tabelul 3.1 din anexa VI la Regulamentul CE nr . 1272/2008 (16 decembrie 2008)
- „ 2,4-Dinitrophenol ” în baza de date cu produse chimice Reptox a CSST (organizația din Quebec responsabilă de securitatea și sănătatea în muncă), accesată la 25 aprilie 2009
- Introducerea „2,4-Dinitrophenol” în baza de date chimice GESTIS a IFA (organism german responsabil cu securitatea și sănătatea în muncă) ( germană , engleză ), accesat la 9 iulie 2009 (este necesar JavaScript)
- (în) O'Neil, MJ (ed.) The Merck Index - An Encyclopedia of Chemicals, Drugs, and Biologicals , Whitehouse Station, NJ, Merck and Co. Inc. , 2006, p. 556
- (în) N Irving Sax și Richard J Lewis , Proprietăți periculoase ale materialelor industriale , New York, Van Nostrand Reinhold,1989, A 7- a ed. ( OCLC 17650465 )
- Fișă toxicologică INRS FT95
- (în) McFee RB, Caraccio TR, MA McGuigan, Reynolds SA Bellanger P, " Dying to be thin: a dinitrophenol related fatality " , Toxicologie veterinară și umană , vol. 46, nr . 5,2004, p. 251-4. ( PMID 15487646 )
- (în) Miranda EJ McIntyre IM DR Parker, Gary RD Logan BK " Două decese atribuite utilizării 2,4-dinitrofenol " , Jurnalul de toxicologie analitică , vol. 30, n o 3,2006, p. 219-22 ( PMID 16803658 )
- (în) Anna Hodgekiss, " Tragedia studentului, de 21 de ani, care a murit după ce a luat din greșeală o doză letală de pastile dietetice pe care le-a cumpărat pe internet " , MailOnline ,20 aprilie 2015( citește online )
- „ Interpol emite o alertă globală cu privire la produsele ilicite și potențial letale ” , la www.interpol.int ,4 mai 2015(accesat la 6 mai 2015 )
- (în) „ Numărul deceselor în care a fost menționat dinitrofenolul (DNP) pe certificatul de deces, Anglia și Țara Galilor, 2007-2016 ” , pe www.ons.gov.uk ,24 octombrie 2017(accesat la 11 iunie 2018 )
- (în) Harper JA, Dickinson K, Brand MD, „ Decuplarea mitocondrială ca țintă pentru dezvoltarea medicamentelor pentru tratamentul obezității ” , Obezity reviews: un jurnal oficial al Asociației Internaționale pentru Studiul Obezității , vol. 2, n o 4,2001, p. 255-65. ( PMID 12119996 )
linkuri externe
- (ro) „ Agenția pentru standarde alimentare emite recomandări urgente cu privire la consumul de capsule„ pentru arzător de grăsimi ”care conțin DNP ” , Agenția pentru standarde alimentare ,17 iunie 2003(accesat la 30 septembrie 2007 )
- (ro) „ ToxFAQ about Dinitrophenols ” , Agenția pentru Registrul Substanțelor Toxice și al Bolilor ,Septembrie 1996(accesat la 17 iulie 2005 )
- Informații generale despre 2,4-dinitrofenol.
- " Fișa cu date toxicologice 2,4-Dinitrophenol " , INRS