Complex alfa dehidrogenază-cetoglutarat
2-Oxoglutarat dehidrogenază Structura unui E. coli E1 ( PDB 2JGD )
Structura unui E. coli E1 ( PDB 2JGD )
| CE nr. | EC |
|---|---|
| numar CAS | |
| Cofactor (i) | TPP |
| IUBMB | Intrare IUBMB |
|---|---|
| IntEnz | Vizualizare IntEnz |
| BRENDA | Intrarea BRENDA |
| KEGG | Intrare KEGG |
| MetaCyc | Calea metabolică |
| PRIAM | Profil |
| PDB | Structuri |
| MERGE | AmiGO / EGO |
S -succinyltransferase
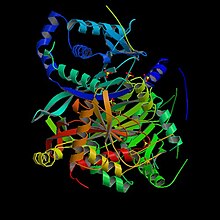 Structura unui E. coli E2 ( PDB 1C4T )
Structura unui E. coli E2 ( PDB 1C4T )
| CE nr. | EC |
|---|---|
| numar CAS |
| IUBMB | Intrare IUBMB |
|---|---|
| IntEnz | Vizualizare IntEnz |
| BRENDA | Intrarea BRENDA |
| KEGG | Intrare KEGG |
| MetaCyc | Calea metabolică |
| PRIAM | Profil |
| PDB | Structuri |
| MERGE | AmiGO / EGO |
 Structura unui E3 uman ( PDB 1ZY8 ).
Structura unui E3 uman ( PDB 1ZY8 ).
| CE nr. | EC |
|---|---|
| numar CAS | |
| Cofactor (i) | ADF |
| IUBMB | Intrare IUBMB |
|---|---|
| IntEnz | Vizualizare IntEnz |
| BRENDA | Intrarea BRENDA |
| KEGG | Intrare KEGG |
| MetaCyc | Calea metabolică |
| PRIAM | Profil |
| PDB | Structuri |
| MERGE | AmiGO / EGO |
Α-cetoglutarat dehidrogenazei complex , de asemenea , numit oxoglutarate dehidrogenaza complex ( OGDC ), este combinația de trei enzime - un decarboxilaza , un aciltransferazei și un oxidoreductaza - care acționează secvențial , în această ordine de a cataliza reacției :
|
|
+ CoA-SH + NAD + → NADH + H + + CO 2 + |
|
| α-cetoglutarat | Succinil-CoA |
Acest complex enzimatic este implicat în trei căi metabolice : ciclul Krebs , degradarea lizinei și metabolismul triptofanului . Este legat structural de complexul piruvat dehidrogenază și de complexul 3-metil-2-oxobutanoat dehidrogenază . Cele trei enzime care alcătuiesc complexul sunt:
| Enzimă | Abbrev. | Co-factori |
| α-cetoglutarat dehidrogenază EC : decarboxilază |
E1 | Pirofosfat de tiamină (TPP) |
| Dihidrolipoamidă S-succiniltransferază EC : aciltransferază |
E2 | Lipoamidă / dihidrolipoamidă Coenzima A (CoA-SH) |
| Dihidrolipoil dehidrogenază EC : oxidoreductază |
E3 | Flucină adenină dinucleotidă (FAD) Nicotinamidă adenină dinucleotidă (NAD + ) |
Mecanismul acestei reacții, care implică succesiv enzimele E1, E2 și E3, fiecare cu cofactorii săi , este destul de complex și poate fi rezumat prin diagrama simplificată de mai jos:
Regulament
Complexul α-cetoglutarat dehidrogenazei este un punct esențial de reglare a ciclului Krebs . Este inhibat de produsele sale de reacție, adică de succinil-CoA și NADH , și atunci când încărcătura de energie a celulei este mare. În special, este inhibat atunci când raporturile de concentrație [ ATP ] / [ ADP ] , [ NADH ] / [ NAD + ] și [ succinil-CoA ] / [ CoA ] sunt ridicate. În schimb , ADP și cationii de magneziu Mg 2+ și calciu Ca 2+ sunt activatori complex alosteric . Acești efectori alosterici acționează în esență asupra enzimei E1, adică α-cetoglutarat dehidrogenază însăși, dar celelalte două enzime sunt, de asemenea, capabile de reglare alosterică.
Reglarea complexului α-cetoglutarat dehidrogenază acționează prin ricoșare asupra fosforilării oxidative și a producției de ATP prin modularea cantității de coenzime reduse, și în special a NADH, prezentă în celule și, mai precis, în mitocondrii în eucariote : activarea α -cetoglutaratul dehidrogenază complex accelerează fosforilarea oxidativă și crește producția de ATP prin creșterea fluxului de electroni injectați în lanțul respirator din NADH.
Prin activarea lanțului respirator, complexul α-cetoglutarat dehidrogenază crește producția de radicali liberi , ceea ce poate duce la stres oxidativ . Acest complex enzimatic este probabil capabil să reacționeze la creșterea radicalilor liberi din celulă prin reducerea activității sale, ceea ce face posibilă limitarea daunelor induse de derivații reactivi ai oxigenului . Mai precis, poate suferi o inhibiție complet reversibilă în prezența unei concentrații mari de radicali liberi, inhibare care poate fi totală în cazuri extreme. Se crede că inhibarea tranzitorie a complexului mitocondrial apare din glutationul reversibil (en) al domeniului de legare a acidului lipoic al enzimei E2, adică dihidrolipoamida S- succiniltransferază . Glutationilarea este o modificare post-translațională care apare în special în prezența radicalilor liberi și poate fi ridicată sub efectul antioxidant al glutaredoxinei . Această modificare are ca efect protejarea acidului lipoic de oxidare .
Răspunsul la stres
Complexul α-cetoglutarat dehidrogenază joacă un rol în răspunsul celular la expunerea acută la stres. Inhibarea sa temporară este de fapt urmată de o creștere a activității atunci când este ridicată, ceea ce face posibilă compensarea expunerii la stres acut prin supraactivitatea complexului α-ketoglutarat dehidrogenazei.
Efectele expunerii acute la stres sunt în general mai bine tolerate de celule decât cele ale expunerii prelungite sau cronice, atunci când aceste efecte se acumulează. Reactivarea complexului α-cetoglutarat dehidrogenazei după inhibarea din cauza stresului poate fi epuizată atunci când inhibarea devine prea mare. In particular, stresul celular poate duce la o perturbare a biosintezei de glutamat , care, în plus față de rolul său structural ca un aminoacid proteinogenici , este , de asemenea , un neurotransmitator . Neurotoxicitate de glutamat in creier rezultatele de la acumularea sa în urma episoade prea frecvente sau prea prelungite de stres. Această acumulare nu poate fi absorbită atunci când reacția complexului α-ketoglutarat dehidrogenazei încetează să mai fie eficientă și aici se pot dezvolta patologii.
Un complex cu α-cetoglutarat dehidrogenază defect poate, de asemenea, sensibiliza celula la alte toxine care pot duce la neurodegenerare .
Note și referințe
- (în) René AW Frank, Amanda J. Price, Fred D. Northrop, Richard N. Perham și Ben F. Luisi , " Structura cristalină a componentei E1 a complexului Escherichia coli 2-Oxoglutarate Multienzyme Dehydrogenase Complex " , Journal of Molecular Biologie , vol. 368, nr . 3, 4 mai 2007, p. 639-651 ( PMID 17367808 , DOI 10.1016 / j.jmb.2007.01.080 , citiți online )
- (în) James E. Knapp Donald Carroll, Janet E. Lawson, Stephen R. Ernst, Lester J. Reed și Marvin L. Hackert , „ xpression, purificare și analiză structurală a formei trimerice a domeniului catalitic al Escherichia coli dihidrolipoamidă succiniltransferază ” , Protein Science , vol. 9, n o 1, ianuarie 2000, p. 37-48 ( PMID 10739245 , PMCID 2144448 , DOI 10.1110 / ps.9.1.37 , citiți online )
- (în) Ewa M. Ciszak Anna Makal, Young S. Hong, K. Ananthalakshmy Vettaikkorumakankauv Lyubov G. Korotchkina și Mulchand S. Patel , " Cum Dihydrolipoamide dehidrogenaza-legare de proteine Leagă Dihydrolipoamide dehidrogenaza in Human piruvatdehidrogenazei Complex " , Journal of Chimie biologică , vol. 281, nr . 1, 6 ianuarie 2006, p. 648-655 ( PMID 16263718 , DOI 10.1074 / jbc.M507850200 , citiți online )
- (ro) Slawomir Strumilo , „ De multe ori au ignorat faptele despre controlul complexului 2-oxoglutarat dehidrogenazei ” , Biochimie și educație pentru biologie moleculară , vol. 33, nr . 4, Iulie 2005, p. 284-287 ( DOI 10.1002 / bmb.2005.49403304284 , citiți online )
- (în) Feng Qi, Ranjan K. Pradhan, K. Ranjan Dash și Daniel A. Beard , " Cinetica detaliată și reglarea 2-oxoglutaratului dehidrogenază la mamifere " , BMC Biochimie , vol. 12, 26 septembrie 2011, p. 53 ( PMID 21943256 , PMCID 3195097 , DOI 10.1186 / 1471-2091-12-53 , citiți online )
- (în) Laszlo Tretter și Vera Adam-Vizi , „ Alfa-cetoglutarat dehidrogenază: un generator țintă și de stres oxidativ ” , Philosophical Transactions of the Royal Society of London. Seria B, Științe biologice , vol. 360, nr . 1464 29 decembrie 2005, p. 2335-2345 ( PMID 16321804 , PMCID 1569585 , DOI 10.1098 / rstb.2005.1764 , JSTOR 30041424 , citiți online )
- (în) Aaron L. McLain, Pamela A. Szweda și Luke I. Szweda , „ α-Ketoglutarate dehidrogenază: Un senzor redox mitocondrial ” , Free Radical Research , vol. 45, n o 1, ianuarie 2011, p. 29-36 ( PMID 21110783 , PMCID 3169906 , DOI 10.3109 / 10715762.2010.534163 , citiți online )
- (ro) Aaron L. McLain, Peter J. Cormier, Michael Kinter și Luke I. Szweda , „ Glutationilarea α-ketoglutaratului dehidrogenază: natura chimică și susceptibilitatea relativă a modificării acidului lipoic cofactor ” , Radical liber Biologie și medicină , vol. 61, August 2013, p. 161-169 ( PMID 23567190 , PMCID 3883985 , DOI 10.1016 / j.freeradbiomed.2013.03.020 , citiți online )
- (în) Milana AB Applegate, Kenneth M. Humphries și Luke I. Szweda , „ Inhibiție reversibilă a α-cetoglutaratului dehidrogenazei prin peroxid de hidrogen: glutationilarea și protecția acidului lipoic ” , Biochimie , vol. 47, n o 1, 8 ianuarie 2008, p. 473-478 ( PMID 18081316 , DOI 10.1021 / bi7017464 , citiți online )
- (ro) Anastasia Graf, Lidia Trofimova, Alexandra Loshinskaja, Garik Mkrtchyan, Anastasiia Strokina, Maxim Lovat, Adam Tylicky, Slawomir Strumilo, Lucien Bettendorff și Victoria I. Bunik , „ Up-regulare a 2-oxoglutaratului a dehidrogenazei ca răspuns la stres ” , Jurnalul Internațional de Biochimie și Biologie Celulară , vol. 45, n o 1, ianuarie 2013, p. 175-189 ( PMID 22814169 , DOI 10.1016 / j.biocel.2012.07.002 , citiți online )
- (în) Gary E. Gibson, John P. Blass, M. Flint Beal și Victoria Bunik , " Complexul α-cetoglutarat-dehidrogenază: un mediator între mitocondriile și stresul oxidativ în neurodegenerare " , Neurobiologie moleculară , Vol. 31, n o 1, Februarie 2005, p. 43-63 ( PMID 15953811 , DOI 10.1385 / MN: 31: 1-3: 043 , citiți online )