Reacția Bergman
Bergman ciclizare sau inel de închidere a Bergman , numit după chimist american Robert Bergman (de) este o reacție de rearanjare în chimia organică a enediyne un derivat radical de benzen .
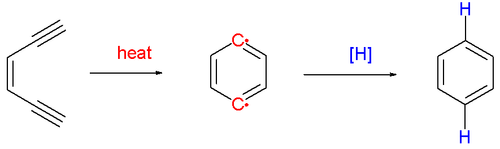
Reacția se desfășoară prin piroliză (peste 200 ° C ), formând un compus diradical 1,4-benzendil , o specie foarte reactivă. Acesta din urmă reacționează cu donatori de radicali hidrogen, cum ar fi ciclohexa-1,4-dienă, pentru a da arena corespunzătoare. Prin tratamentul cu tetraclorometan se obține 1,4-diclorobenzen și cu metanol , alcool benzilic .
Când enina face parte dintr-un inel de 10 carbon (de exemplu, ciclodeca-3-en-1,5-diină din figura de mai jos), reacția poate avea loc la temperaturi mult mai scăzute ( 37 ° C aici) datorită tensiunii ciclului .

Compușii naturali precum calicheamicina conțin aceeași unitate inelară cu 10 carbon și sunt citotoxici . Acestea generează diradicalul intermediar descris mai sus, care poate tăia ADN monocatenar și dublu catenar. Există noi medicamente bazate pe această proprietate, inclusiv anticorpi monoclonali precum mylotarg .
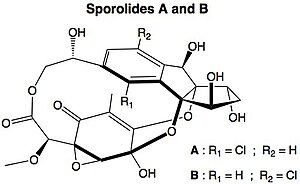
De asemenea, este propus un mecanism diradical pentru formarea anumitor biomolecule de origine marină, sporolidele , care conțin un colorobenzen în structura lor.
În acest mecanism, o sare de halogenură este sursa halogenului. O reacție model cu ciclodeca-1,5-diin-3-enă , bromură de litiu ca sursă de halogen, acid acetic ca sursă de hidrogen în DMSO la 37 ° C face viabilă această teorie:

Reacția este de ordinul întâi în enediyne, cu formarea p- benzzynei A ca etapă limitativă . Ionul halogenură dă apoi doi electroni în timpul formării noii legături Br-C și tranzitelor de electroni radicali printr - o trecătoare de legare C1-C4 pentru a forma intermediarul anion B . Acest anion este o bază puternică capabilă să scoată protoni chiar și din DMSO pentru a da produsul final. Nu se observă formarea compușilor dibromo sau dihidrogen.
linkuri externe
- (ro) Bergman Cycloaromatization Powerpoint Whitney M. Erwin 2002
- (în) Bergman Cycloaromatization Portal Chemistry Organic
Note și referințe
- Name Reactions: O colecție de mecanisme de reacție detaliate de Jie Jack Li Publicat în 2003 Springer ( ISBN 3-540-40203-9 )
- (în) Proiectarea și sinteza precursorilor activați de enediină fuzionată cu heterociclu după dorință Luca Banfi Andrea Basso Giuseppe Guanti și Renata Riva arkivoc 2006 HL-1786GR 261-275 Rezumat
- (în) Charles L. Perrin , Betsy L. Rodgers și Joseph M. O'Connor , " Nucleophilic Addition to a p-Benzyne Derived from year enediyne: A New Mechanism for Halide Incorporation in Biomolecules " , Journal of the American Chemical Society , vol. 129, nr . 15,2007, p. 4795-4799 ( DOI 10.1021 / ja070023e )
- New Route For Halide Addition Stu Borman Chemical & Engineering News 2 aprilie 2007 Link
- ( fr ) Acest articol este preluat parțial sau în totalitate din articolul din Wikipedia engleză intitulat „ Bergman cyclization ” ( vezi lista autorilor ) .