Aryne
Cei arynes sau benzynes sunt intermediari de reacție neutre derivate prin captarea unui arena doi substituenți , lăsând doi orbitali cu doi electroni partajate între ele. La fel ca carbenele și nitrenele , arinele au o stare singletă și o stare tripletă . Cele mai clasice arine sunt orto , dar există și meta- și para-arine. Ortho-arynes sunt exemple de alchine tensionate, iar aryne-ul în sine este 6-annulyne .
Legături în orto-arine
Reprezentarea benzinei cu legătură triplă este cea mai răspândită. Orto-arinii sau 1,2-didehidroarenele sunt descrise în general ca având o legătură triplă strânsă.

Constrângerile geometrice pe legătura triplă din orto- benzină conduc la o reducere a orbitalelor p suprapuse în plan și, prin urmare, la o legătură triplă mai mică. Radziszewski a determinat frecvența vibrațională a legăturii triple a benzinei ca fiind de 1846 cm -1 , indicând o legătură triplă mai slabă decât într-un alchin fără restricții care are o frecvență de vibrație de aproximativ 2150 cm -1 . Cu toate acestea, orto- benzina arată mai mult ca un alchin constrâns decât printr-un biradical, după cum reiese din deviația mare - triplet și reactivitatea asemănătoare alchinului.
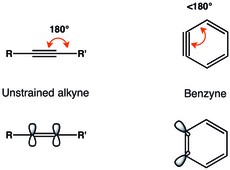
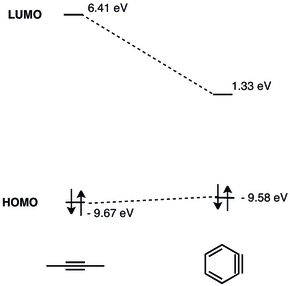
Orbitalul scăzut (BV) vacant al unui arin este mult mai mic decât cel al alchinilor fără restricții, astfel încât interacțiunea este mai bună cu orbitalii ocupați (HO) mari ai nucleofililor. Prin urmare, benzina are un caracter electrofil și suferă reacții cu nucleofili. O analiză detaliată a orbitalilor moleculari ai benzinei a fost prezentată în 1968.
Generarea de orto-arine
Datorită reactivității lor ridicate, arinele trebuie generate in situ . Ca și alți intermediari de reacție , benzina trebuie prinsă, altfel se dimerizează în bifenilenă.
Primele căi spre benzină au implicat dehidrohalogenarea unei halogenuri de arii :
Astfel de reacții necesită o bază puternică și o temperatură ridicată. Arenele orto-disubstituite conduc la benzine în condiții mai blânde. Benzina este generată de deshalogenarea 2-bromofluorobenzenului folosind magneziu. Acidul antranilic poate fi convertit la benzoatediazonium prin diazotizare și neutralizare. Deși este explozivă, această specie zwitterionică este un precursor convenabil și ieftin al benzinei.

O altă metodă se bazează pe triflatele de trimetilsililaril. Deplasarea grupării trimetilsilil de ionul fluor are ca rezultat îndepărtarea triflatului și producerea de benzen:
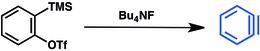
O reacție hexa-dehidro Diels-Alder implică cicloadiția unui 1,3-diin și a unui alchil.

N -amination de benzotriazol cu hydroxylamine- O - sulfonic acidă generează un intermediar care poate fi oxidat la benzyne cu un randament aproape cantitativ folosind plumb (IV) acetat .

Reacțiile orto- arynes
Chiar și la temperaturi scăzute, ariile sunt extrem de reactive. Reactivitatea lor poate fi împărțită în trei categorii principale: (1) adăugări nucleofile, (2) reacții periciclice și (3) inserarea de legături.
Adăugări nucleofile pe arine
Când sunt tratate cu nucleofili bazici, halogenurile de arii deprotonează alfa către grupul părăsit, rezultând în dehidrohalogenare . Benzenul obținut reacționează prin reacție de adiție . Etapa de formare a intermediarului benzină constituie etapa lentă a reacției.

Reacțiile de „cuplare aryne” permit generarea de compuși bifenilici care sunt utili în industria farmaceutică, agricultură și ca liganzi în multe transformări catalizate de metal.
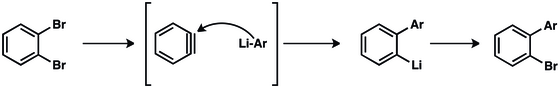
Produsul metal-arenă se poate adăuga, de asemenea, la un alt arin, ducând la polimerizarea lanțului . Folosind cianura de cupru (I) ca inițiator pentru a se adăuga la primul arien, se obțin polimeri care conțin până la aproximativ 100 de unități de arenă.
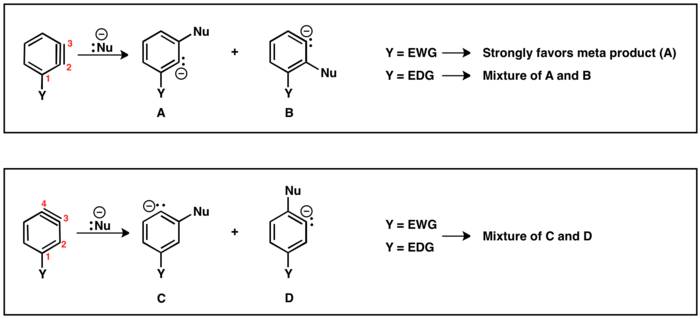
Când grupul părăsit (LG) și substituentul (Y) sunt orto sau para reciproc, este posibil doar un intermediar benzină. Cu toate acestea, atunci când LG și Y sunt meta între ele, sunt posibile mai multe produse (A și B). Dacă Y este un extractor de electroni, atunci H B este mai acid decât H A ceea ce duce la formarea regioizomerului B. Dimpotrivă, dacă Y este un donator de electroni, se generează regioizomerul A, deoarece atunci H A este atunci cel mai acid proton.

Există doi posibili regioizomeri ai benzinei cu substituentul (Y): legătura triplă poate fi poziționată între C2 și C3 sau între C3 și C4. Substituenții orto ai grupului părăsit vor duce la legătura triplă între C2 și C3. Y și LG vor duce la un regioizomer triplu legat între C3 și C4. Substituentul meta poate da cei doi regioizomeri descriși mai sus. În cazul unei triple legături situate între C2 și C3, substituenții care retrag electronii, de exemplu CF3, (GTE) vor direcționa adăugarea de nucleofili pentru a plasa carbanionul cât mai aproape de GTE. Cu toate acestea, substituenții donor de electroni, de exemplu CH 3 (EDG) va avea ca rezultat o selectivitate mică între produse. În regioizomerul în care legătura triplă este localizată între C3 și C4, efectul substituentului asupra adaosului nucleofil este diminuat și se obțin adesea amestecuri de produse para și meta.
Reacții periciclice cu arine
Benzyne suferă o dimerizare rapidă pentru a forma bifenilenă. Anumite procese care produc benzină sunt urmate de această dimerizare într-un mod rapid și cu un randament deosebit de mare. Trimerizarea dă trifenilen .
Benzilii pot suferi reacții Diels-Alder. Când benzina este generată în prezența antracenei , se produce tripticen . Mecanismul concertat al reacției Diels-Alder dintre benzină și furan este prezentat mai jos. Se crede că alte [4 + 2] cicloadiții care implică benzină procedează printr-un mecanism în mai multe etape.

Un exemplu clasic este sinteza 1,2,3,4-tetrafenilnaftalenei. 1,2,4,5-Tetrabromobenzenul poate reacționa cu butillitiu și furan pentru a forma tetrahidroantracen.

Mori și colegii au efectuat ciclizarea [2 + 2 + 2], catalizată de paladiu de arilen și diină în sinteza lor totală a taiwaninelor C.
[4 + 2] cicloadiții de arine au fost utilizate în mod obișnuit pentru sinteza totală a produselor naturale. Principala limitare a acestei abordări este totuși necesitatea de a utiliza diene constrânse, cum ar fi furanul și ciclopentadiena. În 2009, Buszek și colegii săi au sintetizat herbindolul A folosind cicloadiția arinei [4 + 2]. 6,7-Indolină suferă cicloadiție [4 + 2] cu ciclopentadienă pentru a da un produs tetraciclic complex.

Benzilii suferă cicloadiție [2 + 2] cu o gamă largă de olefine. Datorită naturii electrofile a benzinei, olefinele care poartă substituenți de donatori de electroni sunt mai potrivite pentru această reacție.
Datorită unei mari formări de produse secundare, acest tip de reacție este rar utilizat în sinteza totală a produselor naturale. Cu toate acestea, există mai multe exemple. În 1982, Stevens și colab. Au raportat o sinteză de taxodionă folosind [2 + 2] cicloadiție între un arin și o acetal cetenă.

Mori și colegii au efectuat ciclizarea [2 + 2 + 2], catalizată de paladiu de arilen și diină în sinteza lor totală a taiwaninelor C.

Reacții de inserție care leagă aryne
Primul exemplu de reacție de inserție a arilenei prin legătura σ este sinteza melinei în 1973.

Alți dehidrobenzeni
Benzenul este 1,2-didehidrobenzen și are doi izomeri: 1,3-didehidrobenzen și 1,4-didehidrobenzen. Energiile lor in silico sunt respectiv 106, 122 și 138 kcal mol -1 (444, 510 și 577 kJ mol -1 ). Izomerii 1,2 și 1,3 au stări de bază simple, în timp ce pentru 1,4-benzină diferența este mai mică.

A fost studiată interconversia dintre 1,2, 1,3 și 1,4-didehidrobenzeni. O conversie de 1,2 în 1,3-didehidrobenzen a fost postulată în piroliza ( 900 ° C ) a precursorilor de arilen substituiți cu fenil, așa cum se indică mai jos. Pentru interconversia benzină sunt necesare temperaturi extrem de ridicate.

1,4-didehidroarene
Printre experimentele clasice pe 1,4-didehidrobenzen, încălzirea moleculei dideuterate A la 300 ° C produce prin reacție de echilibru molecula B , dar nu și moleculele C sau D. Migrația simultană a atomilor de deuteriu pentru a forma B și absența formării de C sau D poate fi explicat doar prin prezența unui intermediar ciclic și simetric, 1,4-didehidrobenzen.

Au fost luate în considerare două stări pentru 1,4-didehidrobenzen: singlet și triplet, starea singlet fiind mai puțin energică. Starea triplet reprezintă doi centri radicali care nu interacționează și, prin urmare, trebuie să extragă atomii de hidrogen la aceeași viteză ca radicalii fenil. Cu toate acestea, starea singlet este mai stabilizată decât tripleta și, prin urmare, o parte din energia de stabilizare se va pierde pentru a forma starea de tranziție pentru clivajul hidrogenului, care va încetini absorbția hidrogenului. Chen a propus utilizarea analogilor 1,4-didehidrobenzen, care prezintă diferențe mari de energie între single și triplete, pentru a îmbunătăți selectivitatea candidaților la medicamente pe bază de Enediyne.
Istorie
Primele dovezi ale existenței lui Arynes provin din lucrarea lui Stoermer și Kahlert. În 1902, au observat că la tratarea 3-bromobenzofuranului cu o bază în etanol, s-a format 2-etoxibenzofuran. Pe baza acestei observații, ei postulează un arin intermediar.

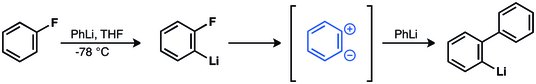
Georg Wittig și colegii săi sugerează că formarea bifenilului prin reacția dintre fluorobenzen și fenilitiu are loc printr-un intermediar zwitterionic. Acest lucru este confirmat experimental de John D. Roberts în 1953.
În 1953, John D. Roberts a descris experimentul de etichetare cu carbon-14, care a furnizat dovezi puternice pentru existența benzinei. Roberts și studenții săi efectuează reacția 1- 14 C-clorobenzen cu amidă de sodiu și analizat încorporarea 14 C tag - ul în anilină rezultat: cantități egale de anilină cu o încorporare de 14 C la C-1 și C-2 s-au observat poziții. Acest rezultat a necesitat un intermediar simetric - numit acum benzină.

La scurt timp după descoperirea lui Roberts, Wittig și Pohmer au descoperit că benzina ar putea participa la reacțiile de cicloadiție [4 + 2].
Dovezi suplimentare pentru existența benzinei au fost furnizate prin studii spectroscopice. Benzyne a fost observat într-un „recipient molecular”.
În 2015, oamenii de știință de la IBM Research și CiQUS de la Universitatea din Santiago de Compostela , Spania, au raportat imagistica unei singure molecule de arna folosind un microscop .
Meta -benzyne este evidențiată pentru prima dată în 1990, de la derivați de benzen 1,3-disubstituite, cum ar fi esterul peroxi 1,3-C 6 H 4 (O 2 C (O) CH 3 ) 2.
Descoperirea care a condus la para-benzine a venit în anii 1960, în urma studiilor reacției Bergman . Acest subiect a devenit actual cu descoperirea ènediynes "citostatic", cum ar fi calicheamicin, care generează un fragment 1,4-didéhydrobenzène care taie ADN-ul dublu catenar.
Exemple de utilizare a benzinelor în sinteza totală
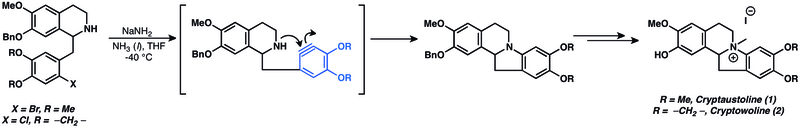
O varietate de produse naturale au fost preparate folosind arine ca intermediari. Adaosurile nucleofile la arine au fost utilizate pe scară largă în sinteza totală a produselor naturale. Într-adevăr, adăugările nucleofile la arine sunt printre cele mai vechi aplicații cunoscute ale chimiei arinei. Acestea sunt utilizate în sinteza criptaustolinei (1) și criptowolinei (2).
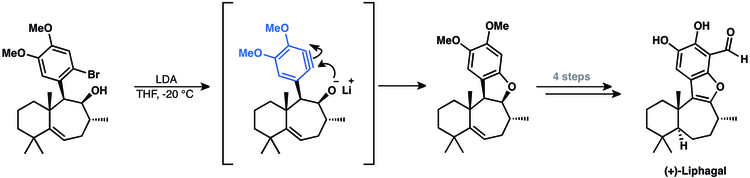
Sinteza meroterpenoidului (+) - liphagal tetraciclic implică un intermediar arinic. Această metodă utilizează ciclizarea arnei pentru a închide ultimul ciclu al produsului natural.
Cele Reacțiile multicomponente cu arynes sunt transformări puternice permit formarea rapidă a arenelor 1,2-disubstituiți. În ciuda utilității lor potențiale, exemplele de reacții multi-componente ale arna în sinteza produselor naturale sunt rare. O reacție de cuplare arilenă cu patru componente a fost utilizată în sinteza dehidroaltenenei B.

Note și referințe
- (în) H. Heaney , „ The Benzyne and Related Intermediates. ” , Chemical Reviews , vol. 62, n o 2Aprilie 1962, p. 81-97 ( DOI 10.1021 / cr60216a001 )
- Hans Henning Wenk, Michael Winkler, Wolfram Sander, „ One Century of Aryne Chemistry ”, Angew. Chem. Int. Ed. , Vol. 42,2003, p. 502 ( DOI 10.1002 / anie.200390151 )
- (in) " {{{title}}} " Compendium of Chemical Terminology [" Gold Book "], IUPAC 1997, versiune corectată online (2006-), ed. A 2- a .
- O intrare în cartea de oaspeți IUPAC pentru „benzine” indică faptul că termenii „ m- benzină” și „ p- benzină” sunt incorecte și ar trebui înlocuit cu 1,3 și 1,4-didehidrobenzen
- Anslyn, EV; Dougherty, DA: Chimie organică fizică modernă , University Science Books, 2006, p.612.
- Gampe, CM; Carreira, EM, „ Arynes and Cyclohexyne in Natural Product Synthesis ”, Angew. Chem. Int. Ed. Engl. , vol. 51, nr . 16,2012, p. 3766–78 ( PMID 22422638 , DOI 10.1002 / anie.201107485 )
- Radziszewski, JG; Hess, Jr. BA; Zahradnik, R., „ Infrared Spectrum of o-Benzyne: Experiment and Theory ”, J. Am. Chem. Soc. , vol. 114,1992, p. 52 ( DOI 10.1021 / ja00027a007 )
- Gilchrist, TL Supliment C: Chimia grupurilor funcționale triple legate, Partea 1 . Patai, S.; Rappaport, Z. Eds., John Wiley & Sons, New York, 1983
- Hoffmann, R.; Imamura, A.; Hehre, WJ J. Am. Chem. Soc. 1968, 90 , 1499
- Wittig, „ Triptycene ”, Org. Sintetizator. , vol. 39,1959, p. 75 ( DOI 10.15227 / orgsyn.039.0075 )
- John M. Sullivan , „ Explozie în timpul preparării clorhidratului de benzenediazoniu-2-carboxilat ” , Journal of Chemical Education , vol. 48, nr . 6,1 st iunie 1971, p. 419 ( ISSN 0021-9584 , DOI 10.1021 / ed048p419.3 , citiți online )
- Logullo, Seitz și Friedman, „ Benzenediazonium-2-carboxilat și bifenilenă (Benzenediazoniu, o -carboxi- , hidroxid, sare interioară) ”, Org. Sintetizator. , vol. 48,1968, p. 12 ( DOI 10.15227 / orgsyn.048.0012 )
- Tadross, PM; Stoltz, BM, " O istorie cuprinzătoare a arinelor în sinteza totală a produselor naturale ", Chem. Rev. , vol. 112, nr . 6,2012, p. 3550–3577 ( PMID 22443517 , DOI 10.1021 / cr200478h )
- Hoye, TR; Baire, B.; Niu, D.; Willoughby, PH; Woods, BP Nature , 2012 , 490 , 208
- Campbell și Rees, „ Reactive intermediari. Partea I. Sinteza și oxidarea 1- și 2-aminobenzotriazolului ”, J. Chem. Soc. C , vol. 1969 n o 5,1969, p. 742–747 ( DOI 10.1039 / J39690000742 )
- Anslyn, EV; Dougherty, DA Chimie organică fizică modernă. University Science Books, 2006 .
- Diemer, V.; Begaut, M.; Leroux, FR; Colobert, F. Eur. J. Org. Chem. 2011 , 341
- Mizukoshi, Mikami și Uchiyama, „ Aryne Polymerization Eniting Directly Synthesis of Elusive Poly ( ortho- arilen) s ”, J. Am. Chem. Soc. , vol. 137, nr . 1,2015, p. 74–77 ( PMID 25459083 , DOI 10.1021 / ja5112207 )
- {{{title}}} , Org. Sintetizator. , col. „zbor. "
- " 1,2,3,4-Tetraphenylnaphthalene ", Sinteze organice , vol. 46,1966, p. 107 ( DOI 10.15227 / orgsyn.046.0107 )
- " Utilizarea 1,2,4,5-Tetrabromobenzenului ca echivalent 1,4-Nenzadiyne: Anti- și Syn-1,4,5,8-tetrahidroantracen 1,4: 5,8-diepoxizi ", Sinteze organice , zbor. 75,1998, p. 201 ( DOI 10.15227 / orgsyn.075.0201 )
- Sato, Y .; Tamura, T.; Mori, M. Angew. Chem. Int. Ed. 2004, 43 , 2436
- Buszek, KR; Brown, N.; Kuo, D. Org. Lett. 2009, 11 , 201
- Pellissier, H.; Santelli, M. Tetrahedron, 2003, 59 , 701
- Stevens, RV; Bisacchi, GS J. Org, Chem. 1982, 47 , 2396
- Guyot, M .; Molho, D. Tetrahedron Lett. 1973 , 1 4 , 3433
- Conversia m-Benzyne la o-Benzyne printr-o schimbare 1,2 a unui grup fenil. Blake, ME; Bartlett, KL; Jones, M. Jr. J. Am. Chem. Soc. 2003 , 125, 6485. DOI : 10.1021 / ja0213672
- O conversie p-Benzyne la m-Benzyne printr-o schimbare 1,2 a unui grup fenil. Finalizarea cascadei Benzyne, Polishchuk, AL; Bartlett, KL; Friedman, LA; Jones, M. Jr. J. Phys. Org. Chem. 2004 , Volumul 17, Numărul 9, Paginile 798 - 806. DOI : 10.1002 / poc.797
- Richard R. Jones și Robert G. Bergman, „ p-Benzyne. Generarea ca intermediar într-o reacție de izomerizare termică și dovezi de captare a structurii 1,4-benzenediil ”, J. Am. Chem. Soc. , vol. 94, n o 21972, p. 660–661 ( DOI 10.1021 / ja00757a071 )
- Clauberg, H.; Minsek, DW; Chen, P. J. Am. Chem. Soc. 1992 , 114 , 99.
- Blush, JA; Clauberg, H.; Kohn, DW; Minsek, DW; Zhang, X; Chen, P. Acc. Chem. Rez. 1992 , 25 , 385
- Chen, P. Angew. Chem. Int. Ed. Angl. 1996 , 35 , 1478.
- Stoermer și Kahlert, " Ueber das 1- und 2-Brom-cumaron ", Berichte der Deutschen Chemischen Gesellschaft , vol. 35, n o 21902, p. 1633–1640 ( DOI 10.1002 / cber.19020350286 )
- Wittig, G., Pieper, G. și Fuhrmann, G. (1940), Über die Bildung von Diphenyl aus Fluorbenzol und Phenyl-lithium (IV. Mitteil. Über Austauschreaktionen mit Phenyl-lithium). Berichte der deutschen chemischen Gesellschaft (Seria A și B), 73: 1193–1197. DOI : 10.1002 / cber.19400731113
- Phenyl-lithium, der Schlüssel zu einer neuen Chemie metallorganischer Verbindungen Georg Wittig Naturwissenschaften, 1942, Volumul 30, Numere 46-47, Pagini 696-703 DOI : 10.1007 / BF01489519
- Wittig, G. (1954), Fortschritte auf dem Gebiet der organischen Aniono-Chemie. Angewandte Chemie, 66: 10-17. DOI : 10.1002 / angel.19540660103
- rearanjare în reacția clorbenzen-1-C14 cu potasiu în mijlocul lui John D. Roberts, Howard E. Simmons Jr., LA Carlsmith, C. Wheaton Vaughan J. Am. Chem. Soc., 1953, 75 (13), pp. 3290-3291 DOI : 10.1021 / ja01109a523
- The Mechanism of Aminations of Halobenzenes John D. Roberts, Dorothy A. Semenow, Howard E. Simmons Jr., LA Carlsmith J. Am. Chem. Soc., 1956, 78 (3), pp. 601–611 DOI : 10.1021 / ja01584a024
- Orientare în aminații de halobenzeni substituiți John D. Roberts, C. Wheaton Vaughan, LA Carlsmith, Dorothy A. Semenow J. Am. Chem. Soc., 1956, 78 (3), pp. 611–614 DOI : 10.1021 / ja01584a025
- Metode moderne de arilare . Editat de Lutz Ackermann 2009 WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim ( ISBN 978-3-527-31937-4 )
- The Benzyne and Related Intermediates . H. Heaney Chem. Rev., 1962, 62 (2), pp. 81–97 DOI : 10.1021 / cr60216a001
- Wittig, G.; Pohmer, L. Angew. Chem. 1955 , 67 (13) , 348.
- Warmuth, R.; Yoon, Acc. Chem. Rez. 2001 , 34 , 96
- Generarea suprafeței și imagistica arinelor prin microscopie cu forță atomică, D. Pérez, E. Guitián, D. Peña, L. Gross, Nature Chemistry , 2015 , 7, 623
- Galm, Hager, Van Lanen și Ju, „ Antibioticele antitumorale: bleomicină, enediynes și mitomicină ”, Chemical Reviews , vol. 105, n o 2Februarie 2005, p. 739–58 ( PMID 15700963 , DOI 10.1021 / cr030117g )
- Kametani, T.; Ogasawara, KJ J. Chem. Soc., C 1967, 2208
- Ziua, JJ; McFadden, RM; Virgil, SC; Kolding, H.; Alleva, JL; Stoltz, BM Angew. Chem. Int. Ed. 2011, 50 , 6814.
- Soorukram, D.; Qu, T; Barrett, AGM, „ Reacții de cuplare cu patru componente ale benzinei: o sinteză totală concisă a dehidroaltenuenului B ”, Org. Lett. , vol. 10, nr . 17,2008, p. 3833–3835 ( PMID 18672878 , DOI 10.1021 / ol8015435 )
- ( fr ) Acest articol este preluat parțial sau în întregime din articolul din Wikipedia engleză intitulat „ Aryne ” ( vezi lista autorilor ) .
Vezi și tu
Un alt exemplu de utilizare a chimiei arinei: triciclobutabenzenul