Clorură de cloracetil
| Clorură de cloracetil | |||
 | |||
| Identificare | |||
|---|---|---|---|
| Numele IUPAC | Clorură de cloracetil | ||
| N o CAS | |||
| N o ECHA | 100.001.065 | ||
| N o EC | 201-171-6 | ||
| ZÂMBETE |
C (CCl) (= O) Cl , |
||
| InChI |
InChI: InChI = 1 / C2H2Cl2O / c3-1-2 (4) 5 / h1H2 |
||
| Aspect | Lichid incolor până la gălbui cu miros înțepător | ||
| Proprietăți chimice | |||
| Formula brută |
C 2 H 2 Cl 2 O [izomeri] |
||
| Masă molară | 112,943 ± 0,006 g / mol C 21,27%, H 1,78%, Cl 62,78%, O 14,17%, |
||
| Proprietăți fizice | |||
| T ° fuziune | −22,5 ° C | ||
| T ° fierbere | 105 ° C | ||
| Solubilitate | se descompune violent în apă | ||
| Masa volumică | 1,417 g · cm -3 ( 20 ° C ) | ||
| Punct de aprindere | > 100 ° C | ||
| Presiunea saturată a vaporilor |
25,3 mbar la 20 ° C 230 mbar la 65 ° C |
||
| Precauții | |||
| Directiva 67/548 / CEE | |||
 T  VS  NU Simboluri : T : Toxic C : Coroziv N : Periculos pentru mediu Fraze R : R14 : Reacționează violent cu apa. R29 : Contactul cu apa eliberează gaze toxice. R35 : Provoacă arsuri severe. R50 : Foarte toxic pentru organismele acvatice. R23 / 24/25 : Toxic prin inhalare, în contact cu pielea și în caz de înghițire. R48 / 23 : Toxic: pericol de deteriorare gravă a sănătății prin expunere prelungită prin inhalare. Fraze S : S7 : Păstrați recipientul bine închis. S8 : Păstrați recipientul departe de umiditate. S26 : În caz de contact cu ochii, clătiți imediat cu multă apă și consultați un specialist. S45 : În caz de accident sau dacă vă simțiți rău, solicitați imediat sfatul medicului (arătați eticheta acolo unde este posibil). S61 : Evitați eliberarea în mediu. Consultați instrucțiunile speciale / fișa cu date de siguranță. (S1 / 2) : A se păstra închis și la îndemâna copiilor. S36 / 37/39 : Purtați îmbrăcăminte de protecție adecvată, mănuși și protecție pentru ochi / față. Fraze R : 14, 23/24/25, 29, 35, 48/23, 50, Fraze S : (1/2), 7, 8, 26, 36/37/39, 45, 61, |
|||
| Transport | |||
668 : material foarte toxic și coroziv Număr ONU : 1752 : CLORURA DE CLORACETIL Clasa: 6.1 Etichete: 6.1 : Substanțe toxice 8 : Substanțe corozive   |
|||
| Ecotoxicologie | |||
| DL 50 |
220 mg (șoarece, oral ) 32 mg · kg -1 (șoarece, iv ) |
||
| CL 50 | 1300 ppm / 2H (mouse, inhalare) | ||
| LogP | -0.220 | ||
| Unități de SI și STP, cu excepția cazului în care se prevede altfel. | |||
Clorura de cloracetil este un compus din familia Clorurile de acil clorurate . Un compus bifuncțional, este interesant ca „element de construcție” chimic, dar cu o dublă reactivitate, se comportă violent în diferite circumstanțe.
Proprietăți
Clorura de cloracetil este un lichid inflamabil foarte scăzut (punctul de aprindere peste 100 ° C ), care se descompune violent în apă. Eliberează fum în prezența umidității în aer. Se descompune la încălzire, în special clorură de hidrogen , clor , fosgen și dioxine . Reacționează violent cu alcooli , apă, baze sau metale alcaline și pulberi metalice.
Sinteză
La scară industrială, este produs de carbonilare de diclormetan , oxidarea de 1,1-dicloretenă , sau prin adăugarea de clor la cetenă . Poate fi preparat și din acid cloracetic și clorură de tionil , pentaclorură de fosfor sau fosgen .
Reacții
Clorura de cloracetil este bifuncțională: partea clorurii de acil formează cu ușurință esteri și amide , în timp ce cealaltă parte a moleculei este capabilă să formeze alte tipuri de legături, de exemplu cu aminele . În exemplul următor, clorura de cloracetil este utilizată în sinteza lidocainei , formând o amidă prin reacție cu 2,6-xilidină (2,6-dimetilanilină):

Aplicații
Datorită reactivității sale duble, clorura de cloracetil este utilizată în multe sinteze organice. Este utilizat în special ca intermediar în producerea alaclorului și butaclorului . Clorura de cloracetil este, de asemenea, utilizată în producția de clorură de fenacil , un alt intermediar chimic, utilizat și ca gaz lacrimogen . Clorura de fenacil este sintetizată prin acilarea Friedel-Crafts pe benzen , catalizată de triclorură de aluminiu :
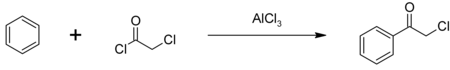
Precauții
La fel ca majoritatea clorurilor de acil, reacționează cu alți compuși protici, cum ar fi aminele, alcoolii sau apa, pentru a produce clorură de hidrogen și a-l face gaz lacrimogen .
Note și referințe
- calculate în masă moleculară de „ masele atomice ale elementelor 2007 “ pe www.chem.qmul.ac.uk .
- Intrarea „Clorură de cloracetil” în baza de date chimice GESTIS a IFA (organism german responsabil cu securitatea și sănătatea în muncă) ( germană , engleză ), accesat la 13/11/2010 (JavaScript este necesar)
- Gigiena i Sanitariya. Pentru traducere în limba engleză, consultați HYSAAV. Zbor. 54 (2), pag. 90, 1989.
- Comandamentul cercetării și dezvoltării armamentului SUA, Laboratorul de sisteme chimice, NIOSH Exchange Chemicals. Zbor. NX # 04538
- „Documentarea valorilor limită prag și indicii de expunere biologică”, ediția a 5-a, Cincinnati, OH, Conferința americană a igienilor industriali guvernamentali, Inc., 1986Vol. 5, pag. 123 (89), 1986.
- (în) „ Clorură cloracetil ” pe ChemIDplus , accesat la 13/11/2010
- (în) Paul R. Worsham, cap. 15 „Derivați halogenați” în Zoeller, Joseph R; Agreda, VH, eds., Acetic acid și derivații săi , New York, M. Dekker,1993, Extras Google Books ( ISBN 0-8247-8792-7 , citit online ) , p. 288–298
- Robert H. Baker și Frederick G. Bordwell, acetat de terț-butil , Org. Sintetizator. , col. „zbor. 3 ",1955
- (în) TJ Reilly, „ The Preparation of Lidocaine ” , J. Chem. Ed. , Vol. 76, nr . 11,1999, p. 1557 ( DOI 10.1021 / ed076p1557 , citiți online )
- Nathan Levin și Walter H. Hartung, ω-Chloroisonitrosoacetophenone , Org. Sintetizator. , col. „zbor. 3 ",1955, p. 191
- ( FR ) Acest articol este preluat parțial sau în întregime din limba engleză Wikipedia articol intitulat „ clorură de cloracetil “ ( a se vedea lista de autori ) .