Trifluorură de clor
| Trifluorură de clor | |||
|
|||
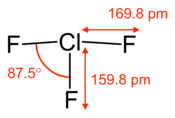
| Structura trifluorurii de clor. | |||
| Identificare | |||
|---|---|---|---|
| N o CAS | |||
| N o ECHA | 100.029.301 | ||
| N o EC | 232-230-4 | ||
| N o RTECS | FO2800000 | ||
| PubChem | 24637 | ||
| ChEBI | 30123 | ||
| ZÂMBETE |
FCl (F) F , |
||
| InChI |
Std. InChI: InChI = 1S / ClF3 / c2-1 (3) 4 Std. InChIKey: JOHWNGGYGAVMGU-UHFFFAOYSA-N |
||
| Aspect | Gaz sau lichid gălbui | ||
| Proprietăți chimice | |||
| Formula brută | ClF 3 | ||
| Masă molară | 92,448 ± 0,002 g / mol Cl 38,35%, F 61,65%, |
||
| Momentul dipolar | 0,6 ± 0,1 D | ||
| Proprietăți fizice | |||
| T ° fuziune | −76,31 ° C | ||
| T ° fierbere | 11,8 ° C | ||
| Masa volumică | 3,57 kg · m -3 la 0 ° C și 101,3 kPa | ||
| Presiunea saturată a vaporilor | 141,9 kPa la 20 ° C | ||
| Punct critic | 174,0 ° C ; 5,78 MPa ; 0,548 g · cm -3 | ||
| Punct triplu | −76,3 ° C | ||
| Termochimie | |||
| Δ vap H ° | 27,53 kJ · mol -1 ( 1 atm , 11,75 ° C ) | ||
| Precauții | |||
| SGH | |||
    Pericol H270, H280, H314, H330, H370, H372, H400, H270 : Poate provoca sau intensifica focul; oxidant H280 : Conține gaze sub presiune; poate exploda dacă este încălzit H314 : Provoacă arsuri severe ale pielii și leziuni oculare H330 : Fatal dacă este inhalat H370 : Provoacă leziuni ale organelor (sau enumeră toate organele afectate, dacă sunt cunoscute) (indicați calea de expunere dacă se dovedește în mod concludent că nu există altă cale de expunere duce la același pericol) H372 : risc demonstrat de deteriorare gravă a organelor (indicați toate organele afectate, dacă sunt cunoscute) în urma expunerii repetate sau prelungite (indicați calea de expunere dacă se dovedește în mod concludent că nicio altă cale de expunere nu cauzează același pericol) H400 : Foarte toxic pentru organismele acvatice |
|||
| Transport | |||
265 : gaz otrăvitor și oxidant (promovează focul) Număr ONU : 1749 : TRIFLUORURĂ DE CLOR Clasa: 2.3 Etichete: 2.3 : Gazele toxice (corespunde grupurilor desemnate de un T capital, adică T, TF, TC, TO, TFC și TOC). 5.1 : Substanțe oxidante 8 : Substanțe corozive Ambalare: -    |
|||
| Unități de SI și STP, cu excepția cazului în care se prevede altfel. | |||
Trifluorura de clor este un interhalogenați cu formula CLF 3. Este un gaz incolor, foarte oxidant și extrem de reactiv, coroziv și toxic, care se condensează într-un lichid galben verzui. Cel mai adesea se găsește pe piață sub forma sa lichidă presurizată la temperatura camerei. Este utilizat în principal în fazele de curățare și pentru gravarea chimică în industria semiconductoarelor și în alte procese industriale. Este utilizat în special în ciclul combustibilului nuclear , unde permite conversia compușilor de uraniu fluorurat nevolatil în hexafluorură de uraniu UF 6, un compus cu proprietăți fizice interesante din punctul de vedere al proceselor de îmbogățire a uraniului :
Utilizarea acestuia ca oxidant pentru propulsia spațială a fost acum abandonată, având în vedere riscurile reale pentru echipamente și pentru echipaje; pe de altă parte, este materia primă pentru sinteza pentafluorurii de clor ClF 5, un propulsor folosit uneori, cel mai adesea cu hidrazină , pentru propulsia anumitor rachete.
Pregătirea și proprietățile
Trifluorura de clor a fost preparată pentru prima dată în 1931 de doi chimiști germani, O. Ruff și H. Kug, prin reacția fluorului F 2pe clor Cl 2, care a produs și monofluorură de clor ClF, separată de trifluorură prin distilare:
3 F 2+ Cl 2→ 2 ClF 3Molecula ClF 3are o formă de T, pe care teoria VSEPR o explică bine:
- atomul de clor se află în centrul moleculei
- una dintre cele trei poziții ecuatoriale este ocupată de un atom de fluor legat de clor printr-o legătură covalentă
- celelalte două poziții ecuatoriale sunt ocupate fiecare de un dublet neobligatoriu
- cele două poziții axiale sunt ocupate fiecare de un atom de fluor care formează, cu atomul central de clor , o legătură cu trei centri și patru electroni , în mod normal rectilinii, dar aici puțin pliați sub efectul celor două dublete care nu se leagă.
Prin urmare, cei trei atomi de fluor sunt legați de clor prin legături de tip diferit, ceea ce duce la lungimi diferite ale legăturii:
- ~ 159,8 µm pentru legătura ecuatorială ( covalentă ) Cl-F
- ~ 169,8 pm pentru legăturile axiale Cl-F (care participă la legătura 3c-4e )
Pure trifluorura de clor este de până stabil la 180 ° C , dar se descompune în F 2și Cl 2 peste această temperatură.
Este un oxidant foarte energic, precum și un agent de fluorurare. Foarte reactiv cu majoritatea materiilor organice și minerale, este posibil să declanșeze arderea spontană, uneori exploziv. Metalul da , de obicei , cloruri și fluoruri , fosfor dă fosfor triclorură pCI 3și pentafluorură de fosfor PF 5, în timp ce sulful dă diclorură de sulf SCl 2precum și tetrafluorură de sulf SF 4. La temperatura camerei, hidrogen sulfurat H 2 Sexplodează la contactul cu trifluorură de clor, care de asemenea se hidrolizează violent la contactul cu apa H 2 Oprin eliberarea unui set de compuși periculoși, începând cu fluorură de hidrogen HF.
Riscuri
Deoarece trifluorura de clor este mai oxidantă decât oxigenul în sine, poate coroda ceramica, precum și diverse materiale pe bază de oxizi anorganici despre care se crede adesea că sunt incombustibili, inclusiv betonul. Orice lucru care intră în contact cu ClF 3 trebuie selectate cu atenție și curățate de orice impurități care ar putea declanșa arderea explozivă.
În contact cu pielea, trifluorura de clor poate declanșa arderea țesutului viu dacă este în cantitate suficientă. Se hidrolizează atacând celulele, într-o reacție foarte exotermă care provoacă arsuri atât termice, cât și chimice, în special de acidul fluorhidric eliberat în țesuturi prin această hidroliză. În plus, acest acid este toxic, astfel încât otrăvirea metabolică se adaugă degradărilor fiziologice cauzate de natura sa acidă.
Note și referințe
- (în) David R. Lide, Manual de chimie și fizică , Boca Raton, CRC, 16 iunie 2008, 89 th ed. , 2736 p. ( ISBN 978-1-4200-6679-1 și 1-4200-6679-X ) , p. 9-50.
- calculate în masă moleculară de „ masele atomice ale elementelor 2007 “ pe www.chem.qmul.ac.uk .
- Intrarea „Clorotrifluorură” în baza de date chimice GESTIS a IFA (organism german responsabil cu securitatea și sănătatea în muncă) ( germană , engleză ), accesat la 27 mai 2018 (este necesar JavaScript)
- (în) David R. Lide, Manualul de chimie și fizică al CRC, CRC Press, 2009, Ediția a 90- a . , 2804 p. , Hardcover ( ISBN 978-1-4200-9084-0 ).
- (în) Hitoshi Habuka Takahiro Sukenobu, Hideyuki Koda, Takashi Takeuchi și Masahiko Aihara, „ Silicon Etch Rate Using Chlorine Trifluoride ” , Journal of the Electrochemical Society , Vol. 151, nr . 11,2004, G783 - G787 ( DOI 10.1149 / 1.1806391 ).
- Brevetul SUA 5849092 „Procedeu de curățare a camerei de trifluorură de clor” .
- Brevetul SUA 6034016 "Metoda de regenerare a catalizatorilor halogenați ai acidului Lewis" .
- ( BEST) Board on Environmental Studies and Toxicology , Acute Exposure Guideline Levels for Selected Airborne Chemicals: Volume 5 http: //books.nap.edu/catalog.php?record_id=11774 (citare la National Academies Press) , Washington, National Academies Press ,2006, 267 p. , buzunar ( ISBN 978-0-309-10358-9 , LCCN 2002275572 ) , p. 40.
- în special anumite rachete balistice intercontinentale , care utilizează în general propulsori lichizi cu câteva excepții, cum ar fi, se pare, noul israelian Jericho-3.
- (în) Otto Ruff , H. Krug, " Über ein neues Chlorfluorid CIF- 3 " , Zeitschrift für anorganische und allgemeine Chemie , vol. 190, n o 1,1931, p. 602–608 ( DOI 10.1002 / zaac.19301900127 ).