Pentaclorură de antimoniu
| Pentaclorură de antimoniu | |||||
| |||||
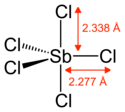
| Structura pentaclorurii de antimoniu | |||||
| Identificare | |||||
|---|---|---|---|---|---|
| Sinonime |
clorură de antimoniu ( V ) |
||||
| N o CAS | |||||
| N o ECHA | 100.028.729 | ||||
| N o EC | 231-601-8 | ||||
| N o RTECS | CC5075000 | ||||
| PubChem | 24294 | ||||
| ZÂMBETE |
Cl [Sb] (Cl) (Cl) (Cl) Cl , |
||||
| InChI |
Std. InChI: InChI = 1S / 5ClH.Sb / h5 * 1H; / q ;;;;; + 5 / p-5 Std. InChIKey: VMPVEPPRYRXYNP-UHFFFAOYSA-I |
||||
| Aspect | lichid galben cu miros înțepător | ||||
| Proprietăți chimice | |||||
| Formula brută | Sb Cl 5 | ||||
| Masă molară | 299,025 ± 0,011 g / mol Cl 59,28%, Sb 40,72%, |
||||
| Proprietăți fizice | |||||
| T ° fuziune | 3,5 ° C | ||||
| Solubilitate | se descompune violent la contactul cu apa | ||||
| Masa volumică | 2,358 g · cm -3 la 16 ° C | ||||
| Presiunea saturată a vaporilor | 110 Pa la 20 ° C | ||||
| Precauții | |||||
| SGH | |||||
  Pericol H314, H411, P273, P280, P310, P305 + P351 + P338, H314 : Provoacă arsuri severe ale pielii și leziuni oculare H411 : Toxic pentru viața acvatică cu efecte de lungă durată P273 : Evitați eliberarea în mediu. P280 : Purtați mănuși de protecție / îmbrăcăminte de protecție / protecție a ochilor / protecție a feței. P310 : Apelați imediat un CENTRU DE TOXICOLOGIE sau un medic / medic. P305 + P351 + P338 : În cazul ochilor: clătiți cu atenție cu apă timp de câteva minute. Scoateți lentilele de contact dacă victima le poartă și acestea pot fi îndepărtate cu ușurință. Continuați să clătiți. |
|||||
| Transport | |||||
Lichid:
X80 : material coroziv sau material care prezintă un grad minor de corozivitate care reacționează periculos cu apa) Număr ONU : 1730 : ANTIMONY PENTACHLORIDE LIQUID Clasa: 8 Etichetă: 8 : Substanțe corozive Ambalare: Grup de ambalare II : substanțe medii periculoase;  Soluţie:
80 : material coroziv sau material care prezintă un grad minor de corozivitate Număr ONU : 1731 : ANTIMONY PENTACHLORIDE SOLUTION Clasa: 8 Etichetă: 8 : Substanțe corozive Ambalare: Grupa de ambalare II / III : substanțe cu pericol mediu / scăzut.  |
|||||
| Unități de SI și STP, cu excepția cazului în care se prevede altfel. | |||||
Pentaclorură de antimoniu este un compus chimic cu formula SbCl 5. Este un lichid incolor cu miros înțepător, care fumează la contactul cu aerul, în general colorat în galben prin impuritățile sale. Este o substanță foarte oxidantă și foarte corozivă care hidrolizează violent, eliberând acid clorhidric la contactul cu apa. Se carbonizes materiale plastice nefluorurate. Molecula sa în stare gazoasă are o geometrie bipiramidală trigonală .
Pentaclorura de antimoniu se obține prin trecerea clorului Cl 2în SbCl 3 triclorură de antimoniu decolorare:
SbCl 3+ Cl 2→ SbCl 5.În prezența unor cantități mici de apă, forma de hidrați pentaclorură de antimoniu : monohidrat SbCl 5 · H 2 Oși SbCl 5 4H 2 O tetrahidrat. În prezența mai multă apă, se hidrolizează violent, formând oxicloruri de antimoniu, cum ar fi acidul antimonic (de) H 3 SbO 4cu eliberare de acid clorhidric HCI:
SbCl 5+ 4 H 2 O→ H 3 SbO 4 (de) + 5 HCI .Această reacție dispare în cazul unui exces mare de cloruri datorită formării complexelor ionice hexaclorantimonat [SbCl 6] - :
SbCl 5+ Cl - → [SbCl 6] - .Acest compus formează aducti cu multe baze Lewis . Este utilizat drept catalizator pentru polimerizarea și pentru clorurarea a compușilor organici .
Note și referințe
- Intrarea „Pentaclorură de antimoniu” în baza de date chimice GESTIS a IFA (organism german responsabil cu securitatea și sănătatea în muncă) ( germană , engleză ), accesat la 12 iunie 2018 (este necesar JavaScript)
- calculate în masă moleculară de „ masele atomice ale elementelor 2007 “ pe www.chem.qmul.ac.uk .
- (în) Neil G. Connelly și William E. Geiger * ‡ , „ Chemical Redox Agents for Organometallic Chemistry ” , Chemical Reviews , Vol. 96, n o 2 28 martie 1996, p. 877-910 ( PMID 11848774 , DOI 10.1021 / cr940053x , citiți online )
- (în) Norman N. Greenwood și Alan Earnshaw, Chimia elementelor , ediția 2 e , Butterworth-Heinemann, 1997. ( ISBN 0-08-037941-9 )