Sulfură de potasiu
| Sulfură de potasiu | |
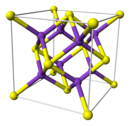  S 2– ioni (în galben) și ioni K + (în violet) |
|
| Identificare | |
|---|---|
| Numele IUPAC | sulfură de potasiu |
| Sinonime |
monosulfură de dipotasiu |
| N o CAS | |
| N o ECHA | 100.013.816 |
| N o EC | 215-197-0 |
| N o RTECS | TT6000000 |
| Codul ATC | |
| InChI |
InChI: InChI = 1 / 2K.S / q2 * + 1; -2 InChIKey: DPLVEEXVKBWGHE-UHFFFAOYAJ Std. InChI: InChI = 1S / 2K.S / q2 * + 1; -2 Std. InChIKey: DPLVEEXVKBWGHE-UHFFFAOYSA-N |
| Aspect | incolor, pur, galben-maroniu |
| Proprietăți chimice | |
| Formula brută |
K 2 S [izomeri] |
| Masă molară | 110,262 ± 0,005 g / mol K 70,92%, S 29,08%, |
| Proprietăți fizice | |
| T ° fuziune | 840 ° C |
| T ° fierbere | Dec. |
| Solubilitate | reacție cu apă → KHS + KOH solubil în etanol , glicerol |
| Masa volumică | 1,81 g · cm -3 |
| Cristalografie | |
| Structura tipică | anti fluorit |
| Precauții | |
| Directiva 67/548 / CEE | |
 VS  NU Simboluri : C : Coroziv N : Periculos pentru mediu Fraze R : R31 : Contactul cu acizii eliberează gaze toxice. R34 : Provoacă arsuri. R50 : Foarte toxic pentru organismele acvatice. Fraze S : S26 : În caz de contact cu ochii, clătiți imediat cu multă apă și solicitați sfatul medicului. S45 : În caz de accident sau dacă vă simțiți rău, solicitați imediat sfatul medicului (arătați eticheta acolo unde este posibil). S61 : Evitați eliberarea în mediu. Consultați instrucțiunile speciale / fișa cu date de siguranță. Expresii R : 31, 34, 50, Fraze S : 26, 45, 61, |
|
| Unități de SI și STP, cu excepția cazului în care se prevede altfel. | |
Sulfura de potasiu este un compus anorganic și un solid ionic cu formula moleculară K 2 S. Solidul incolor nu este întâlnit în mod normal , în condiții naturale , deoarece reacționează rapid și ireversibil cu apă , pentru a forma hidrogenul sulfurat din potasiu (KHS) și hidroxid de potasiu ( KOH). În plus, anionul sulfurat se oxidează foarte rapid la contactul cu oxigenul atmosferic și se transformă în anionul sulfat .
Structura
Sulfura de potasiu adoptă o structură antifluorită, ceea ce înseamnă că ionii K + mici ocupă siturile tetraedrice ale anionilor F - în fluorit, iar centrele S 2– mai mari ocupă cele 8 locuri de coordonare ale Ca 2+ . Li 2 S, Na 2 S și Rb 2 S cristalizează în același mod.
Sinteza și reacțiile
K 2 S rezultă din combinația de potasiu și sulf . În laborator, poate fi obținut prin reacția sulfului elementar cu potasiu metalic dizolvat în amoniac lichid anhidru . Cu toate acestea, acest tip de sinteză nu este comun din cauza măsurilor de siguranță necesare.
Poate fi produs industrial prin reducerea termosulfatului (TSR) prin încălzirea sulfatului de potasiu , K 2 SO 4 cu carbon :
K 2 SO 4 + 2 C → K 2 S + 2 CO 2K 2 SO 4 + 4 C → K 2 S + 4 COAceastă sare conține anioni S 2− care sunt foarte de bază și care hidrolizează complet conform următoarei ecuații:
S 2– + H 2 O → HS - + OH -K 2 S + H 2 O → KHS + KOHAtunci când este utilizată pentru a induce precipitarea sulfurilor metalice insolubile ( metale de tranziție și metale grele ), această soluție de ioni HS - și OH - se comportă ca o sursă de S 2– . Alte sulfuri de metale alcaline se comportă în mod similar.
Utilizare în artificii
Sulfura de potasiu se poate forma atunci când se arde pulbere neagră care conține exces de sulf . Este un intermediar important în multe efecte pirotehnice , cum ar fi Senko Hanabi și unele formulări de sclipici.
Utilizare în bijuterii
Prin formarea sulfurii de argint (Ag 2 S) într-un film foarte subțire, poate da tot felul de nuanțe la suprafața obiectelor de argint (portocaliu, roșu, albastru, până la negru). Acest fenomen optic se datorează interferenței în lama subțire, de asemenea, responsabilă pentru apariția memoriilor pe suprafața peliculei subțiri de ulei care plutesc pe suprafața apei. Astfel de pelicule de oxid de argint (Ag 2 O) cauza , de asemenea reflecții moire pe suprafața oxidată argintărie .
Note și referințe
- (fr) Acest articol este preluat parțial sau în totalitate din articolul din Wikipedia engleză intitulat „ Sulfură de potasiu ” ( vezi lista autorilor ) .
- calculate în masă moleculară de „ masele atomice ale elementelor 2007 “ pe www.chem.qmul.ac.uk .
- „ Vechiul sistem de semnalizare a substanțelor periculoase, învechit din 2010 și 2015, link către actualizare ” ( Arhivă • Wikiwix • Archive.is • Google • Ce trebuie făcut? ) (Accesat pe 5 martie 2021 )
- Holleman, AF; Wiberg, E. (2001). „Chimie anorganică” Academic Press: San Diego, ( ISBN 0-12-352651-5 ) .
- Shimizu, Takeo. „Artificii: artă, știință și tehnică”. Publicații Pyrotechnica : Austin, 1981. ( ISBN 0-929388-05-4 ) .