Reacție de deshidratare
În chimie, o reacție de deshidratare este o reacție chimică în care reactivul de pornire pierde un atom de hidrogen și o grupare hidroxil sau o moleculă de apă , inversul reacției de hidratare . Reacțiile de deshidratare sunt o subcategorie a reacțiilor de eliminare .
Întrucât gruparea hidroxil (–OH) este un grup rău părăsitor , având un acid Brønsted ca catalizator promovează protonarea grupului, transformându-l în –OH 2 + , cu atât este mai bine părăsirea grupului. Agenții de deshidratare utilizați în mod obișnuit în sinteza organică sunt acidul sulfuric concentrat , acidul fosforic concentrat , oxidul de aluminiu fierbinte și ceramica fierbinte.
O reacție de condensare poate elibera uneori o moleculă de apă ca produs. Aceasta este uneori denumită sinteză prin deshidratare. Acesta este, de exemplu, cazul a două monozaharide , cum ar fi glucoza sau fructoza , care se pot condensa într-o dizaharidă ( zaharoză ) prin sinteză prin deshidratare. Reacția inversă este apoi hidroliza , apa recombinându-se cu cele două grupări hidroxil, dizaharida fiind reconvertită în două monozaharide.
Exemple
În sinteza organică, există multe exemple de reacții de deshidratare, de exemplu, deshidratarea alcoolilor sau a zaharurilor.
| Reacții de deshidratare | ||
| Reacţie | Ecuaţie | Exemple |
|---|---|---|
| Conversia alcoolilor în eteri | 2 R-OH → ROR + H 2 O | |
| Conversia alcoolilor în alchene | R-CH 2- CHOH-R → R-CH = CH-R + H 2 O | de exemplu, conversia glicerolului în acroleină :
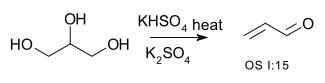 sau deshidratarea 2-metil-1-ciclohexanolului în (în principal) 1-metilciclohexenă :  |
| Conversia acizilor carboxilici în anhidridele acide | 2 RCOOH → (RCO) 2 O + H 2 O | |
| Conversia amidelor în nitrili | RCONH 2 → R-CN + H 2 O | |
| Rearanjare dienol-benzen | 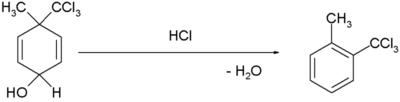 |
|
Note și referințe
- Sinteze organice OS I: 15 Link
- Deshidratarea 2-metil-1-ciclohexanolului: rezultate noi dintr-un experiment popular de laborator universitar J. Brent Friesen și Robert Schretzman J. Chem. Educ., 2011, 88 (8), pp. 1141–1147 DOI : 10.1021 / ed900049b
- H. Plieninger și Gunda Keilich, „ Die Dienol-Benzol-Umlagerung ”, Angew. Chem. , vol. 68, nr . 19,1956, p. 618–618 ( DOI 10.1002 / angel.19560681914 )
- Margaret Jevnik Gentles, Jane B. Moss, Hershel L. Herzog și EB Hershberg, „ Rearanjarea Dienol-Benzen. Some Chemistry of 1,4-Androstadiene-3,17-dione ”, J. Am. Chem. Soc. , vol. 80, nr . 14,1958, p. 3702–3705 ( DOI 10.1021 / ja01547a058 )
- ( fr ) Acest articol este preluat parțial sau în întregime din articolul Wikipedia din limba engleză intitulat „ Dehydration reaction ” (a se vedea lista autorilor ) .