Organomagneziu
Un organomagneziu este un compus organic cu o legătură carbon - magneziu . Aceasta este o familie importantă de compuși organometalici în sinteza organică, deoarece include reactivi Grignard , care sunt organomagnezii amestecați sub forma R - Mg X , unde R este un lanț de carbon și X este un halogen , în general brom. Sau clor , uneori iod - fluorul nu este utilizat în general datorită prea mică polarizabilitatea de difluor F 2. Acești reactivi sunt utilizate pe scară largă în industrie și descoperirea lor la sfârșitul XIX - lea secol de chimistul francez Victor Grignard a permis pentru a obține Premiul Nobel pentru chimie în 1912 , deoarece acestea pot lega o mare varietate de blocuri pentru a moleculelor organice.
În plus față de reactivi Grignard, organomagnezieni includ molecule , cum ar fi dimetilmagneziu (CH 3 ) 2 Mg, Dibutilmagnetiu (CH 3 CH 2 CH 2 CH 2 ) 2 Mgsau antracen-magneziu .
Caracter organometalic al R - Mg - X
Carbonul are un electronegativitate puternic: . Și observăm și asta . Acest fapt fizic impune deci polarizarea legăturii C - M: C —M . Observăm o inversare a polarității legăturilor clasice de carbon: într-un organometalic, carbonul poartă o sarcină (acest carbon se numește carbanion), în plus această legătură este ionică de 35%, ceea ce va permite prin reacție cu, de exemplu, o halogenură alchil ( R —X ) creând o legătură carbon-carbon .
Organomagneziile sunt una dintre cele mai puternice baze Brönsted din chimia organică cu un pKa de ordinul 40 la 60. R-Mg-X este un nucleofil puternic.
Sinteza organomagneziului
Datorită bazicității lor extreme, compușii organomagneziu nu există în mod natural. Rezultatele generale ale sintezei sunt următoarele:
Mod de operare
Sinteza de organomagneziu este delicat: a mediului de reacție trebuie să fie anhidru, datorită proprietăților produsului dorit; reacția este puternic exotermă și solventul este volatil și inflamabil. Manipularea necorespunzătoare are ca rezultat și crearea unui produs parazit - numit „ cuplaj Wurtz ”.
Materiale necesare :
- Minge tricolor;
- Pâlnie de turnare izobarică;
- Condensator de reflux;
- Păstrează CaCl 2 (sau lucrează sub atmosferă inertă);
- Agitator magnetic cu încălzire;
- Bărci de magneziu;
- Dietil eter sau THF anhidru;
- Derivat halogenat;
- Baie de apă apoi apă rece.
Mod de operare
- Efectuați un ansamblu de adiție cu reflux, cu protecție a mediului de reacție împotriva umidității atmosferice și prin plasarea unei bare magnetice ovoide în balonul cu trei gâturi.
- Așezați așchii de magneziu, care au fost activați anterior în cuptor, în tricol. Acoperiți-le cu câțiva cm 3 de eter etilic anhidru. Adăugați un mic cristal de diodă.
- Condiționați pâlnia de turnare cu soluția derivatului halogenat în eter etilic anhidru și opriți-o cu un dop de sticlă.
- Se toarnă câteva picături din soluția de halogenură pe așchii de magneziu, se așteaptă câteva minute pentru observarea unei decolorări care apare în mediul de reacție.
- Când culoarea iodului a dispărut în mediul de reacție, încălziți într-o baie de apă pentru a seta un reflux și turnați halogenura încet și picătură cu picătură, amestecând magnetic.
- Odată ce adăugarea este completă, încălziți mediul de reacție la reflux, astfel încât să obțineți o reacție completă.
Comentarii
Pentru a preveni apariția unei cuplări Würtz între organomagneziul sintetizat și halogenură. De la începutul reacției, eterul fierbe: refluxul servește la condensarea vaporilor de eter care curg în balon; refluxul trebuie, de asemenea, menținut foarte scăzut, pentru a nu crea reacția parazitară menționată mai sus. Nu este necesar să se încălzească pe tot parcursul manipulării, deoarece reacția este foarte exotermă .
Soluția obținută în cele din urmă este de o culoare cenușie destul de deschisă, în general.
Solvent
Eterul joacă un rol dublu aici, solvatează organomagneziul format și îl stabilizează, organomagneziul este aici un acid Lewis, solventul joacă aici rolul bazei Lewis , astfel dubletele de oxigen care nu se leagă merg să stabilizeze centrul reactiv al magneziu . Este posibil, de exemplu, să se utilizeze dietil eter sau THF - tetrahidrofuran , cf. figura de mai jos.

Mediul în care se scaldă organomagneziul trebuie să fie complet anhidru: reacția apă / RMgX este plină de viață.
Reactivitatea organomagneziului
Reacții asupra compușilor organici obișnuiți
Pe apaReacția organomagneziilor asupra apei este foarte vie (este o reacție acid-bazică : p K a (RH / R-) = 50) și exotermă. Acesta este motivul pentru care modul de operare necesită deshidratarea totală a aerului din sticlărie, precum și a suprafețelor și a solvenților. Cu excepția cazurilor speciale, această reacție este considerată parazită și duce la distrugerea organomagneziu.
Reacția organomagneziului asupra apei este următoarea:
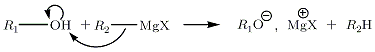 Cu acizi carboxilici
Cu acizi carboxilici
 Cu amine
Cu amine
 Cu alchine terminale
Cu alchine terminale

Reacții de substituție nucleofilă
Înlocuirea nucleofilă, exemplu de I 2Propunem substituția nucleofilă a RMgX pe I 2 (polaritatea acestei molecule este indusă).
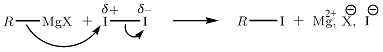 Substituție nucleofilă cu derivați halogenați
Substituție nucleofilă cu derivați halogenați
Derivat halogenat: mecanism R'-X: SN2
R-MgX + R'-X -> RR '+ MgX2
Notă: funcționează bine cu RI și Ar-CH2X deoarece sunt stabilizate prin efect inductiv pentru RI și mezomer pentru Ar-CH2X
Reacția asupra epoxidelorMecanism: SN2
În eter:
R ---- Mg ---- X + O (CH2) 2 (ciclu) → R-CH2-CH2-O-Mg-X
Apoi H3O + hidroliza acidă:
R-CH2-CH2-O-Mg-X + H + → R-CH2-CH2-OH + MgX +
Reacții de adiție nucleofilă ...
... pe aldehide și cetone- Pe aldehide :

Reacția dintre organomagnezici și aldehide conduce la formarea unui alcool secundar, în cazul în care R 1 și R 2 Lanțurile conțin cel puțin un atom de carbon. Dacă carbonul suport al grupei finale de alcool este asimetric, adică dacă cele două lanțuri R sunt diferite, produsul va fi compus din cei doi izomeri cu configurație R și S.
- Pe cetone :

Această reacție duce la crearea unui alcool terțiar. În ceea ce privește aldehidele, dacă carbonul format este asimetric, se obține un amestec R / S 50/50; astfel, nu există stereoselectivitate. Un studiu al mecanismului de reacție arată că, de fapt, există un intermediar ciclic:

- Caz special al sintezei unui alcool primar :
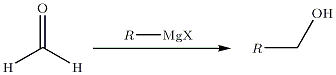 ... pe esteri
... pe esteri
Reacția este similară cu reacția pe o cetonă. După hidroliză, obținem hemiacetalul într-un mod intermediar ;
Acest lucru este instabil, suferă o eliminare care duce la o cetonă. Organomagneziul prezent va reacționa chimioselectiv cu cetona înainte de ester, care este mai puțin reactiv deoarece nucleul de carbon al carbonilului său este oarecum mascat de electronii care nu se leagă ai oxigenului legat de o singură legătură. Prin urmare, evaluarea generală a reacției duce la formarea unui alcool terțiar, fără posibilitatea izolării cetonei intermediare.
... pe cloruri de acilReacția este similară cu reacția pe o cetonă, dar mai rapidă, deoarece nucleul de carbon legat de clor prezintă o sarcină pozitivă mai atractivă pentru radicalul organomagneziu.
R ---- Mg ---- X + R'-CO-Cl → R'-CO-R + Cl-Mg-X
Prin urmare, reacția duce la formarea unei cetone izolabile dacă nu există prea mult organomagneziu. Această cetonă instabilă va reacționa cu agentul organomagneziu care se află în mediul de reacție în conformitate cu următoarea reacție: R'-CO-R + RMgX → R-R'COMgX-R și apoi sub acțiunea H2O obținem un alcool terțiar. Dacă vrem să ne oprim în etapa cetonică, trebuie să operăm la -65 ° C
... pe CO 2
Folosirea dioxidului de carbon sub formă de gheață uscată . Reacția la -40 ° C duce la formarea unui acid carboxilic R-COOH.
Note și referințe
- Victor Grignard , „ Despre unele noi combinații organometalice de magneziu și aplicarea lor la sinteza alcoolilor și hidrocarburilor ”, Rapoarte săptămânale ale sesiunilor Académie des sciences , vol. 130, 1900, p. 1322-1325 ( citește online )
- (în) „ Premiul Nobel pentru chimie în 1912 ” (accesat la 27 octombrie 2018 ) .




